导读:
近日,北京大学焦宁教授团队利用硒蒽试剂介导的新策略,成功实现烯烃到炔烃的直接转化。该方法可兼容多种离去基团和敏感官能团,并用于分子的后期编辑。该方法不仅提升了炔烃的可及性,还拓展新转化空间,如通过炔烃中间体实现Z/E构型反转,或在Z/E混合物中选择性转化E-烯烃。
“Direct conversion from alkenes to alkynes
Junhong Meng (蒙骏鸿), Yiqi Liang (梁亦奇), Ruilin Xu (徐瑞麟), Zengrui Cheng (程增瑞), Yilei Huang (黄祎磊), Hongwei Shi (石宏伟), Yichi Chen (陈奕驰), Xi Wang (王曦), Jialiang Wei (魏佳良), Teng Wang (王腾), Binzhi Zhao (赵斌治) & Ning Jiao (焦宁)*
Nature 2026. DOI: 10.1038/s41586-026-10372-3”
正文
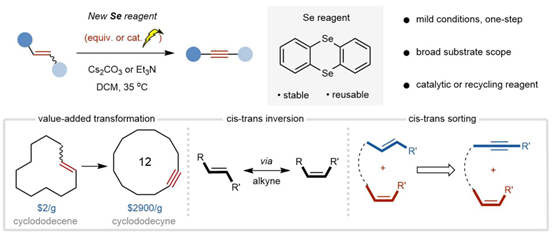
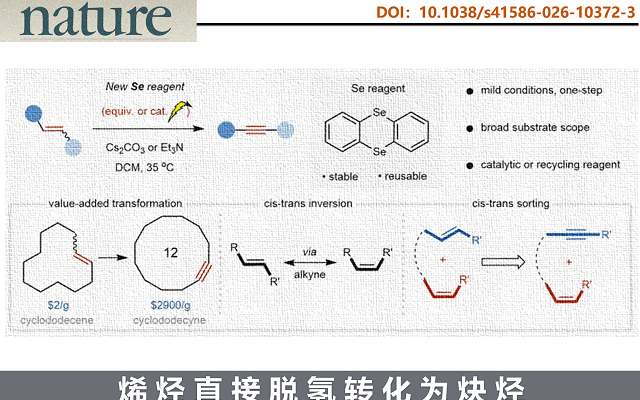
炔烃不仅是药物、材料和复杂分子合成中的基础单元,还是具有广泛用途的结构单元。尽管目前烯烃来源丰富、应用广泛,直接将烯烃直接脱氢转化为炔烃是一种直接高效的策略。此转化不仅可实现分子骨架的精准编辑,如将弯曲的烯烃转化为线性炔烃,能够快速获得结构类似物,并能显著增强生物活性。相比之下,炔烃的合成可及性远低于烯烃,凸显发展高效烯烃→炔烃转化策略的必要性与紧迫性。现有方法(如1861年提出的卤化-消除法)依赖强碱或高温,官能团耐受性差,无法用于后期编辑。其中,根本难点在于:热力学上不利的脱氢过程,以及需选择性活化更强的乙烯基C–H键(而非更易反应的烯丙基C–H键)。自1861年以来,寻求一种温和且通用的策略将烯烃转化为炔烃仍然是百年以来难以逾越的鸿沟。
近日,北京大学焦宁教授团队利用硒蒽试剂介导的新策略,成功实现烯烃到炔烃的直接转化。该方法可兼容多种离去基团和敏感官能团,并用于分子的后期编辑。该方法不仅提升了炔烃的可及性,还拓展新转化空间,如通过炔烃中间体实现Z/E构型反转,或在Z/E混合物中选择性转化E-烯烃。相关文章发表于Nature上。
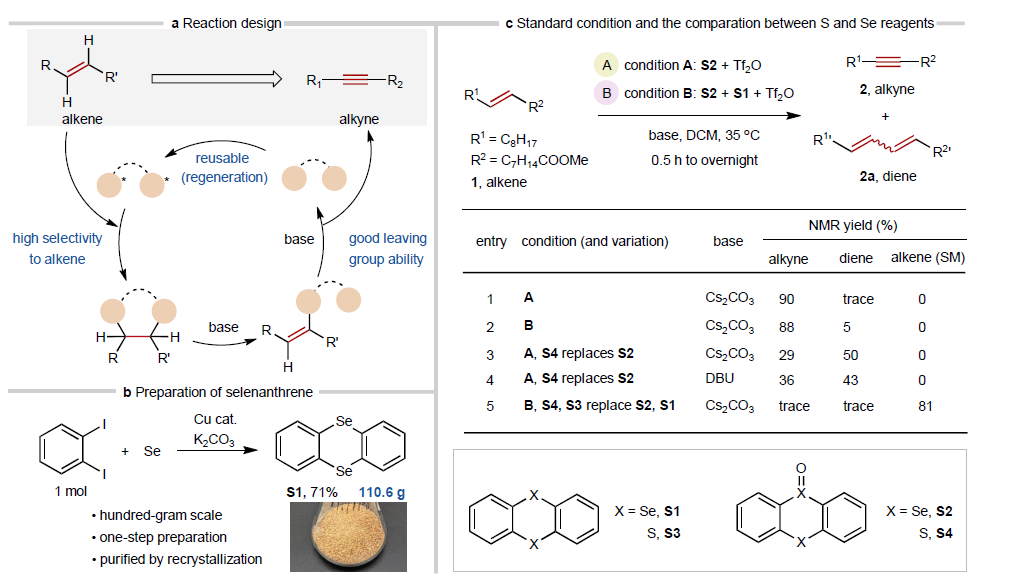
Fig. 1 | Reaction design and conditions.
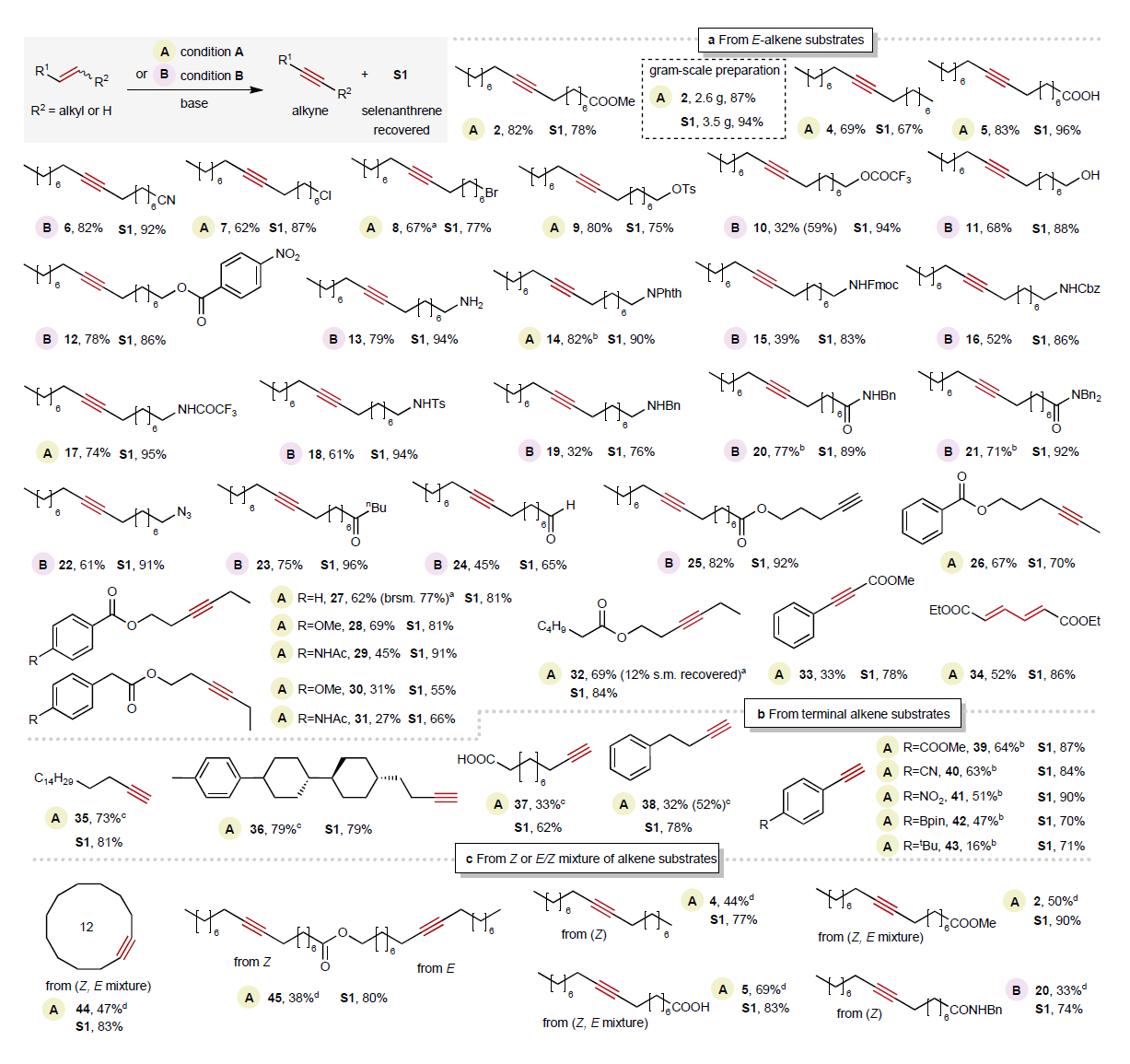
Fig. 2 | Substrates.
受硒试剂高反应性和噻蒽易环加成、可再生特性的启发,作者设计并合成了一种新型硒蒽环(S1)及其氧化物(S2)。S1可百克级规模一步合成并重结晶纯化(Figure 1b);S2在烯烃→炔烃转化中表现优异(Figure 1c)。基于S2/Tf₂O体系生成活性硒物种中路径的差异,作者建立可两种反应条件:条件A(不加额外S1)操作简便,适用于氧化敏感或易发生H-攫取的底物;条件B(加入化学计量S1)适用性更广,兼容复杂官能团分子。最优条件是CH₂Cl₂或MeCN中,以Cs₂CO₃等温和碱、35°C反应,E-烯烃高选择性转化为炔烃(80–90% yields)(Figure 1c,entries 1-2)。对照实验表明:未修饰噻蒽主要生成共轭二烯;而S2衍生的活性物种反应更快、选择性更高。碱的选择显著影响产物分布——弱无机碱(K₂CO₃、CH₃COOK)和有机碱(Et₃N、DBU)利于炔烃生成,吡啶则倾向生成二烯。
在最优条件下,作者对底物的兼容性进行了研究,如Figure 2所示。即该方法可兼容多种难以耐受的官能团,如卤素(7、8)、磺酸酯(9)、Fmoc(15)、三氟乙酸酯(10)、三氟乙酰胺(17)和环氧化物(44)(Figure 2a)。同时,硒试剂对烯烃的高选择性也使其能够与活性基团兼容,如羧酸(5)、胺(13)、酰胺(20、21)、叠氮(22)、醛(24)和炔烃(25)等活性基团也表现出高选择性(Figure 2a)。富电子芳烃业可耐受,但产率略降(28–31);吸电子取代基则促使副反应发生,主要生成共轭二烯(34),进而证实碱介导的烯丙基质子消除是该路径的关键步骤。此外,E型、Z型及末端烯烃均可高效转化为炔烃:Z型和末端烯烃仅需将碱换为NaOH或KOtBu即可(Figure 2b、2c);E/Z混合物亦能高收率转化(Figure 2c),实现传统方法难以获得的炔烃产物。反应后,活性硒物种定量再生为硒蒽(S1),经m-CPBA氧化可循环使用为S2。
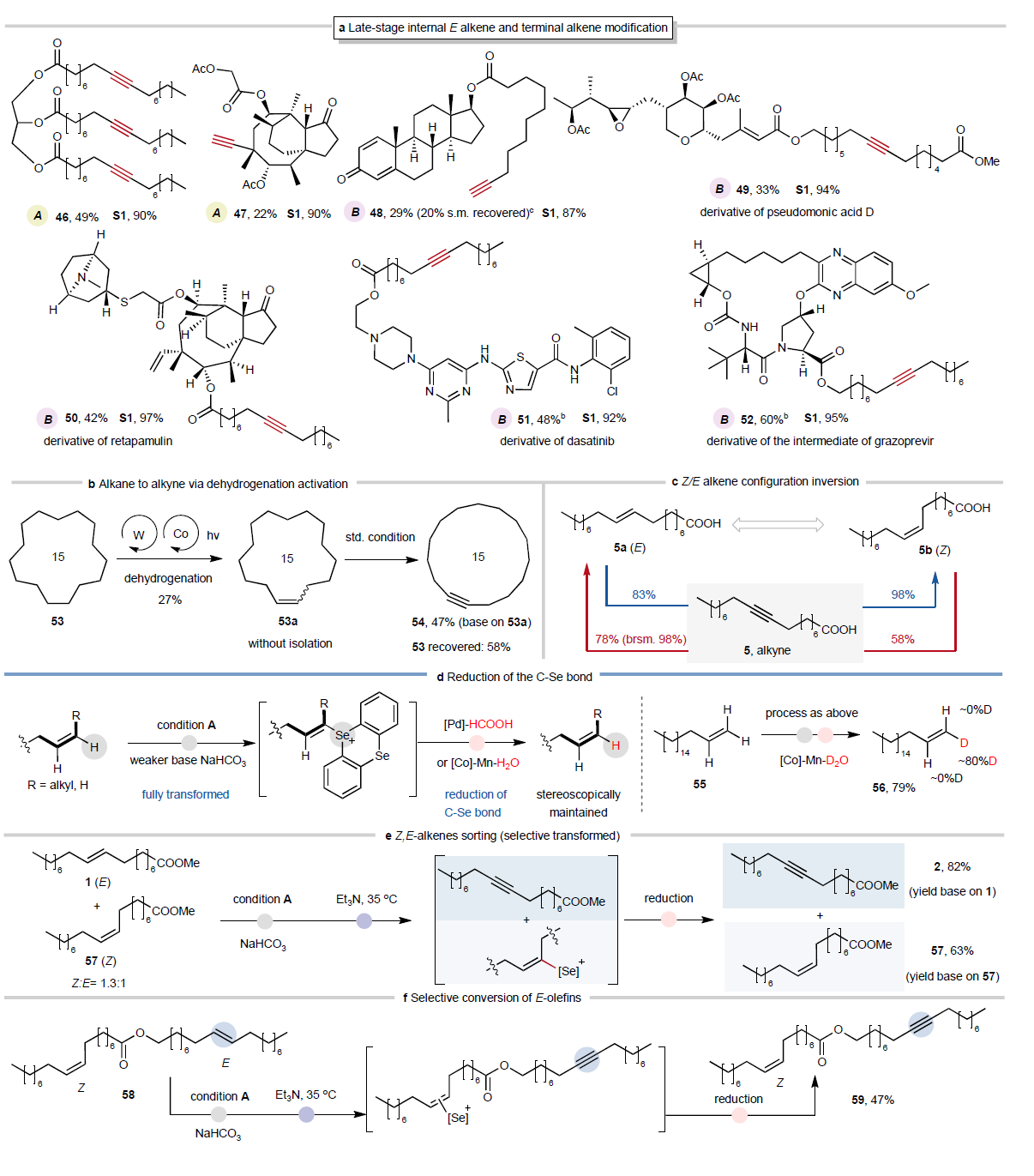
Fig. 3 | Synthetic applications.
接下来,对该方法在复杂分子中后期修饰进行了研究(Figure 3)。即该策略在含有多个烯烃的底物(46)中实现了完全转化,并且能耐受烯酮(48)、不饱和酯(49)和可氧化的硫化物(50)(Figure 3a)。特别的是,在具有空间位阻烯烃的底物中,空间位阻较小的双键被选择性转化(50)。同时,该方法还可兼容多种含氮基团,如达沙替尼衍生物(51)中的胺、嘧啶、噻唑,以及环肽(52)中的吡嗪和多重肽键。进一步将烯烃脱氢和烷烃脱氢结合脱氢→硒化/消除),进而拓展了底物的兼容性(Figure 3b)。此外,该方法还可实现通过炔烃的立体选择性半还原,实现烯烃E/Z构型反转(Figure 3c)。另外一方面,用碳酸氢钠替代强碱,可捕获立体专一的烯基硒蒽盐中间体(Figure 3d):内烯烃产物保持原构型;末端烯烃专一生成E型产物(Figure 4a)。此特点显著优于传统卤化-消除法(常破坏内烯立体化学,且末端烯得E/Z混合物)。特别的是,该烯基硒蒽盐在Pd或Co催化下还原C–Se键为C–H键,定量再生原烯烃构型(Figure 3d);氘标记证实D仅引入C–Se位点(80% D),其余乙烯基位置无氘。 此外,三乙胺选择性促进E-烯烃衍生的硒蒽正离子发生消除,而Z型对应物不反应,从而实现E/Z异构体的化学区分与分离。如将1和57的Z/E混合物(Z:E = 1.3:1)依次用硒试剂、NaHCO3、三乙胺和还原剂处理,可选择性生成炔烃2(82%),并通过Z-衍生的中间体再生Z-烯烃(63%)(Figure 3e)。该策略同样适用于分子内体系,在底物58中,Z-烯烃得以保留,而E-烯烃取代基则被选择性引入炔烃产物(Figure 3f)。
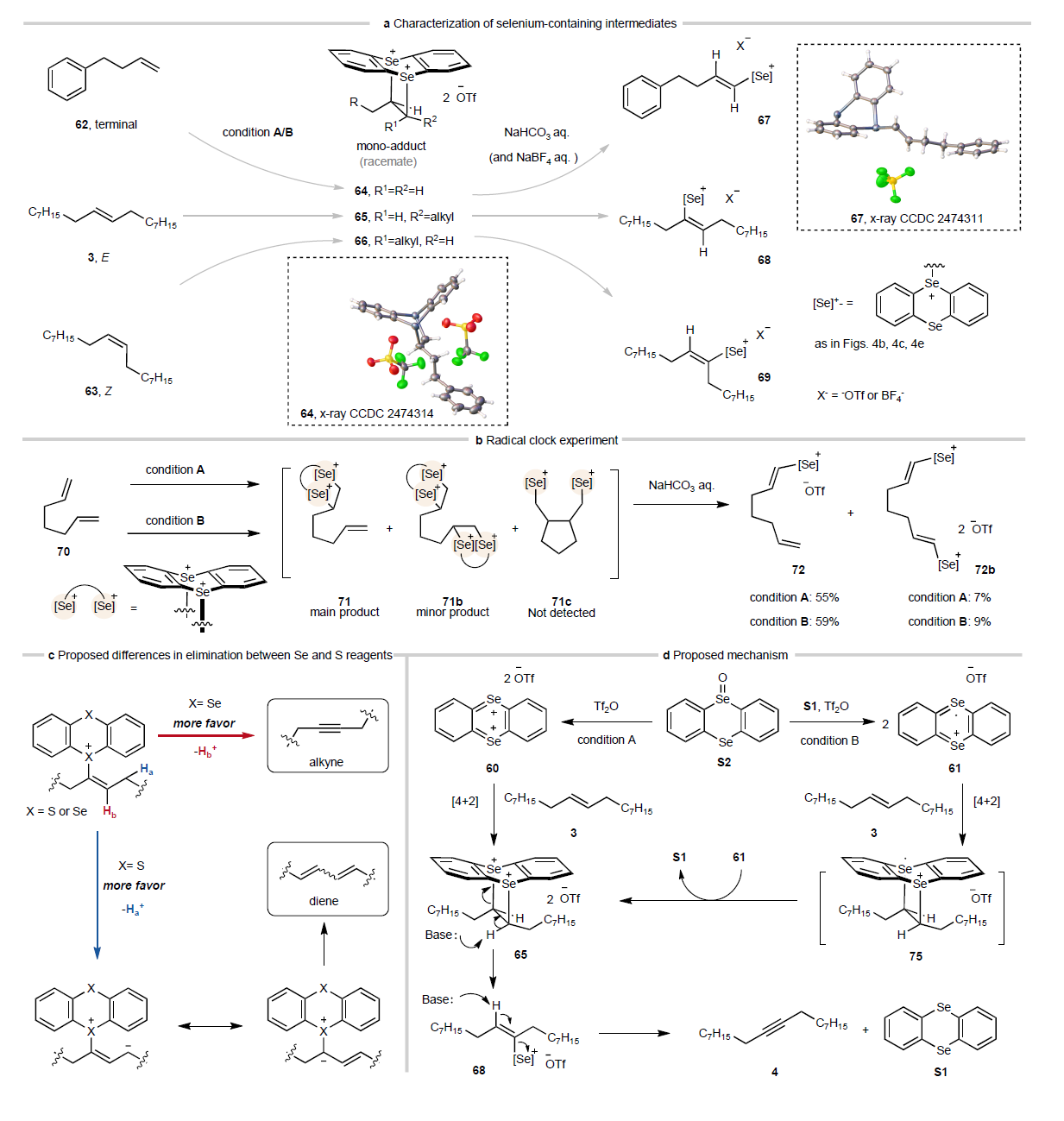
Fig. 4 Mechanistic study.
最后,作者通过一系列实验对反应机理进行了研究。即1)机理研究表明不同条件下生成两类明确的活性硒物种:条件A下为硒蒽二阳离子60,条件B下为自由基阳离子61。二者均经¹H、¹³C和⁷⁷Se NMR表征;自由基阳离子结构还通过X射线晶体学确认。尽管电子态不同,两种条件下烯烃反应均只生成稳定单加合物64–66作为可检测中间体,并经消除转化为烯基硒蒽盐67–69(Figure 4a);2)自由基时钟实验(1,6-庚二烯)未检出环化产物(Figure 4b,图S33–S41),排除逐步自由基路径。此外,活性硒物种与苯炔反应生成中等产率的阳离子三苯并环辛烯类似物74,证实其可参与环加成,并将适用范围拓展至烯烃以外;3)对比硫试剂,硒试剂更有利于炔烃而非二烯生成(Figure 4c)。此源于硫鎓离子更强的碳负离子稳定能力,使其衍生的烯基硫鎓盐更易发生烯丙基质子消除——该副反应在硒体系中被显著抑制。 综上所述,作者提出了合理的反应机理(Figure 4的):在条件A下,硒蒽-5-氧化物(S2)与Tf₂O反应生成亲电性二价阳离子60,与烯烃发生[4+2]环加成得中间体65;在条件B下,过量硒蒽S1存在时生成自由基阳离子61,其与烯烃环加成得75,再经61单电子氧化,同样汇聚至65。随后,65在碱作用下连续消除,生成烯基硒蒽盐并最终得到炔烃,同时再生硒S1。
总结
北京大学焦宁教授团队利用硒蒽试剂介导的新策略,成功实现烯烃到炔烃的直接转化。该方法可兼容多种离去基团和敏感官能团,并用于分子的后期编辑。该方法不仅提升了炔烃的可及性,还拓展新转化空间,如通过炔烃中间体实现Z/E构型反转,或在Z/E混合物中选择性转化E-烯烃。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841
请登陆TCI试剂官网查看更多内容
https://www.tcichemicals.com/CN/zh/



















No comments yet.