作者:石油醚
导读:
近日,Emory University的代明骥教授团队在J. Am. Chem. Soc.上,以 “Convergent and Efficient Total Synthesis of (+)-Heilonine Enabled by C–H Functionalizations” 为题,以11步或13步线性最长步骤完成了天然产物(+)-Heilonine的全合成。其中关键步骤涉及1)C-H官能团化,即Boc-导向C-H锂化/Negishi 交叉偶联(Boc-directed C–H lithiation–Negishi cross-coupling)、钯催化羰基化C-H内酰胺化(palladium-catalyzed carbonylative C–H lactamization)、内酰胺导向铑催化的C-H碘化(lactam directed rhodium-catalyzed C–H iodination)、可见光诱导Na2-Eosin Y催化C-H羟基化 (Na2-Eosin Y-catalyzed visible-light-induced C–H hydroxylation);2)Stille插羰交叉偶联(Stille carbonylative cross-coupling)连接AB环系统和DEF环系统;3)Nazarov环化(Nazarov cyclization)以构建五元环。
“Convergent and Efficient Total Synthesis of (+)-Heilonine Enabled by C–H Functionalizations.
Yuan Jin, Sovanneary Hok, John Bacsa, and Mingji Dai*
J. Am. Chem. Soc., 2024, ASAP. doi: 10.1021/jacs.3c13492”
正文
Heilonine (1)是由日本科学家Koh Kaneko 教授及其同事于1989年从黑龙江省百合科植物Fritillaria ussuriensis Maxim中分离获得[1] (Figure 1),并且其被认为是重要的中草药“贝母”的成分[2](传统中医中用来镇静、止咳和祛痰)。Heilonine (1)是Veratrum甾体生物碱家族成员之一,其成员具有共同得C-nor-D-homo甾体骨架,而根据其与哌啶环(F环)的连接方式可分为三类[3]:cevanine型(1-5)、veratramine型(6,7)和jervine型(8,9)(Figure 1A)。其中,环巴胺(cycloparamine, 7)是最值得注意和研究的一个,其已被鉴定是一种Hedgehog信号通路抑制剂,并且其类似物Patidegib目前正在进行癌症治疗的人体临床试验[4]。
由于Veratrum甾体生物碱的结构多样性、复杂性和治疗潜力。自20世纪60年代以来,Veratrum甾体生物碱引起了科学家极大的关注,如Masamune、 Johnson、 Kutney、Giannis、Baran、高栓虎以及罗佗平等小组均在该方面做出了突出的贡献。目前为止,仅有Rawal和Cassaidy在2021年以21步LLS步骤完成天然产物(+)-Heilonine的全合成 (Figure 1B)[5],其关键步骤设计有机催化不对称Diels-Alder反应以及Rh催化的[2 + 2 + 2]环加成。近日,Emory University的代明骥教授团队,以11步或13步线性最长步骤完成了天然产物(+)-Heilonine的全合成,并发表于J. Am. Chem. Soc.上。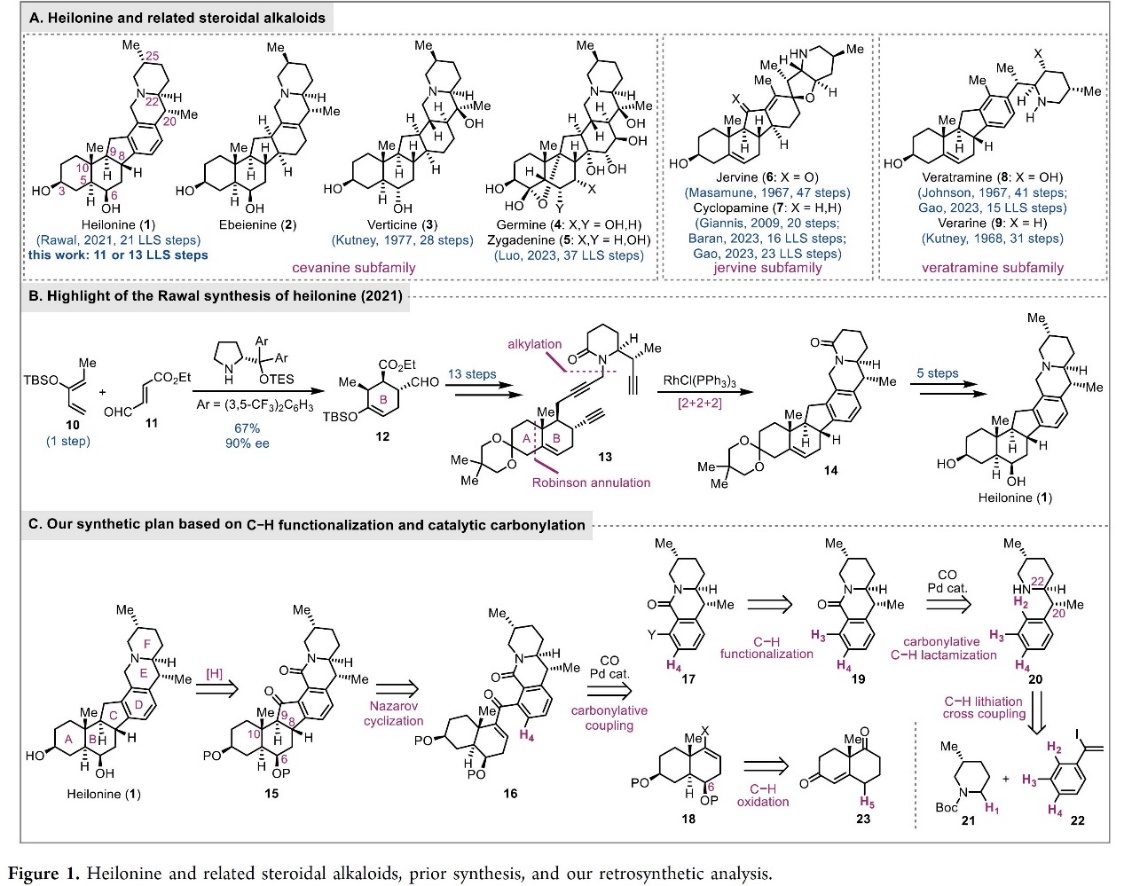
Heilonine是含有芳香D环的cevanine型生物碱,其包含稠合的六环结构以及9个立体中心。基于其特殊的骨架,作者对Heilonine (1)进行了相关的逆合成分析(Figure 1C),即砌块21和22经Boc-导向C-H锂化/交叉偶联合成中间体20,20通过钯催化羰基化C-H内酰胺化构建合成子19。随后,19经过C-H官能团化构建中间体17。同时,23经过C-H羟基化合成中间体18。其次,17和18通过钯催化羰基化合成关键中间体16,16经Nazarov环化(Nazarov cyclization)以构建五元环中间体15。最后,15通过羰基还原完成Heilonine的全合成。
天然产物Heilonine的全合成步骤,如Scheme 1所示。
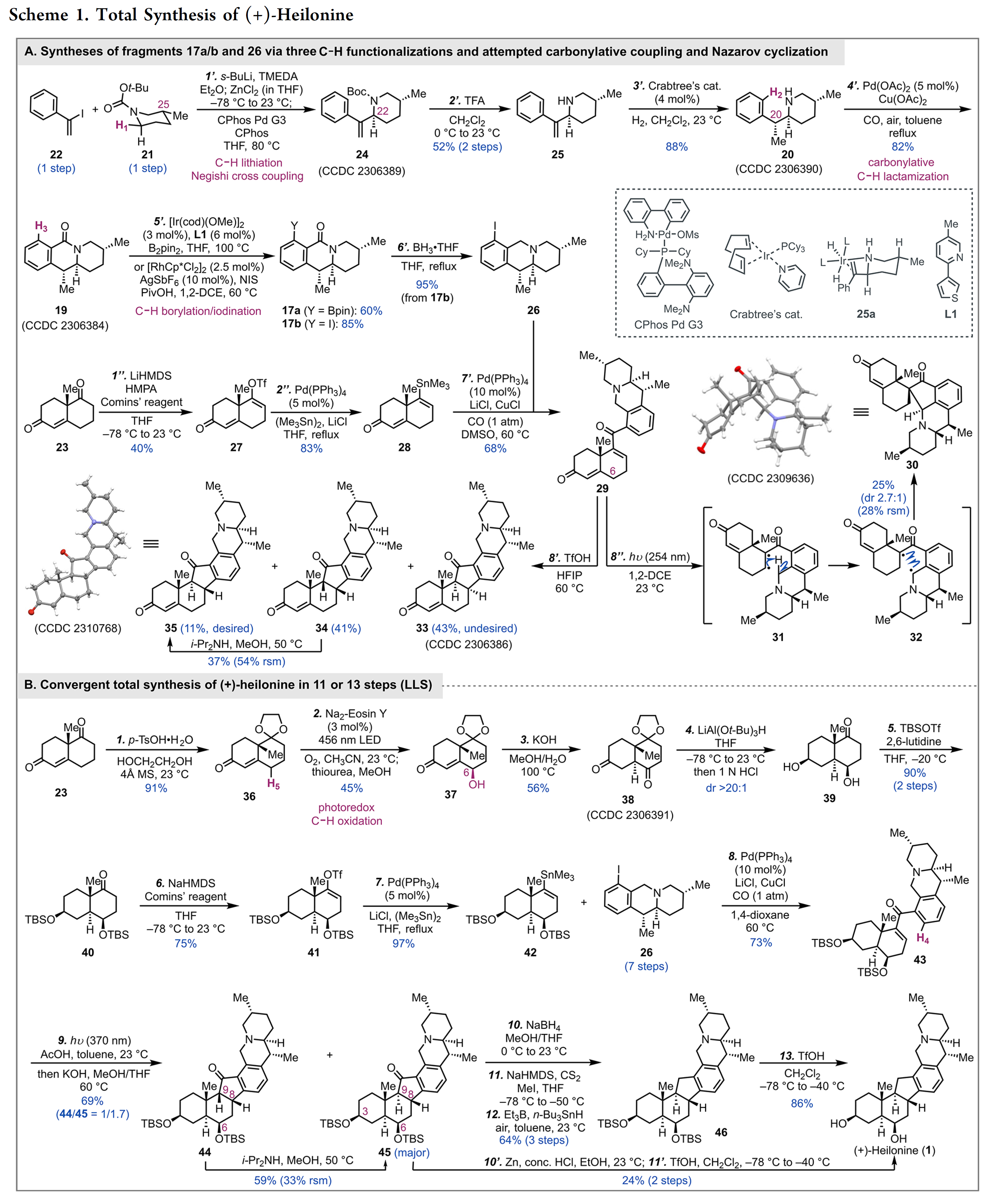

总结,代明骥教授团队以11步或13步线性最长步骤完成了天然产物(+)-Heilonine的全合成。其中关键步骤涉及1)C-H官能团化,即Boc-导向C-H锂化/Negishi 交叉偶联(Boc-directed C–H lithiation–Negishi cross-coupling,)、钯催化羰基化C-H内酰胺化(palladium-catalyzed carbonylative C–H lactamization)、内酰胺导向铑催化的C-H碘化(lactam directed rhodium-catalyzed C–H iodination)、可见光诱导Na2-Eosin Y催化C-H羟基化 (Na2-Eosin Y-catalyzed visible-light-induced C–H hydroxylation);2)Stille-插羰交叉偶联(Stille carbonylative cross-coupling)连接AB环系统和DEF环系统;3)Nazarov环化(Nazarov cyclization)以构建五元环。
参考文献:
- [1] Y. Kitamura, M. Nishizawa, K. Kaneko, M. Shiro, Y.-P. Chen, H.-Y. Hsu, Tetrahedron 1989, 45, 7281. doi: 10.1016/S0040-4020(01)89188-2.
- [2] Q.-W. Jiang, M.-W. Chen, K.-J. Cheng, P.-Z. Yu, X. Wei, Z. Shi, Med. Res. Rev. 2016, 36, 119. doi: 10.1002/med.21346.
- [3] H.-J. Li, Y. Jiang, P. Li, Nat. Prod. Rep. 2006, 23, 735. doi: 10.1039/B609306J.
- [4] J. K. Chen, Nat. Prod. Rep. 2016, 33, 595. doi: 10.1039/C5NP00153F.
- [5] H. Shao, W. Liu, M. Liu, H. He, Q.-L. Zhou, S.-F. Zhu, S. Gao, J. Am. Chem. Soc. 2023, 145, 25086. doi: 10.1021/jacs.3c10362.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
















No comments yet.