本文作者:竹悠
导言
Cp*Co(III)催化的喹啉氮氧化物C-8位二烯化反应。反应经过钴催化的喹啉氮氧化物的C-H活化,区域选择性迁移插入联烯,再经β-氧消除完成二烯化反应。这种选择性C-H活化具有优秀的选择性,并且条件温和,另外发现添加30mol%的NaF是反应关键。反应具有较强的官能团兼容性,并且可以实现克级规模反应。
正文
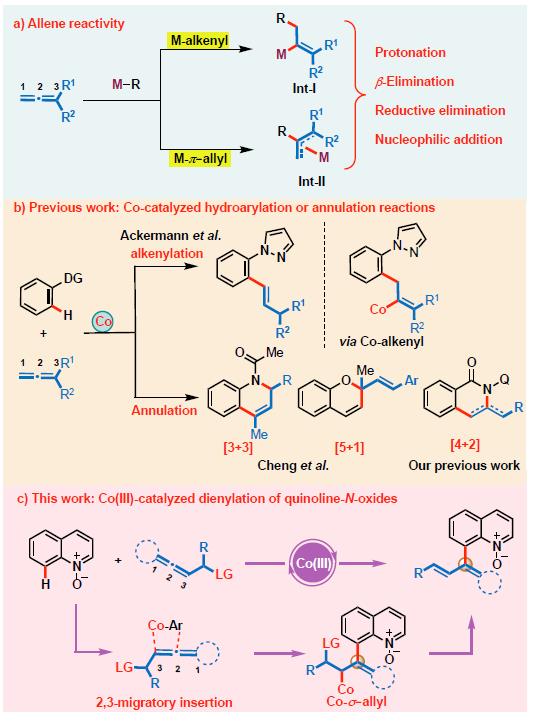
联烯是有机合成中重要官能团,可以用于环合和偶联反应。近年来,联烯作为耦合配体,同时也作为过渡态金属催化的C-H活化反应中热点。联烯中有两个正交的双键,增加了反应的区域和化学选择性挑战,但也是快速构建复杂结构的有效手段。例如,根据联烯中的立体-电子本性,选择合适的金属催化剂M,C-H活化后生成有机金属中间体R-M,可以有两个迁移插入途径(Scheme 1a)。R-M进行1,2-插入联烯得到的Int-Ⅰ,插入C2=C3得到π-烯丙基中间体Int-Ⅱ。两个中间体都是高度活泼,可以发生多种反应,如质子化、β-消除、还原消除、Tsuji-Trost亲核加成等。
目前常用的过渡态金属多为第三排的过渡态金属如Ir(III), Rh(III), Ru(II) 和Pd(II)。而第一排的钴金属廉价、含量多,同时具有更高的路易斯酸性和较好的选择性,尤其适合作为环境友好的催化剂。如Ackermann的C-H烯化反应,Cheng的[3+3]和[5+1]环合反应。以及作者报道的,以酰胺为导向基团,和联烯反应的[4+2]环合反应。反应通过Co-s-allyl络合物,钴中间体区域选择性插入到联烯中的C2=C3双键中(Scheme 1b)。
1 反应设计
在本文中,作者延续之前的研究,进一步理解反应机理、拓展应用范围,在联烯的烯丙基位置上引入离去基团,以便进行消除反应,完成催化的双烯化反应。论文发表在Angew. Chem. Int. Ed.上。
Chandra M.R Volla, Rahul K. Shukla, Akshay M. Nair, and Salman Khan,
Cobalt-catalyzed C8-Dienylation of Quinoline-N-oxides
Angew. Chem. Int. Ed. DOI: 10.1002/anie.202003216
Scheme 1 联烯用于偶联反应总览
喹啉是药物化学和有机合成化学中的重要芳香杂环,C2位上的氢具有酸性易于衍生,但C8位却极少报道。若将其氮氧化后,可改变了电子效应使C-8位活化。因此,作者期望钴-烯丙基络合物进行区域选择性2,3-迁移插入到联烯中,再进行氧消除反应,生成二烯,如(Scheme 1c)所示。
2 优化离去基团
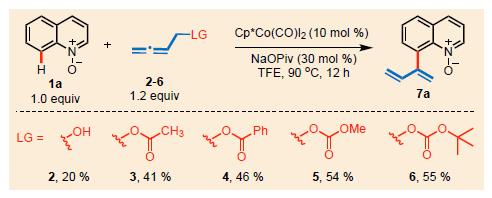
作者首先以含有羟基的联烯2尝试反应,使用Cp*Co(CO)I2、30 mol%的NaOPiv在TFE溶剂中90℃反应12h,得到产物7a(20%)。继续实验发现,醇进行酯化后收率提高,其中碳酸酯5和6的收率相当,在55%左右,Scheme 2所示。
Scheme 2优化离去基团
3 优化反应条件
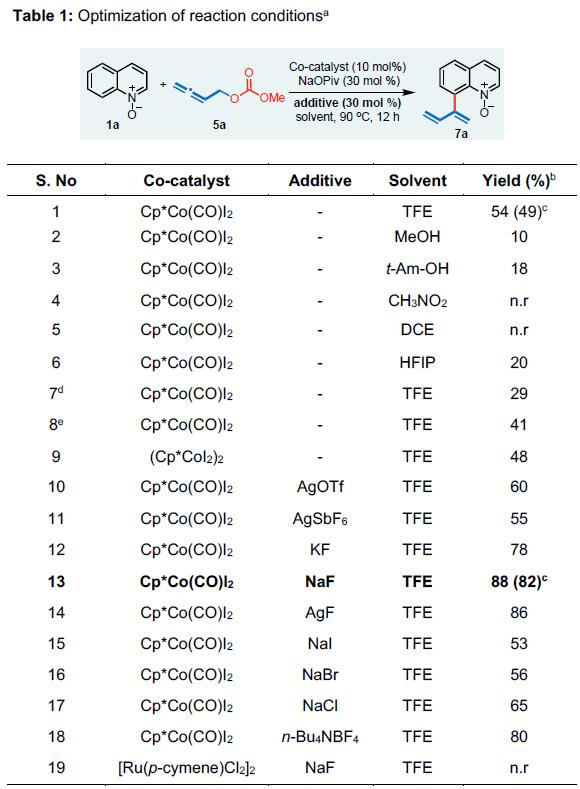
为获得理想收率,对反应溶剂等进行筛选,如表1所示的MeOH, DCE, HFIP(entries 1-6),碱(entries 7-8),银盐AgOTf、AgSbF6(entries 10-11),氟化物KF、NaF(entries 12-13),以及其他添加物(entries 14-18)。最优化的条件为:1当量的N-氧化物1a,1.3当量的5a,10mol%的钴催化剂Cp*Co(CO)I2,30mol%的碱NaOPiv,30mol%添加物NaF,反应溶剂为TFE,温度为90℃,产物7a的收率为82%。
4 底物扩展
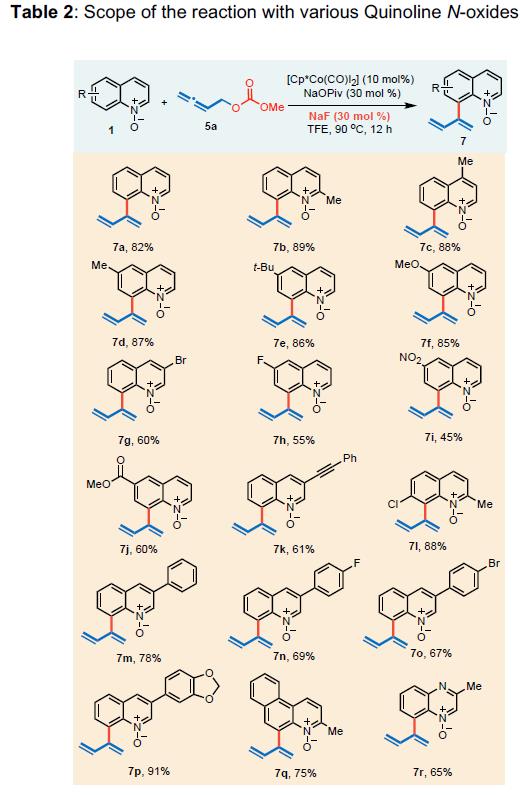
得到优化反应条件后,考察了不同结构的喹啉-N-氧化物,如烷基取代,不同电子效应,均可以得到产物,收率范围为45-91%,如表2所示。
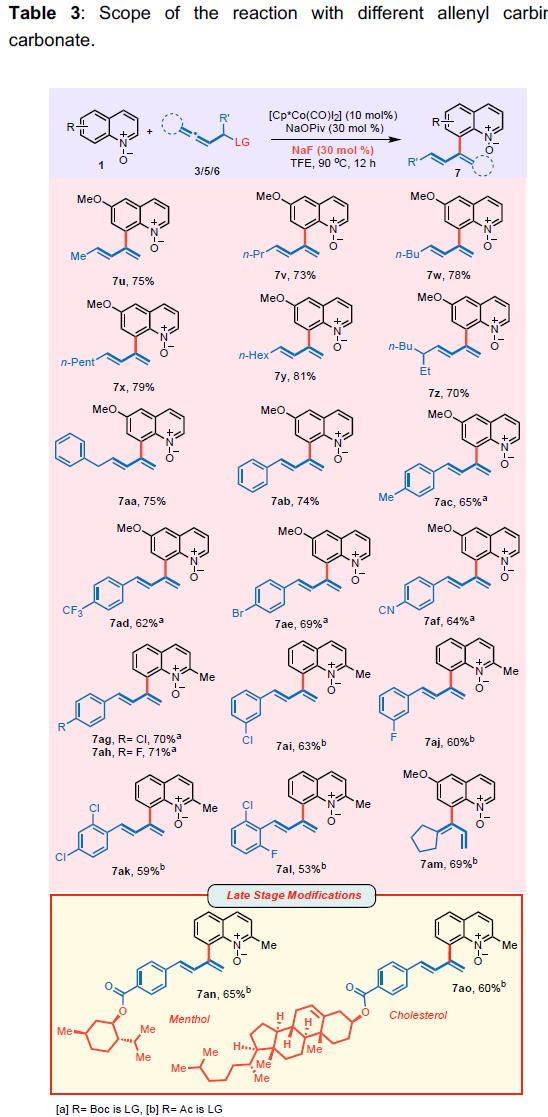
并考察了不同的联烯碳酸酯,收率范围为53-79%,并可以进行复杂化合物的后期修饰,如表3所示。
5 继续衍生
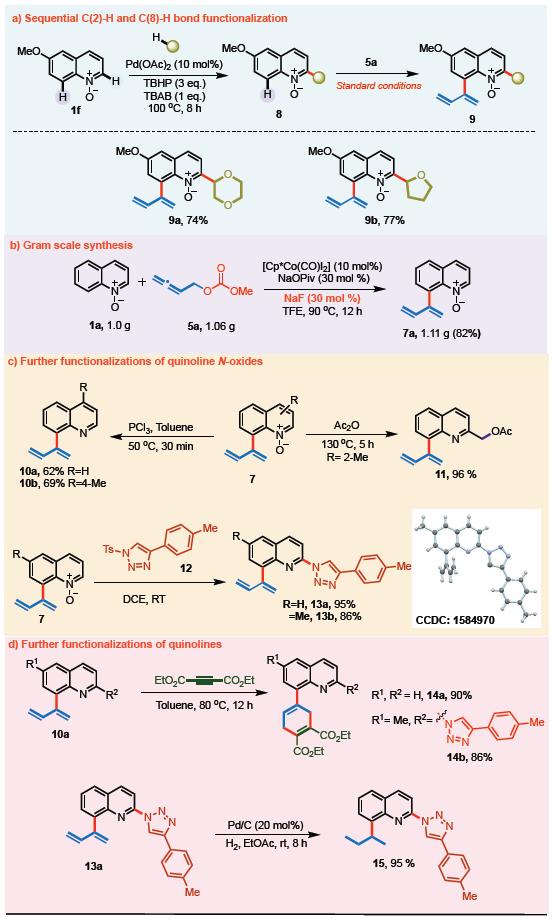
喹啉-N-氧化物可以先进行2位衍生,再在标准条件下进行8位衍生,分别得到产物9a和9b。反应也可以扩大规模到克级别,1g喹啉-N-氧化物可生成1.11g产物7a,收率为82%。产物7可继续进行反应,如与PCl3生成10a和10b;醋酸酐下生成乙酰化产物11;与三氮唑进行偶联得到13a和13b。二烯可进行化合反应或者还原反应,Scheme 3所示。
Scheme 3 继续衍生
6 反应机理研究
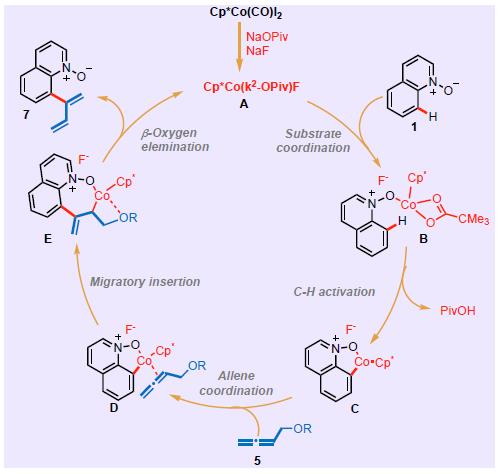
通过H/D交换反应及对照实验,作者认为反应机理如Scheme 4所示:首先Cp*Co(CO)I2在NaOPiv和NaF作用下生成活化的Co(Ⅲ)络合物A,与喹啉-N-氧化物1络合,受氧影响,在C-8选择性C-H活化得到C。联烯5参与钴的配位,选择性插入到C2=C3双键中,得到中间体E,发生β-氧消除,生成产物7。
Scheme 4 可能的反应机理
总结
本文首次报道了钴催化的喹啉氮氧化物的C-8位选择性二烯化反应,以联烯碳酸酯为二烯化试剂,实现了多种底物的反应,拓展了喹啉类衍生物的合成方法和联烯在C-H活化中的作用。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!




















No comments yet.