本文作者 芃洋雪
从天然产物中获取灵感,设计新药一直是药物化学中长盛不衰的话题。大自然的鬼斧神工创造了多种多样的天然产物,结构的丰富多姿,令新药设计者也自愧弗如,但天然产物的结构复杂、密集、多环、多手性中心等特点,使其大规模合成较为困难。
从化学上来看,快速有效的合成高价值复杂化合物的途径有两条:
1.从多个简单合成砌块起,构建复杂母体结构。
2.从复杂的母核起,构建分子多样性,即从复杂到多样complexity-to-diversity (CtD)策略。
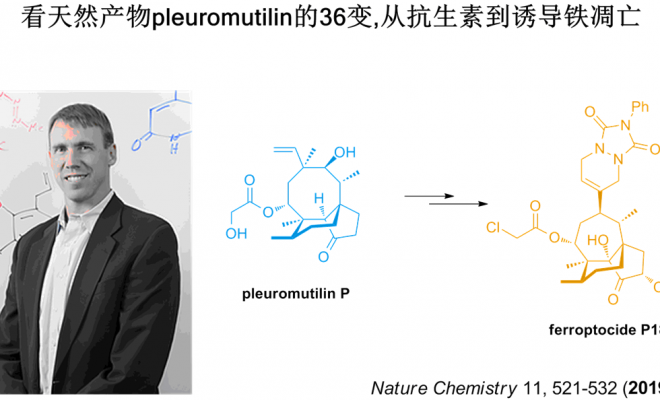
来自 University of Illinois的Paul J. Hergenrothe等,以天然产物pleuromutilin(截短侧耳素)为起点,通过CtD策略制备了多类化合物,筛选它们的抗癌活性,并探究作用模式,在这一系列衍生物中,发现了化合物 ferroptocide,它能快速诱导癌细胞死亡。
Diverse compounds from pleuromutilin lead to a thioredoxin inhibitor and inducer of ferroptosis
Evijola Llabani, Robert W. Hicklin, Hyang Yeon Lee, Stephen E. Motika, Lisa A. Crawford, Eranthie Weerapana & Paul J. Hergenrother
Nature Chemistry , 2019, 11, 521–532. doi.org/10.1038/s41557-019-0261-6
结构衍生
Pleuromutilin为二萜类化合物,存在于多种真菌中,是种强效的细菌50S核糖体抑制剂。一些半合成的P衍生物被用做抗生素抗革兰氏阴性菌和一些阳性菌。从结构上看,P具有五、六和八元环,以及8个连续的手性中心。得益于先前对于pleuromutilin的抗菌活性研究,如构型关系、结构阐释、合成信息等,可以方便的对P进行的结构衍生,衍生化合物结构如图1所示:
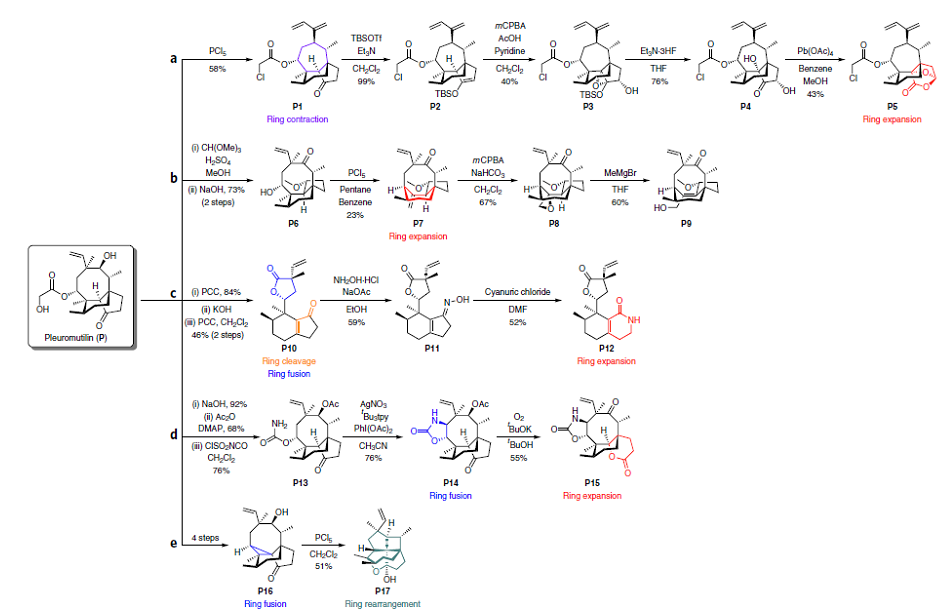
图1. Pleuromutilin的结构衍生策略.图片来源:Nature Chemistry.
经过PCl5和羟基反应,碳离子重排以及缩环得到重用的二烯衍生物P1。P1再通过硅烷化、环氧化、脱硅烷、以及氧化裂解、内酯化和重排反应得到P5。
经酸催化的异构化反应和1,5氢迁移得到醇P6,和PCl5反应新成一个六元环,消去后生成骨架P7,再经环氧化、消除、开环反应等得到P9.
P的八元环断裂得到内酯P10,然后生成肟P11,经三聚氰酸作用下发生Beckmann重排反应得到扩环后的P12。
氨基甲酸酯P13通过银催化发生分子内氮宾插入反应生成新的环化合物P14,然后再碱金属自动氧化下生成内酯P15。以及之前获得的氧桥窗烷化合物P17。
生物活性研究
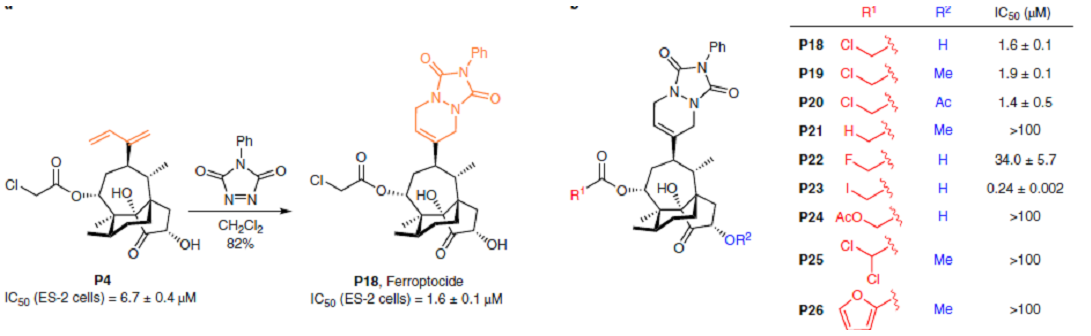
以卵巢癌ES-2 为例,进行抗肿瘤活性筛选,化合物P4脱颖而出,IC50为6.7μM 。P4进行[[4+2]环加成反应,得到P18,即 ferroptocide。它的效果更好, IC50=1.6 μM。
构效关系表明,醇羟基和α-氯酯基对活性影响较大,这些结构和活性如图2所示,只有碘代物P23的活性更高。
图2. 化合物结构及IC50值. 图片来源:Nature Chemistry.
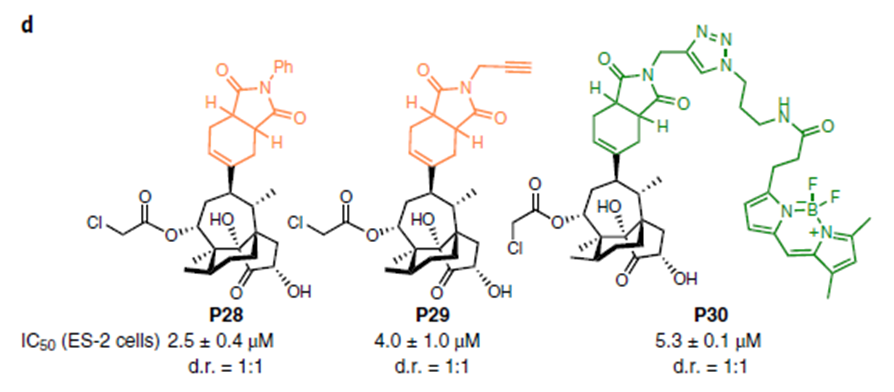
与pleuromutilin不同,先导化合物ferroptocide没有抗微生物活性,但具有抗几十种肿瘤细胞的活性,活性优于5-氟尿嘧啶,依托泊苷,PAC-1等。将ferroptocide中的N-N键替换为C-C键,即化合物P28,活性没什么损失,也由此得到了工具化合物P29,它具有炔烃基团,可以发生1,3偶极环加成反应即click反应,得到有荧光性质的P30,进行亚细胞定位,这两个化合物也有类似的活性。
图3. Ferroptocideh结构衍生及IC50值. 图片来源:Nature Chemistry.
接下来,对ferroptocide的药理进行研究。ferroptocide杀死多种肿瘤细胞的速度很快, 如杀死半数ES-2 胞的时间为1h,说明ferroptocide不诱导细胞凋亡,细胞周期分析也证明了这一点。透射电子显微镜监测ferroptocide处理后的细胞形态变化,也没有出现细胞膜起泡、染色质凝聚等凋亡现象,但发现了线粒体肿胀现象,说明ferroptocide可能作用于线粒体。线粒体中产生活性氧ROS,可以荧光探针监测ROS含量来验证。实验表明,ferroptocide在ES-2 细胞中的表现与阳性对照ertbutylhydroperoxide (TBHP)、butyl hydroperoxide (TBHP)等类似,这说明,ferroptocide扰乱了线粒体的活性。
这些现象,可能与ferroptosis有关,ferroptosis是一种新型的细胞死亡方式,是铁依赖的脂质过氧化累积介导的细胞死亡,特征是出现脂质过氧化物以及一些细胞保护作用。Ferroptosis引起活性氧ROS,可以通过荧光探针C11-BODIPY监测,而ferroptocide在 ES-2 ,HCT 116 以及4T1 细胞中的表现和其他ferroptosis诱导剂类似,而且ferroptocide的作用更迅速,稳健。
在转录水平的研究中, RNA–seq 基因测序发现 GCLC (3.5倍), GCLM (4.9倍), SLC7A11(8.1倍) 和CHAC1 (9.8倍)等基因上调,同时内质网应激也上调,内质网中的其他蛋白也受到影响,这些现象都指向了氧化应激和 ferroptosis。
构效关系发现, ferroptocide 的生物活性和 α氯酯的亲电性相关,可能与靶标的共价修饰有关。在体外Ferroptocide可以和谷胱甘肽反应,在肿瘤细胞中,Ferroptocide与类似物发生竞争性反应。炔烃衍生物P29用于生物素-链霉亲和素系统实验,筛选了9种蛋白,首先排除了GPX4蛋白。为区分在靶和脱靶细胞毒性相关靶标,采用siRNA 和CRISPR–Cas9技术,又排除了KEAP1 和GSTO1 通路。(PTGES2, PGLS, TXNRD1, TXNRD2, TXNRD3 和 PDP1也不是靶蛋白,剩下的仅有硫氧还蛋白。
硫氧还蛋白Thioredoxin (TXN) 是一种广泛存在的氧化还原酶,具有维持生物体内氧化还原平衡和调控生物信号传导等功能,它和硫氧还蛋白还原酶(thioredoxin reductase),NADPH构成了硫氧还蛋白系统。TXN的活性源自两个半胱氨酸(C32和C35)用于还原二硫键。晶体结构显示Ferroptocide共价修饰硫氧还蛋白的关键活性部位C73S氨基酸,抑制了细胞中的活性,导致细胞内的氧化平衡失调,产生过多的ROS和脂质过氧化,最终使细胞死亡。抑制能力高于其他抑制剂如 PMX464 和PX-12。
本文通过从复杂到多样complexity-to-diversity (CtD)策略,合成了一系列天然产物pleuromutilin(截短侧耳素)衍生物,发现化合物Ferroptocide具有快速诱导ferroptosis的作用,导致肿瘤细胞死亡,这些发现,使pleuromutilin类衍生物,不必局限于抗生素研究,还可能用于抗肿瘤药物,拓展了应用领域。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!





















No comments yet.