作者:石油醚
导读:
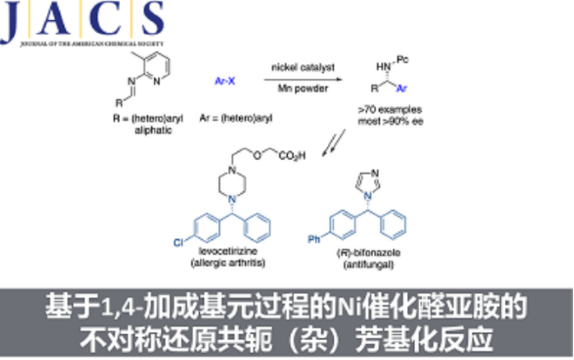
近日,北京大学深圳研究生院周建荣课题组以商业易得或易于制备的(杂)芳基卤化物和芳基磺酸酯为(杂)芳基化亲电试剂,通过一价芳基镍为关键物种的1,4-基元加成过程,实现了金属镍催化不对称亚胺的还原(杂)芳基化反应。相关成果近期发表在J. Am. Chem. Soc.上(DOI: 10.1021/jacs.3c00548)。
“Nickel-Catalyzed Enantioselective Reductive Arylation and Heteroarylation of Aldimines via an Elementary 1,4-Addition。 Luoqiang Zhang, Xiuhua Wang, Maoping Pu, Peng Yang, Yun-Dong Wu, Yonggui Robin Chi and Jianrong Steve Zhou*
J. Am. Chem. Soc.2023, ASAP. DOI: 10.1021/jacs.3c00548
正文:
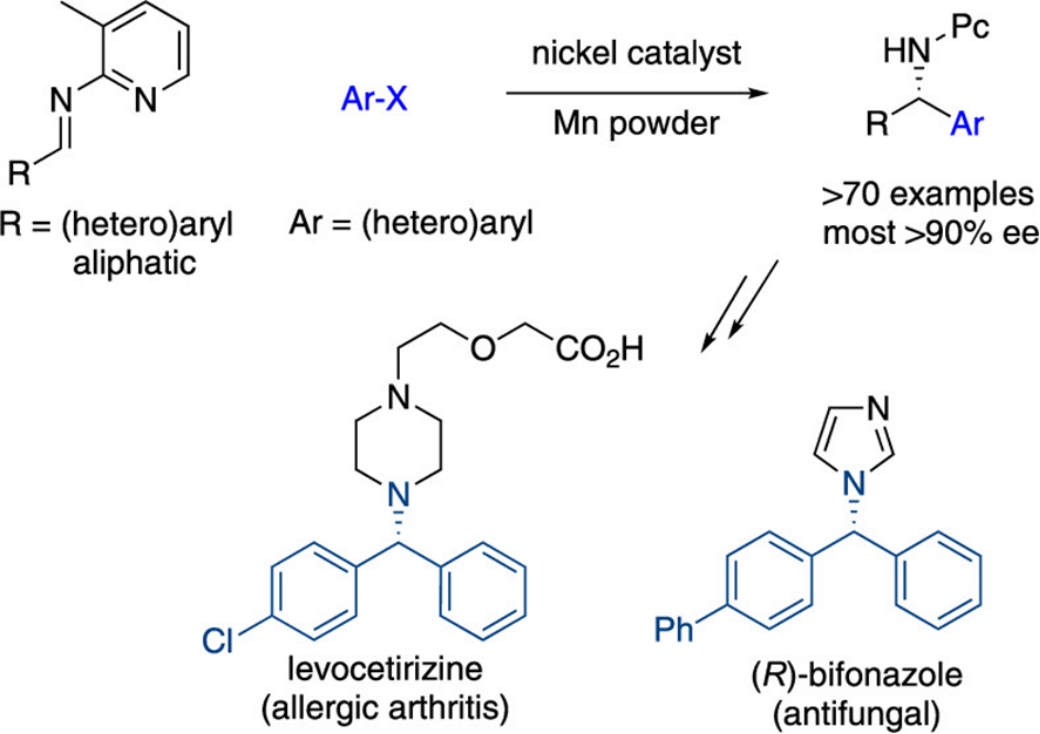
目前,市售的小分子药物中约40%含有烷基胺结构,尤其是手性苄胺和二芳基甲胺骨架出现频繁。发展高效新方法来立体选择性合成这些手性胺骨架一直是合成化学家们的兴趣所在。在众多方法中,贵重金属(如铑、钯)催化的芳基硼试剂对亚胺的不对称加成反应被广泛研究并取得长足发展。
近日,北京大学深圳研究生院周建荣课题组以商业易得或易于制备的(杂)芳基卤化物和芳基磺酸酯为(杂)芳基化亲电试剂,通过一价芳基镍为关键物种的1,4-基元加成过程,实现了金属镍催化不对称亚胺的还原(杂)芳基化反应。相关成果近期发表在J. Am. Chem. Soc.上(DOI: 10.1021/jacs.3c00548)。
在模板反应中,N-3-甲基-2-吡啶基(Pc)醛亚胺1a和溴苯2a以 100%的产率和97% ee得到芳基化产物(图1)。最优条件包括,NiBr2(DME)(5 mol%)和手性tBu-pyrox L1(6 mol%)作为催化剂,锰粉作为还原剂在DMF中室温下反应24小时。 当4-吡啶基、苯基、苄基或对甲苯磺酰基作为醛亚胺N-保护基时,在最优条件下未检测到芳基化产物生成。
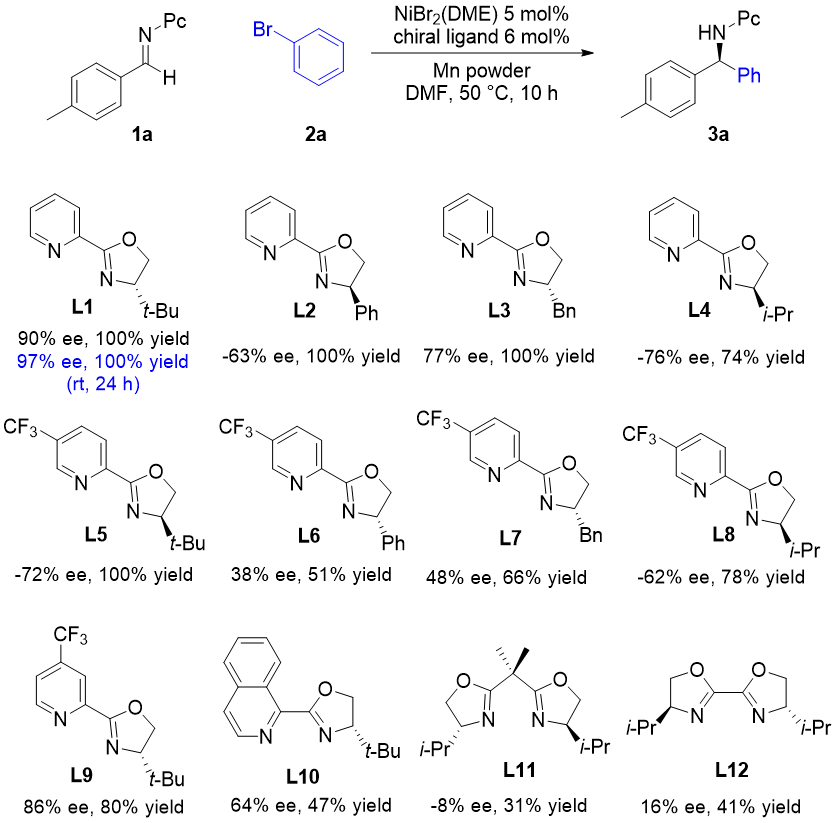
图1. 手性配体筛选
在得到最优条件后,作者对溴代(杂)芳烃的适用范围进行了考察(图2)。结果显示,无论是供电性还是吸电性的官能团都能被很好的兼容。醇(3i),酰胺(3m, 3r-s)、氯(3o)、醛(3t)、酮(3u)、酯(3v)、氰基(3w)、硼酸酯(3x)等敏感性基团也都能很好的兼容于该反应体系。此外,溴代杂芳环,如苯并呋喃、苯并噻吩、吲哚、喹啉、吡啶和吡啶酮,也都是适用的底物。
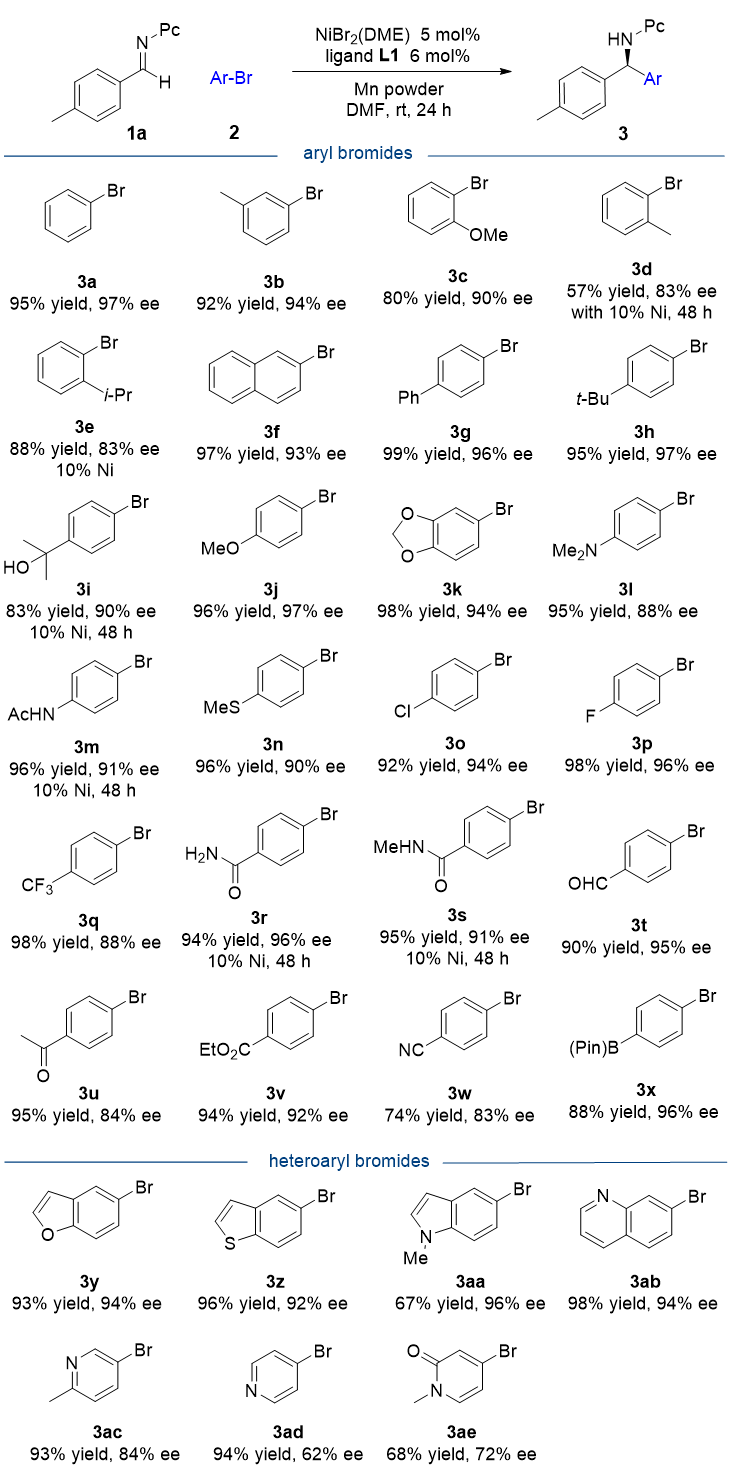
图2. 溴代(杂)芳环底物范围考察
除了(杂)芳基溴化物外,作者还对其他亲电芳基化试剂进行了探索(图3)。结果发现,相比于芳基溴,芳基碘的反应较慢。当碘苯与醛亚胺1a反应48小时后,只能得到70%产率的产物。后来发现加入一当量的NaBr能加速反应进程。缺电基团取代的芳基卤化物在标准条件下能顺利发生反应。然而氯苯由于对低价镍的氧化加成反应活性低,需要10 mol%的催化剂用量和加入NaBr在80 ℃下反应。芳基磺酸酯同样能作为芳基化试剂参与反应。其中对于非吸电基取代的芳基对甲苯磺酸酯和芳基三氟甲磺酸酯底物,需要对反应条件进行调整。
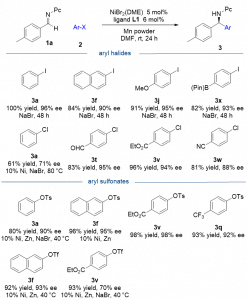
图3. 其他亲电芳基化试剂底物范围考察
大多数醛亚胺容易水解,难以纯化和保存。作者以1:1醛和氮杂芳基胺缩合得到的醛亚胺,只需经过简单的过滤和浓缩,可直接使用亚胺参与不对称还原共轭(杂)芳基化反应 (图4)。结果显示,除了2-吡啶胺类杂芳基胺外,吡嗪胺、2-喹啉胺和4-三氟甲基-2-嘧啶胺也都能顺利与醛缩合生成亚胺并参与不对称还原共轭(杂)芳基化反应。此外,各种取代的(杂)芳基醛都适用于此方法。二级、三级烷基醛的有效缩合反应,需调整反应条件。一级烷基醛由于在合成亚胺过程中主要生成aldol缩合副产物,不适用于该方法。
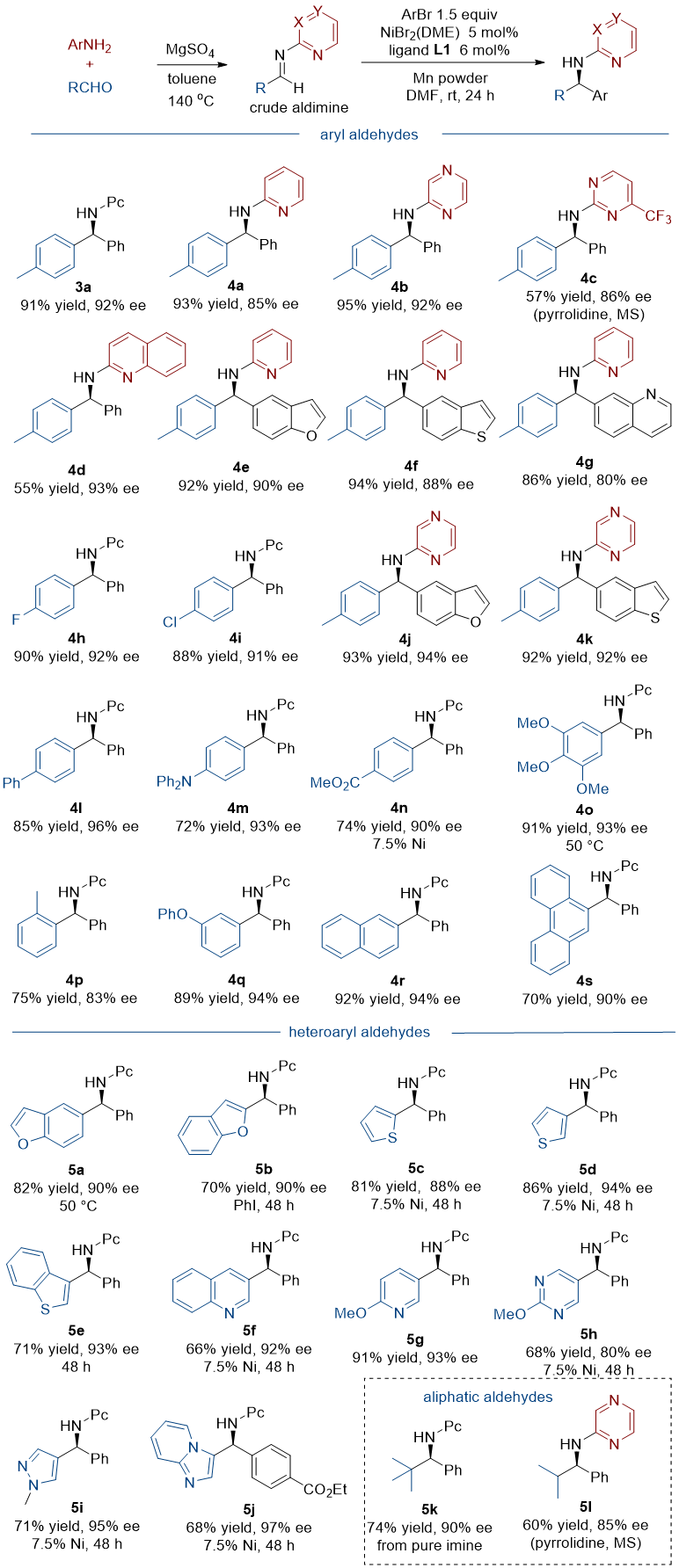
图4. 杂芳基胺和醛的底物普适性考察
作者对产物3a中3-甲基-2-吡啶基进行了脱除,能够以高产率得到Boc保护的手性胺6b,且ee值几乎不变(图5a)。此外,作者用所建立的方法作为核心步骤,得到了药物分子Levocetirizine和(R)-bifonazole的关键中间体6d和6e(图5b和5c)。

图5. 合成应用
基于实验和理论计算反应机理研究(见全文),作者催化循环如下:首先芳基卤对零价镍氧化加成得到二价芳基镍中间体(L1)NiII(Ar)Br B,接着被锰粉还原为一价芳基镍物种 (L1)NiI(Ar) B′,随后对亚胺进行快速的1,4-加成,最后生成的氨基镍物种D与MnBr2发生配体交换,释放的一价镍被锰粉还原成零价镍完成催化循环(图6)。
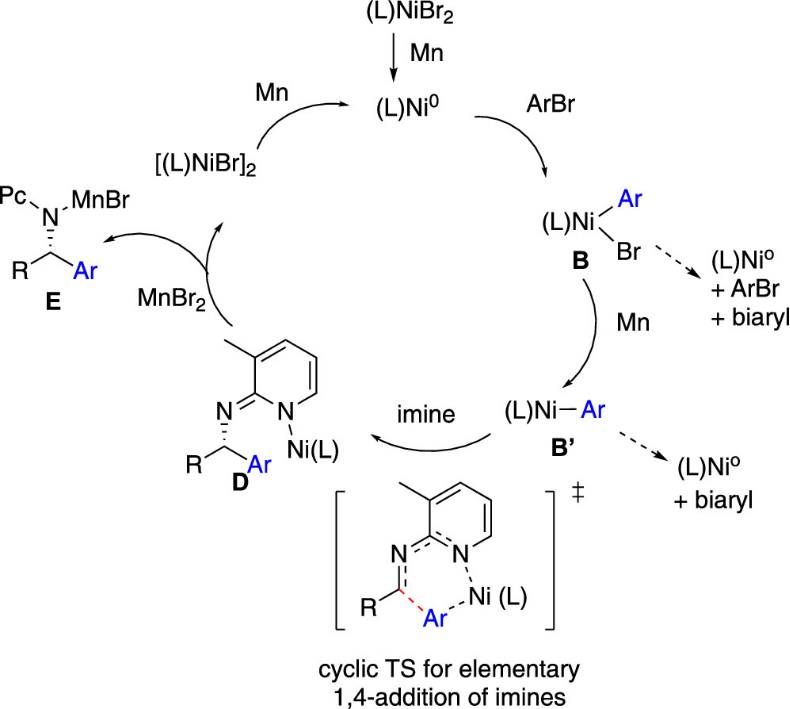
图6. 推测的催化循环
在本文中,作者报道了一种镍催化醛亚胺的不对称还原(杂)芳基化反应。该方法以(杂)芳基卤化物和芳基磺酸酯作为(杂)芳基化试剂,具有优异的官能团兼容性和广阔的底物普适性等优点。此外,作者发展了MgSO4促进的亚胺缩合方法,生成的亚胺无需提纯,可直接参与镍催化的还原(杂)芳基化反应,增强了该方法的实用性。结合实验和理论计算机理研究表明,该反应经历一个非平面六元过渡态的一价芳基镍中间体对N-氮杂芳基亚胺的1,4-加成基元过程。其中实验部分大部分工作由张骆强博士与研究生王秀华合作完成,部分实验由张骆强博士在南洋理工大学Robin Chi 教授实验室完成。DFT计算由吴云东院士课题组蒲茂平博士完成。
相关链接:
网址: http://scbb.pkusz.edu.cn/2019/synthetic_0523/73.html
周建荣实验室网址 http://web.pkusz.edu.cn/stevezhou/
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载























No comments yet.