本文作者:薛定谔的猫
导读
中国科学院上海有机化学研究所胡金波课题组发展了一种手性亚砜亚胺试剂,通过立体选择性加成/原位取代/氧化的策略,实现了手性二氟磺酰胺的高效、高立体选择性合成。
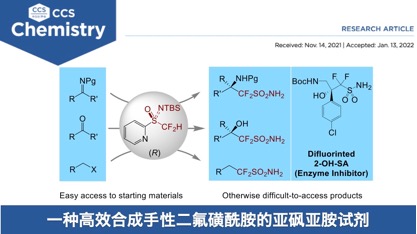
Difluoromethyl 2-Pyridyl Sulfoximine: A Stereoselective Nucleophilic Reagent for Difluoro(aminosulfinyl)methylation and Difluoro(aminosulfonyl)methylation
Qinghe Liu, Chuanfa Ni, Qian Wang, Depei Meng and Jinbo Hu
CCS Chemistry 2022, ASAP, DOI:org/10.31635/ccschem.022.202101634
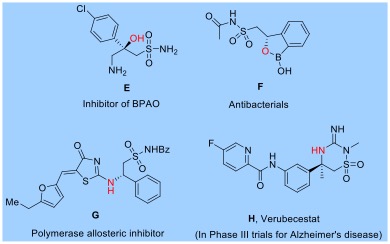
磺酰胺基团广泛存在于药物分子中,迄今为止,已经有超过150种磺酰胺化合物被FDA批准上市,并且仍呈逐年增加的趋势。作为酶抑制剂或消炎剂时,二氟磺酰胺分子通常比非氟对应体表现出更好的效果;这主要是因为氟原子不仅能调节细胞膜通透性、中枢神经渗透性,还能调节磺酰胺的碱性。然而,二氟磺酰胺分子合成方法非常局限,仅能够合成简单的RCF2SO2NR’2 (R = H, n-alkyl, or aryl),而且步骤繁琐[1](7步27%的产率)。考虑到手性磺酰胺分子在药物化学和化学生物学的广泛应用(图1),开发简洁、高效合成手性二氟磺酰胺的方法显得尤为重要。
图1 手性分子
正文
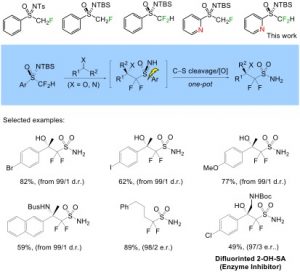
上海有机所胡金波研究员课题组一直致力于氟化、氟烯基化、氟烷基化领域的研究[2]。最近,他们利用亚砜亚胺基团优异的立体诱导性开发了一系列含氟亚砜亚胺试剂(Sulfoximine):通过立体选择性加成、亚砜亚胺脱除(切断烷基C-S键),实现了高选择性的一氟甲基化、二氟甲基化、单氟烯基化等[3-6]。在这样的背景下,他们提出了通过原位取代反应,高区域选择性切断芳基C-S键策略,首次实现了亚砜亚胺既作为手性辅助基也作为功能转化基的合成应用(图2)。
图2 亚砜亚胺试剂与芳基C-S键切断策略
为验证这一策略,他们开发了一种新的亚砜亚胺试剂,(R)-二氟甲基-2-吡啶基亚砜亚胺;在碱的作用下可以高效、高立体选择性的与羰基化合物、亚胺化合物发生加成反应;然后,在EtSNa/EtSH的缓冲体系下,高区域选择性的切断芳基C-S键,经简单氧化可得到二氟磺酰胺的手性醇、手性胺分子,产率和er值高达82%和99/1。作者系统筛选了亚砜亚胺试剂上的(杂)芳基取代基,包括对苯基、硝基苯基、嘧啶基、苯并噻唑基,发现吡啶取代基是反应取得成功的关键,无论是对立体选择性的控制还是C-S键的区域选择性的切断,均能给出较好的结果。该反应兼容性较好,可以兼容溴苯、碘苯、醚、硫醚、炔、吡咯、噻吩等。作者还将该试剂应用于BPAO抑制剂的合成中,以两步49%的产率得到difluorinated 2-OH-SA,对比前文提到的7步27%的产率合成二氟磺酰胺生物活性分子,该方法在步骤大大缩减的同时,效率几乎翻倍。这将使药物化学家和化学生物学家获得一系列立体构型明确的二氟磺酰胺分子并检测它们的生物活性成为可能。
这项工作首次实现了亚砜亚胺分子中芳基C-S键的选择性断裂,成功制备了一系列二氟磺酰胺取代的手性胺和手性醇,为具有生物活性的二氟磺酰胺分子的精准合成提供了一种新途径。该工作以research article的形式发表在CCS Chemistry,已在官网“Just Published”栏目上线(DOI: 10.31635/ccschem.022.202101634)。
- 参考文献
- [1] Y. Liu, V. Ahmed, B. Hill, S. D. Taylor. Org. Biomol. Chem., 2005, 3, 3329. doi: 10.1039/B508852F
- [2] C. Ni, M. Hu, J. Hu. Chem. Rev. 2015, 115, 765. doi:org/10.1021/cr5002386
- [3] W. Zhang, W. Huang, J. Hu. Angew. Chem. Int. Ed. 2009, 48, 9858. doi:10.1002/anie. 200905077
- [4] X. Shen, W. Miao, C. Ni, J. Hu. Angew. Chem. Int. Ed. 2014, 53, 775. doi:10.1002/anie.201308484
- [5] X. Shen, W. Zhang, C. Ni, Y. Gu, J. Hu. J. Am. Chem. Soc. 2012, 134, 16999.doi:10.1021/ja308419a
- [6] Q. Liu, X. Shen, C. Ni, J. Hu. Angew. Chem. Int. Ed. 2017, 56, 619. doi:10.1002/anie.201610127
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载



















No comments yet.