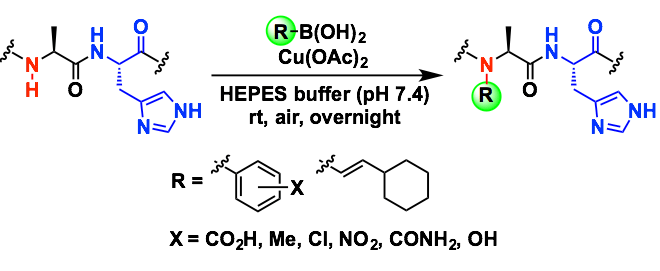
莱斯大学的Zachary T. Ball组(研究中心是对多肽,蛋白质大分子进行体外化学修饰),最近报道了通过利用Cu(II)催化进行的芳基/烯丙基硼酸的氧化偶联,在中性・室温条件下对多肽的主链N-H进行修饰。该反应的特点是可以选择性的对组氨酸附近的酰胺N-H键进行选择性的修饰,从而以蛋白质为底物也能得到位置选择性的修饰产物。
“Histidine-Directed Arylation/Alkenylation of backbone N-H Bonds Mediated by Copper(II)”
Ohata, J.; Minus, M. B.; Abernathy, M. B.; Ball, Z. T.* J. Am. Chem. Soc.2016, 138, 7472. DOI: 10.1021/jacs.6b03390
问题点与工作意义
多肽的N-烷基化衍生物的合成一直以来是一个比较困难的课题。一直以来比较普遍的方法是利用tRNA作为载体的非天然氨基酸的引入法[1],或者固相合成法[2],但是这些方法普遍效率都很低下。另外在多肽的主链上直接进行修饰的手法的报道也非常少,并且蛋白质的修饰反应基本都是以多肽的侧链为反应位点进行的。
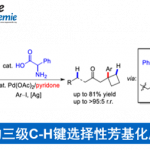
本次介绍的论文中所用条件如标题中的图所示,该反应是对组氨酸(His)残基附近的多肽主链的修饰,这也是该研究的亮点。由于N-H键通常会形成氢键,从而对蛋白质的结构具有很大的影响。因此该方法可以用于构筑一些与普通蛋白质不同的具有新的折叠构型・稳定性・功能化的多肽library。同时,由于对蛋白质活性区域,组氨酸附近的部位进行这样的修饰,也可以用于观察蛋白质的功能变化。
解决手法
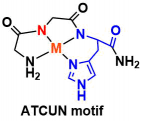
作者着眼于在Chan-Lam-Evans偶联反应条件下,通过硼酸对N-H键进行活化修饰,由于反应底物是多肽,因此通过对条件的改良,使得反应能够在水中,并且是中性条件下进行。反应位点是与His的N侧相连得酰胺N-H键。而选择性的由来,作者认为反应中形成了与ATCUN(amino-terminal Cu and Ni-binding) motif 类似的中间体。
反应条件筛选
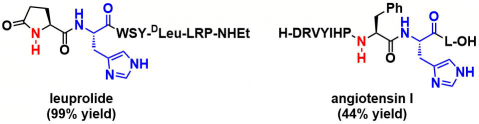
作者以tyrotropin-releasing hormone (TRH, Glp-His-Pro-NH2)为底物进行条件筛选。铜(II)催化剂是必须的,确定了组氨酸旁的焦谷氨酸(Gip)为反应位点,在反应后对产物进行纯化并且通过NOESY・COSY・MS/MS进行确定验证。反应试剂硼酸衍生物可以拓展到芳基硼酸与烯基硼酸。
本条件同样适用于蛋白质,对溶菌酶(一级结构中只含有一个His),利用有机三氟硼酸盐为反应试剂得到了一级结构的修饰产物。该方法也可以引入叠氮化物,炔,脱硫生物素等在化学生物学上比较有用的基团。
还需改进的方面(个人观点)
- 相对于底物,硼酸的用量必须过量(多肽的话,需要用5~10当量,溶菌酶的话需要50当量)。即便如此,反应时间也还是比较长(overnight)。
- 根据氨基酸的种类不同,它们的反应性差异很大。特别是反应点在内部的情况下,反应特别慢。不过对于含有多个组氨酸的多肽来说,说不定通过这点反应性的差异可以达到单位置选择性修饰。
- 组氨酸经常作为蛋白质的活性中心,对蛋白质的构型的维持具有重要作用,而该修饰方法通过修饰组氨酸附近的酰胺基团,改变了构型从而也使得蛋白质失活,因此应用性上值得考量。
相关联的可借鉴研究?
- 可以看出本反应的开发历程的一篇文章、利用铜(II)+硼酸体系对多肽的N-末端的修饰反应的研究[4]
- 蛋白质的位置选择性修饰研究例[5]
参考文献
- Liu, C. C.; Schultz, P. G. Annu. Rev. Biochem. 2010, 79, 413. doi: 10.1146/annurev.biochem.052308.105824
- Chatterjee, J.; Laufer, B.; Kessler, H. Nat. Protoc. 2012, 7, 432. doi:10.1038/nprot.2011.450
- Harford, K.; Sarkar, B. Acc. Chem. Res. 1997, 30, 123. DOI: 10.1021/ar9501535
- Ball, Z. T. et al. Chem. Commun. 2017, 53, 1622. DOI: 10.1039/C6CC09955F
- (a) Davis, B. G. et al. J. Am. Chem. Soc. 2016, 138, 8678. DOI: 10.1021/jacs.6b04043 (b) Pentelute, B. L. et al. Nat. Chem. 2016, 8, 120. doi:10.1038/nchem.2413
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!




















No comments yet.