本文作者:漂泊
铊是一种剧毒的元素,自铊被发现以来,就不断有铊中毒的事件发生。在早期,铊盐被用作脱毛剂和老鼠药,后来已被限制使用。铊在工业上可以用于加工合金以及制造铊灯,铊灯是一种穿透力很好的绿色光源,对于水下照明非常有用。
铊的基本物理性质
| 分类 | 第ⅢA族▪金属 |
| 原子序号・原子量 | 81 (204.3833) |
| 电子配置 | 6s26p1 |
| 密度 | 11.85 g/cm3 |
| 熔点 | 303.5 oC |
| 沸点 | 1457 oC |
| 色・形状 | 银灰色金属 |
| 丰度 | 0.000014ppm(海水) |
| 发现者 | William Crookes , Claude Auguste Lamy |
| 主要的同位素 | 203Tl, 205Tl |
| 用途例 | 灭鼠药、铊灯、光电探测器 |
| 前后的元素 | 汞-铊-铅 |
铊的发现
1861年, William Crookes 和 Claude Auguste Lamy利用火焰光谱法,分别独自发现了铊元素。由于铊的化合物在火焰中会发出绿光,所以William Crookes提议把它命名为“Thallium”,源自希腊文中的“θαλλός”(thallos),即“绿芽”之意。
在Robert Bunsen和Gustav Kirchhoff发表有关改进火焰光谱法的论文以及在1859至1860年发现铯和铷元素之后,科学家开始广泛的使用火焰光谱法来鉴定矿物和化学物的成份。这一方法开始成为发现新元素的主流方法。William Crookes开始用这种新方法去鉴定数年前August Hofmann交给他的样品,这个样品是德国哈茨山上的一座硫酸工厂进行铅室法过程后的产物。他想鉴定其中的硒化物是否含有碲。1862年,William Crookes发现并分离了一小部分含有新元素的化合物,并且对它的一些性质进行了分析。他发现了之前从未发现过的绿色谱线。
Claude Auguste Lamy所用的光谱仪与William Crookes的相似。他以黄铁矿作为原料生产硫酸过程中产生的含硒物质,他对这一物质进行了光谱分析,同样观察到了绿色谱线,因此推断当中含有新元素。Claude Auguste Lamy的朋友Fréd Kuhlmann有一家硫酸工厂能够为他提供大量的副产品,这为Claude Auguste Lamy的研究带来了化学样本上的帮助。他利用大量的样品判断了多种铊化合物的性质,并通过电解法从铊盐制备了单质铊。
Claude Auguste Lamy在1862年伦敦国际博览会上“为发现新的、充裕的铊来源”而获得一枚奖章。William Crookes在抗议之后,也“为发现新元素铊”而获得奖章。两人之间有关发现新元素的荣誉之争议持续到1862至1863年。争议在1863年6月William Crookes获选为英国皇家学会院士之后逐渐消退。 [1-10]
铊的冶炼
铊主要从有色重金属硫化矿冶炼过程中作为副产品回收,铊的氧化物挥发性很强,在铜、铅、锌硫化物精矿焙烧、烧结和冶炼时大部分挥发进入烟尘。硫酸厂焙烧黄铁矿时,炉气净化系统的富铊烟尘也可作为提取铊的原料。例如炼铅时约有60%~70%的铊进入烧结、焙烧烟尘中。烟尘中的铊多半是氧化铊、硫酸铊和氯化铊。用稀硫酸浸出含铊烟尘时,锌、镉、铁及其他元素同时进入溶液。高锰酸钾的稀溶液可以将TI+氧化成Tl3+,根据铊、锌、镉在不同的pH值溶液中沉淀的原理,可以将铊从溶液中以氢氧化铊的形态沉淀析出。溶液中铊离子浓度较大时,也可以加过量的氯化钠使铊以难溶的氯化铊形态沉淀下来。
高纯度铊可采用电解精炼法。用一般方法制得的铊,尚含有铜、铅、镉等杂质,先用碱和硝酸钠与金属铊进行熔炼,使铅生成铅酸钠而被除去,如铅含量超过0.03%,则需熔炼两次。这样也可使铜、镉成为氢氧化物而被除去。电解精炼时,阴极用纯铊或钽片,电解质中铊含量为30~40 g/L,硫酸浓度为70 g/L,温度为55~60℃,阴极电流密度为100A/m2,阳极电流密度为200A/m2,阳极套以布套。经过两次到三次电解精炼,可获得99.999%的高纯铊。[11-12]
光电应用
硫化铊是一种对红外线特别敏感的半导体材料,用它制作的红外光敏光电管可以在黑夜或浓雾大气中接受信号,硫化铊还可用于制造红外线光敏电池。卤化铊的晶体则可制造各种高精密度的光学棱镜、透镜和特殊光学仪器零件。用溴化铊与碘化铊制成的光纤对激光的透过率比石英光纤要好好很多,非常适合于远距离的多路通讯。填充碘化铊的高压汞铊灯是一种非常好的绿色光源,它可以优化灯泡温度和显色性,并将光谱转移到绿色区域,这对水下照明非常有用,在信号灯生产和化学工业光反应的特殊发光光源方面广泛应用。此外,在玻璃生产过程中,添加少量的硫酸铊或碳酸铊,还可以大幅提升其折射率。 [13-17]
铊灯
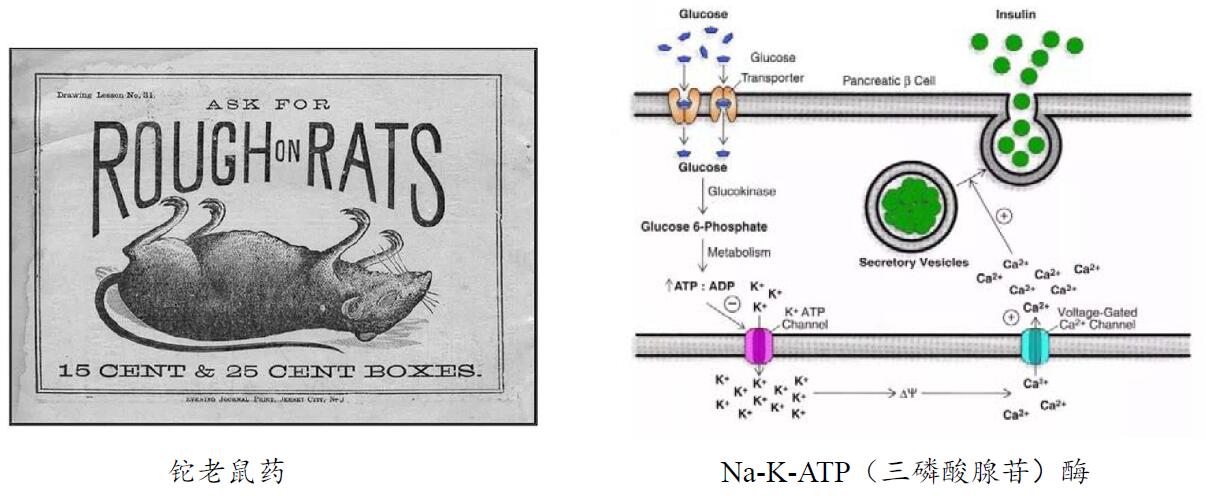
使人脱发的毒药
人们发现铊之后,最开始是用铊的化合物如醋酸铊来治疗头癣等疾病,因为服用铊盐会导致毛发脱落,对于应对癣类疾病有帮助。后来由于发现其毒性大,因而作为杀鼠药和杀虫剂。铊的大量使用也使得许多患者中毒。随着以后对铊毒副作用的更深入研究和了解,很多国家为了避免铊化物对环境造成污染,纷纷限制或禁止铊的使用。铊对人体的毒性超过了铅和汞,近似于砷。铊的化合物具有诱变性、致癌性和致畸性,其致突变活性大于有明显致突变作用的氯化汞,这会导致多种癌症疾病的发生,危害性极大。
铊最直接的危害是它还可以与细胞膜表面的Na-K-ATP(三磷酸腺苷)酶竞争结合进入细胞内,与线粒体表面含巯基团结合,抑制其氧化磷酸化过程,干扰含硫氨基酸代谢,抑制细胞有丝分裂和毛囊角质层生长。同时,铊可与维生素B2及维生素B2辅助酶作用,破坏钙在人体内的平衡铊具有明显的细胞毒作用。铊离子进入细胞后,在细胞核处浓度最高。铊离子能取代钾离子,某些酶的亲和力比钾大10倍。铊不仅作用于体细胞。也能损伤生硫细胞染色体。
铊中毒患者胃肠道症状非常明显,短期内会出现恶心,阵发性腹绞痛,胃肠道出血等症状;神经系统症状也十分明显,出现惊厥或是昏迷状态,类似癫痛病样发作,神经紊乱;此外,患者会感觉下肢麻木、酸疼、无力。后期还会出现脱发,起初为斑秃,以后逐渐发展为全秃。从铊被发现至今,一直未找到理想的治疗铊中毒药物,现在临床上主要采用普鲁士蓝等金属络合剂来治疗急性铊中毒。[18-24]
参考文献
- [1] Liddell, Henry George and Scott, Robert (eds.) “θαλλος Archived 2016-04-15 at the Wayback Machine”, in A Greek–English Lexicon, Oxford University Press.
- [2] Crookes, William (March 30, 1861) “On the existence of a new element, probably of the sulphur group,” Chemical News, vol. 3, pp. 193–194; reprinted in: Crookes, William (April 1861). “XLVI. On the existence of a new element, probably of the sulphur group”. Philosophical Magazine. 21 (140): 301–305. doi:10.1080/14786446108643058.;
- [3]Lamy, A. (May 16, 1862) “De l’existencè d’un nouveau métal, le thallium,” Comptes Rendus, vol. 54, pages 1255–1262.
- [4] Weeks, Mary Elvira (1932). “The discovery of the elements. XIII. Supplementary note on the discovery of thallium”. Journal of Chemical Education. 9 (12): 2078. Bibcode:1932JChEd…9.2078W. doi:10.1021/ed009p2078.
- [5]G. Kirchhoff; R. Bunsen (1861). “Chemische Analyse durch Spectralbeobachtungen”. Annalen der Physik und Chemie. 189 (7): 337–381. Bibcode:1861AnP…189..337K. doi:10.1002/andp.18611890702.
- [6]Crookes, William (1862–1863). “Preliminary Researches on Thallium”. Proceedings of the Royal Society of London. 12: 150–159. doi:10.1098/rspl.1862.0030. JSTOR 112218.
- [7] Crookes, William (1863). “On Thallium”. Philosophical Transactions of the Royal Society of London. 153: 173–192. doi:10.1098/rstl.1863.0009. JSTOR 108794.
- [8]DeKosky, Robert K. (1973). “Spectroscopy and the Elements in the Late Nineteenth Century: The Work of Sir William Crookes”. The British Journal for the History of Science. 6 (4): 400–423. doi:10.1017/S0007087400012553. JSTOR 4025503.
- [9] Lamy, Claude-Auguste (1862). “De l’existencè d’un nouveau métal, le thallium”. Comptes Rendus. 54: 1255–1262.
- [10] James, Frank A. J. L. (1984). “Of ‘Medals and Muddles’ the Context of the Discovery of Thallium: William Crookes’s Early”. Notes and Records of the Royal Society of London. 39 (1): 65–90. doi:10.1098/rsnr.1984.0005. JSTOR 531576.
- [11] 和段琪,蒋兴明,梁双陆等.云南金属材料产业发展研究:冶金工业出版社,2015.06:197页
- [12] 中国冶金百科全书总编辑委员会.中国冶金百科全书·有色金属冶金.北京:冶金工业出版社,1999年:第741-744页
- [13] Hammond, C. R. (2004-06-29). The Elements, in Handbook of Chemistry and Physics (81st ed.). CRC press. ISBN 978-0-8493-0485-9.
- [14] Nayer, P. S; Hamilton, O. (1977). “Thallium selenide infrared detector”. Appl. Opt. 16 (11): 2942–4. Bibcode:1977ApOpt..16.2942N. doi:10.1364/AO.16.002942. PMID 20174271.
- [15] Reiling, Gilbert H. (1964). “Characteristics of Mercury Vapor-Metallic Iodide Arc Lamps”. Journal of the Optical Society of America. 54 (4): 532. doi:10.1364/JOSA.54.000532.
- [16] Gallo, C. F. (1967). “The Effect of Thallium Iodide on the Arc Temperature of Hg Discharges”. Applied Optics. 6 (9): 1563–5. Bibcode:1967ApOpt…6.1563G. doi:10.1364/AO.6.001563. PMID 20062260.
- [17] Wilford, John Noble (1987-08-11). “UNDERSEA QUEST FOR GIANT SQUIDS AND RARE SHARKS”.
- [18]Jump up to: a b Emsley, John (2006). “Thallium”. The Elements of Murder: A History of Poison. Oxford University Press. pp. 326–327. ISBN 978-0-19-280600-0.
- [19]约翰·埃姆斯利.致命元素:毒药的历史[M].毕小青,译.生活·读书·新知三联书店.2012
- [20]Taylor, George J. (2004). Primary care cardiology. Wiley-Blackwell. p. 100. ISBN 978-1-4051-0386-2.
- [21] 朱延河, 牛小麟. 铊的生态健康效应及其对人体危害[J]. 国外医学医学地理分册, 2008, 29(1):14-16.
- [22] 周清平, 胡劲, 姚顺忠. 铊的应用以及对人体的危害[J]. 南方金属, 2009(3):10-12.
- [23] “Biology of Thallium”. webelemnts. Retrieved 2008-11-11.
- [24] Yang, Yongsheng; Faustino, Patrick J.; Progar, Joseph J.; et al. (2008). “Quantitative determination of thallium binding to ferric hexacyanoferrate: Prussian blue”. International Journal of Pharmaceutics. 353 (1–2): 187–194. doi:10.1016/j.ijpharm.2007.11.031. PMID 18226478.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
























No comments yet.