- 概要
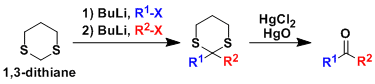
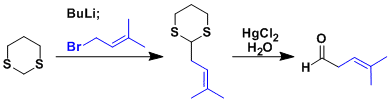
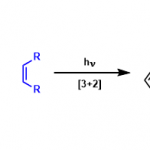
1,3-二噻烷的二号位亚甲基上的氢具有较高的酸性(pKa31.1),与烷基锂试剂等强碱反应的话能得到烷基碳负离子。硫缩醛的脱保护会得到羰基,1,3-二噻烷相当于酰基负离子的等价体来使用(酰基的极性变换)。这样一来与炔基卤化物等亲核试剂反应后,水解就能得到酮或醛。
硫缩醛这种物质,必须用汞或是高价态的碘这类软路易斯酸来活化脱去(布朗苏特酸无法活化它)、因此能够用于羰基的保护基团。通常与缩醛保护基区分开。
- 基本文献
・Seebach, D. Synthesis 1969, 17.
・Grobel, B. T.; Seebach, D. Synthesis 1977, 357. DOI: 10.1055/s-1977-24412
・Seebach, D., Corey, E. J. J. Org. Chem. 1975, 40, 231. DOI:10.1021/jo00890a018
・Seebach, D. Angew. Chem. Int. Ed. Engl. 1977, 18, 239. DOI:10.1002/anie.197902393
- 反应机理
与取代,加成等、有机锂试剂同样的反应相同。
- 反应实例
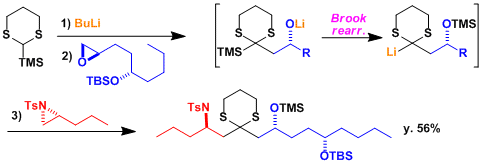
锂化硅取代二噻烷,与环氧化合物反应发生Brook重排,生成被保护的醇。[1] A.B.Smith等人将这一连串的反应命名为Anion Relay Chemistry。
用雷尼镍催化的加氢还原反应中,能得到脱硫产物。是将羰基还原成亚甲基的一种方法(同样的还原方法还有Wolff-Kischner还原、Clemmensen还原等)。(参照:雷尼镍催化的二噻烷还原)
- 实验步骤
- 实验技巧
- 参考文献