- 概要
用卤代芳烃或烷烃与端基炔的偶联反应。催化剂量的Pd(0)催化剂+CuI+胺的组合可以促进反应进行。
近年来,也发现在没有Pd和Cu等存在下,反应也能进行的体系。
- 基本文献
・ Sonogashira, K.; Tohda, Y.; Hagihara, N. Tetrahedron lett. 1975, 50, 4467. doi:10.1016/S0040-4039(00)91094-3
・ Sonogashira, K. Comprehensive Organic Synthesis 1991, 3, 521.
・ Sonogashira, K. J. Organomet. Chem. 2002, 653, 46. doi:10.1016/S0022-328X(02)01158-0
・ Negishi , E.-i.; Anastasia, L. Chem. Rev. 2003, 103, 1979. DOI: 10.1021/cr020377i
・ 有機合成化学協会誌 2004, 62, 355.
・ Chinchilla, R.; Najera, C. Chem. Rev. 2007, 107, 874. DOI: 10.1021/cr050992x
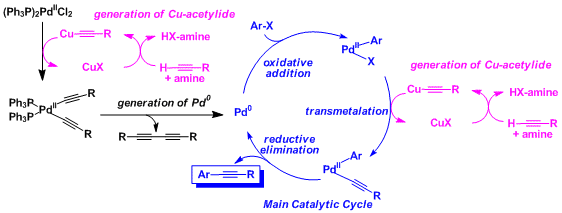
- 反应机理
- 反应实例
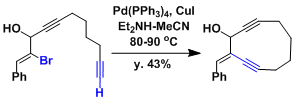
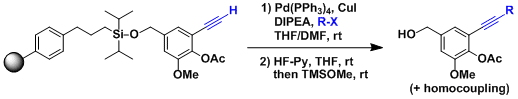
Gingkolide的合成[1]
用分子内的薗头-萩原偶联反应合成炔二烯的骨架。收率较低,最高仅有43%。
这并不是对条件敏感的反应,所以可用固相载体的反应来提高收率。也可组合利用于合成多种类的化合物、衍生物群。
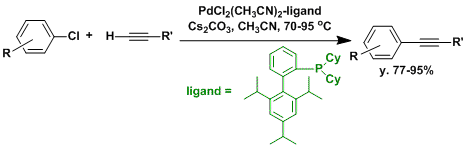
近年用Pd催化剂的偶联反应的发展势头显著,使用大位阻,富电子的膦配体可以使反应性较低的芳基溴,芳基氯作为偶联反应的原料。[5][6]
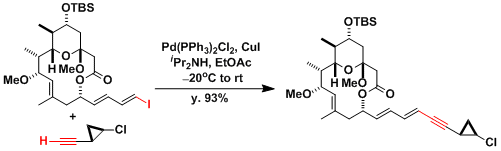
Callipeltoside苷元的合成[7]
- 实验步骤
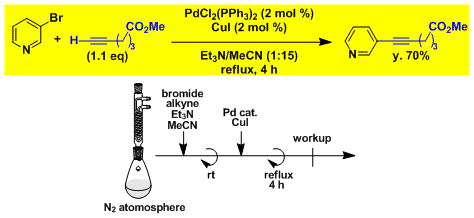
溴代吡啶的薗头反应
- 实验技巧
- 参考文献
[2] Zhang, Q. et al. J. Org. Chem. 2003, 65, 7977. DOI: 10.1021/jo000978e
[3] Dai, W-M.; Wu, A. TetrahedronLett. 2001, 42, 81. DOI:10.1016/S0040-4039(00)01890-6
[4] Liao, Y. et al. Tetrahedron Lett. 2001, 42, 1815. DOI:10.1016/S0040-4039(01)00052-1
[5] Buchwald, S. L. et al. Org. Lett. 2000, 2, 1729. DOI: 10.1021/ol0058947
[6] Buchwald, S. L. et al. Angew. Chem., Int. Ed. 2003, 42, 5993. DOI:10.1002/anie.200353015
[7] Paterson, I.; Davies, R. D. M.; Marquez, R. J. Angew. Chem. Int. Ed. 2001, 40, 603. [abstract]
- 相关书籍


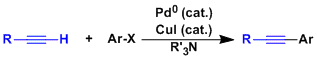
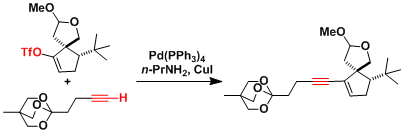
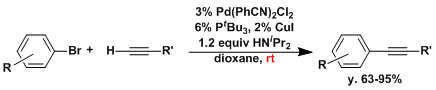














No comments yet.