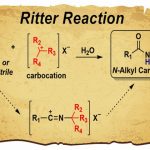
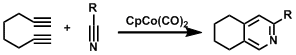概要
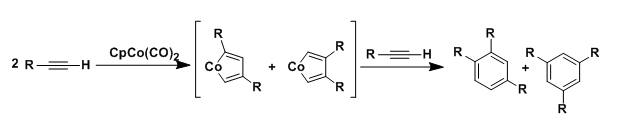
最开始该反应利用Ni、Rh进行催化形成各种过渡金属配位中间体,继而进行的环三量体化。但是在这些金属催化剂中,CpCo(CO)2是使用率最高的一种。
分子间的反应常常伴有位置选择性问题的发生,所以一般该方法常用于分子内反应。
基本文献
- Vollhardt, K. P. C. Angew. Chem. Int. Ed. Engl. 1984, 23, 539. doi:10.1002/anie.198405393
- Saito, S.; Yamamoto, Y. Chem. Rev. 2000,100, 2901. DOI: 10.1021/cr990281x
- 斉藤慎一, 山本嘉則, 有機合成化学協会誌 2001, 59, 346.
- Valera, J. A.; Saa, C. Chem. Rev. 2003, 103, 3787. DOI: 10.1021/cr030677f
- Omae, I. Appl. Organomet. Chem. 2007, 21, 318. DOI: 10.1002/aoc.1213
- Pauson, P.L. e-Encyclopedia of Reagents for Organic Synthesis. 2001. doi:10.1002/047084289X.rd078
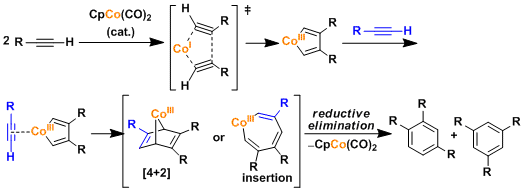
反应机理
参考:J. Am. Chem. Soc. 1983, 105, 1907.
反应实例
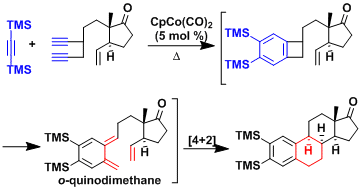
通过邻醌二甲烷构筑一些复杂的缩环骨架。
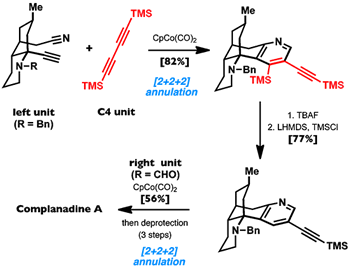
二炔与异腈的组合合成吡啶衍生物。
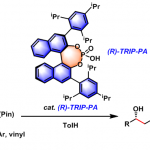
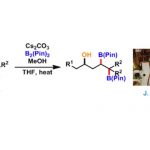
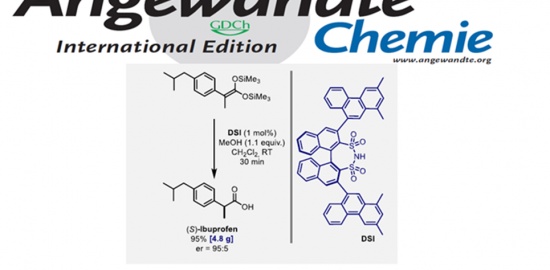
不对称反应实例[1]
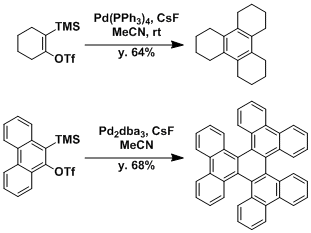
苯炔(=扭曲炔烃)环化三聚
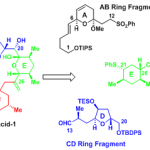
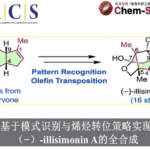
Complanadines A的全合成[2]
实验步骤
实验技巧
参考文献
[1] Sato, Y.; Nishimata, T.; Mori, M. J. Org. Chem. 1994, 59, 6133. DOI: 10.1021/jo00100a003[2] Yuan, C.; Chang, C-T.; Axelrod, A.; Siegel, D. J. Am. Chem. Soc. 2010, 132, 5924. DOI: 10.1021/ja101956x
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!