本文作者:杉杉
导读:
近日,美国California Institute of Technology的B. M. Stoltz小组成功完成首例天然产物havellockate的全合成路线设计。这一路线设计中的关键步骤主要涉及通过Julia-Kocienski烯基化策略,完成两种对映富集结构片段之间的连接,获得相应的二烯砌块;通过丙炔酸 (propiolic acid)酯化/Diels-Alder串联策略,构建分子中的稠合碳环骨架;通过锌试剂促进的Barbier烯丙基化策略,构建havellockate分子中最后的C-C键以及分子中的双重邻近立体生成中心;通过铜催化的空气氧化策略,获得相应的β-hydroxybutanolide结构单元,并最终完成havellockate分子的全合成。
Asymmetric Total Synthesis of Havellockate
Nicholas J. Hafeman, Melinda Chan, Tyler J. Fulton, Eric J. Alexy, Steven A. Loskot, Scott. C. Virgil, Brian M. Stoltz, J. Am. Chem. Soc. 2022, ASAP. doi: 10.1021/jacs.2c09583.
正文:
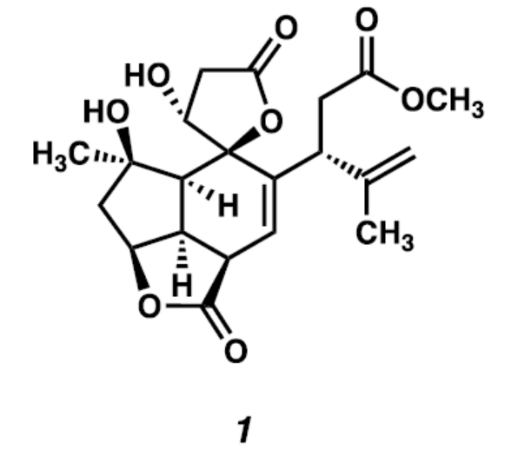
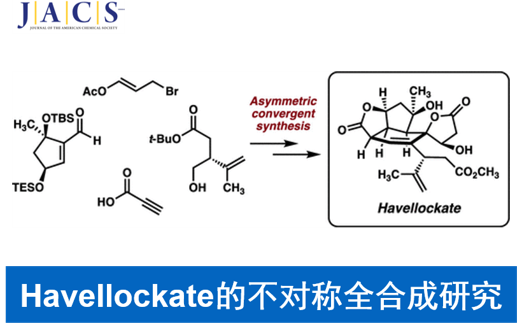
Havellockate(1)是由Sinularia granosa中首次分离获得的一种C20-cembranoid类天然产物[1]。然而,对于havellockate(1) (Figure 1A)的全合成研究,仍面临诸多的挑战[2]-[3]。并且,目前尚未有相关的文献报道。这里,美国California Institute of Technology的B. M. Stoltz小组报道首例天然产物havellockate的全合成路线设计。
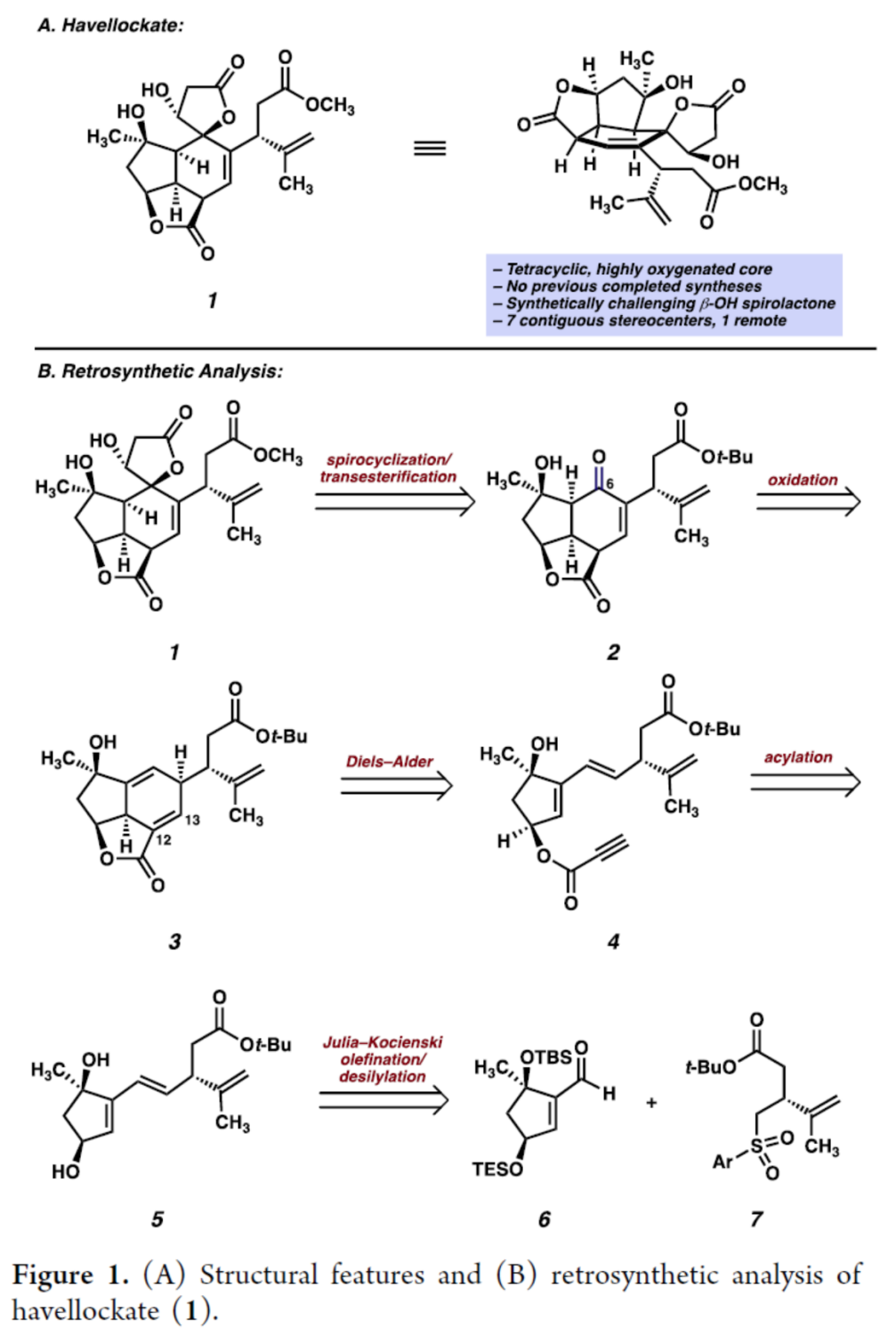
首先该小组通过逆合成分析 (Figure 1B)表明,天然产物havellockate的全合成路线设计中的关键砌块主要涉及:烯酮砌块2、三环砌块3、丙炔酸酯砌块4、二醇砌块5、醛砌块6与以及砜砌块7。
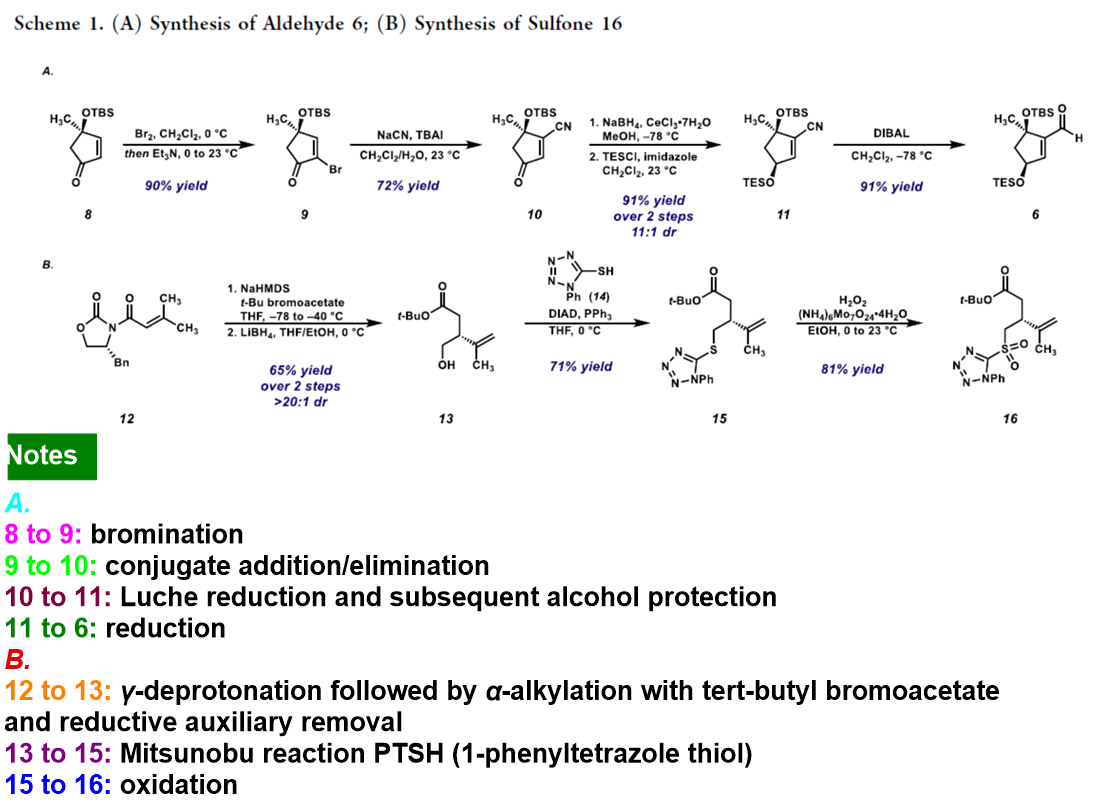
之后,该小组首先进行醛砌块6 (Scheme 1A) 以及砜砌块16的构建 (Scheme 1B)。
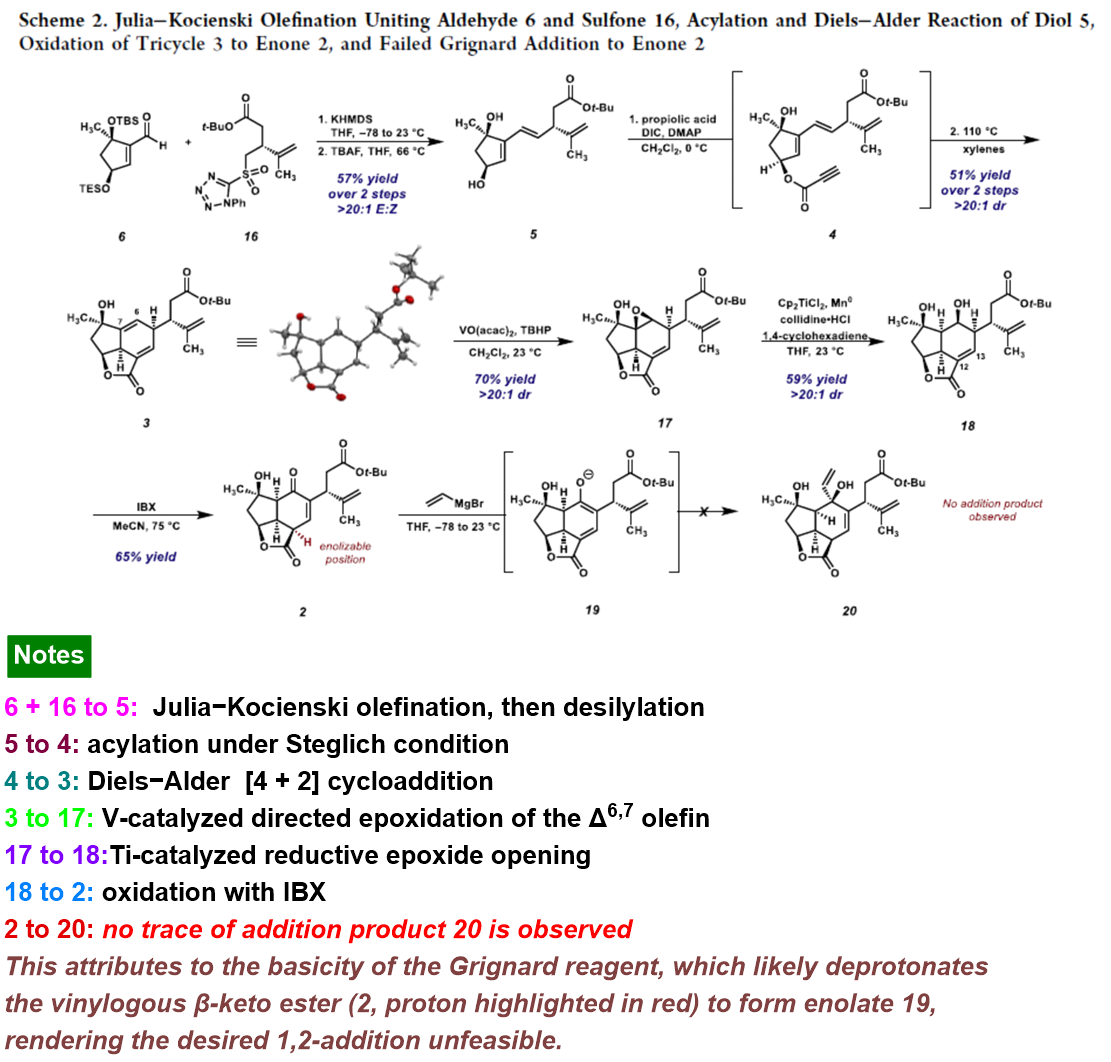
接下来,该小组进一步完成烯酮砌块2 (Scheme 2) 的构建。
之后,该小组进一步通过砌块2,最终完成havellockate (1)的全合成 (Scheme 3)。
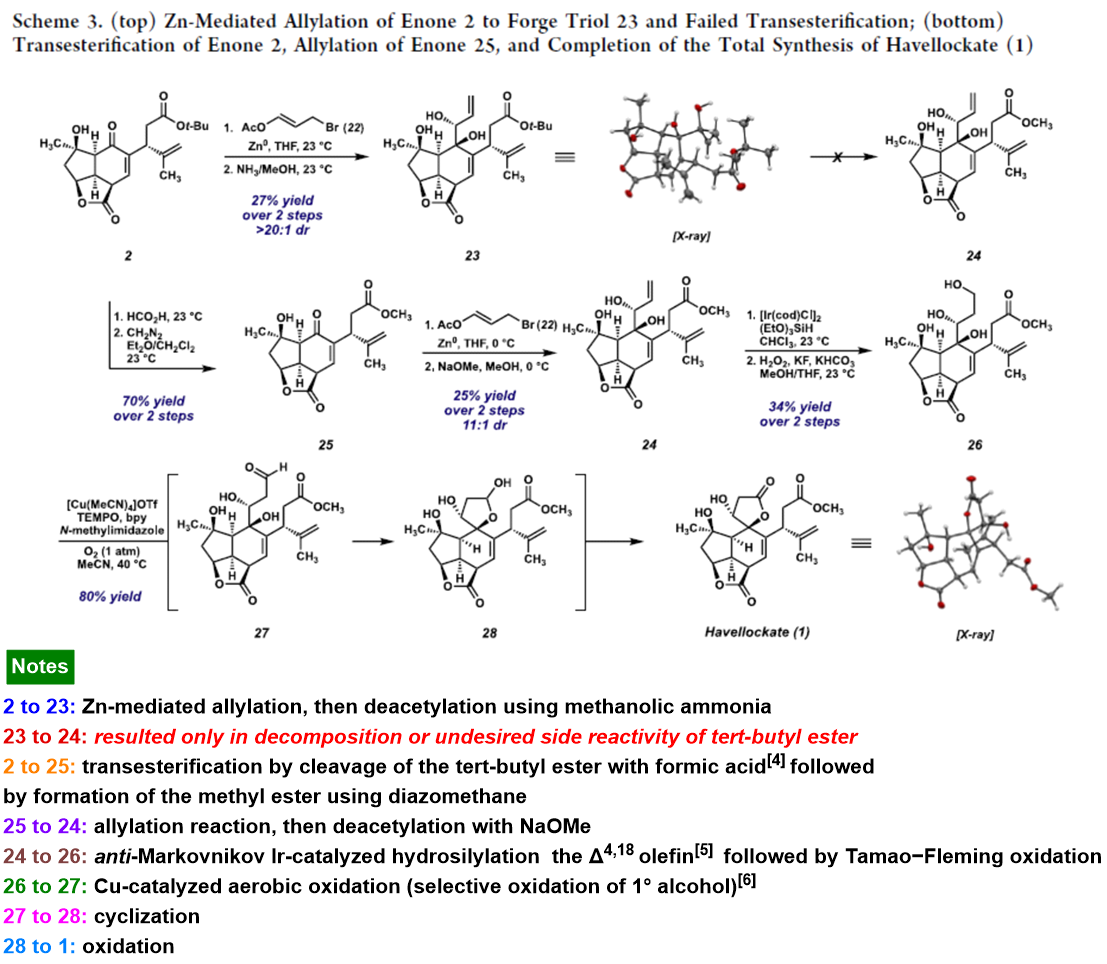
总结:美国California Institute of Technology的B. M. Stoltz团队成功设计出首例天然产物havellockate的全合成路线。其中,关键步骤主要涉及:通过Julia-Kocienski烯基化反应,将两种对映富集的结构片段进行连接;通过分子内Diels-Alder反应,完成havellockate分子中六元环骨架的构建;通过立体选择性的烯酮 1,2-acetoxyallylation 策略,完成havellockate分子中最后的C-C键以及剩余立体生成中心的构建;通过硅氢化/ Tamao-Fleming氧化以及铜催化的氧化环化策略,完成havellockate分子中butanolide环的构建,并最终完成havellockate的全合成。
参考文献:
- [1] A. S. R. Anjaneyulu, M. J. R. V. Venugopal, P. Sarada, J. Clardy, E. Havellockate. Lobkovsky, Tetrahedron Lett. 1998, 39, 139. doi: 10.1016/S0040-4039(97)10470-1.
- [2] G. Mehta, R. S. Kumaran, Tetrahedron Lett. 2001, 42, 8097. doi: 10.1016/S0040-4039(01)01721-X.
- [3] R. L. Beingessner, J. A. Farand, L. Barriault, J. Org. Chem. 2010, 75, 6337. doi: 10.1021/jo101279z.
- [4] S. Chandrasekaran, A. F. Kluge, J. A. Edwards, J. Org. Chem. 1977, 42, 3972. doi: 10.1021/jo00444a046.
- [5] X. Xie, X. Zhang, H. Yang, X. Ji, J. Li, S. Ding, J. Org. Chem. 2019, 84, 1085. doi: 10.1021/acs.joc.8b02838.
- [6] J. M. Hoover, S. S. Stahl, J. Am. Chem. Soc. 2011, 133, 16901. doi: 10.1021/ja206230h.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载




















No comments yet.