本文作者:杉杉
导读
烷基(芳基)氯化物作为最丰富和稳定的碳亲电子试剂,尽管它们与碳亲核试剂的偶联反应已取得一定的成果,但芳基氯化物与烷基氯化物的亲电偶联反应仍具有难度。近日,美国威斯康星大学麦迪逊分校(University of Wisconsin-Madison)的Daniel J. Weix教授课题组在美国化学学会杂志(Journal of the American Chemical Society)发表论文,使用少量的二碘/溴化镍作为催化剂,使用吡啶-2,6-双(N-氰基甲脒)(PyBCamCN)作为配体,即可实现芳基氯化物与伯烷基氯化物的亲电偶联反应。此外,Br–和I–可作为助催化剂,可产生反应性更高的烷基溴/碘化物。
Nickel-Catalyzed Cross-Electrophile Coupling of Aryl Chlorides with Primary Alkyl Chlorides
Seoyoung Kim, Matthew J. Goldfogel, Michael M. Gilbert, Daniel J. Weix*
J. Am. Chem. Soc. 2020, 142, 9902–9907 DOI: 10.1021/jacs.0c02673
正文
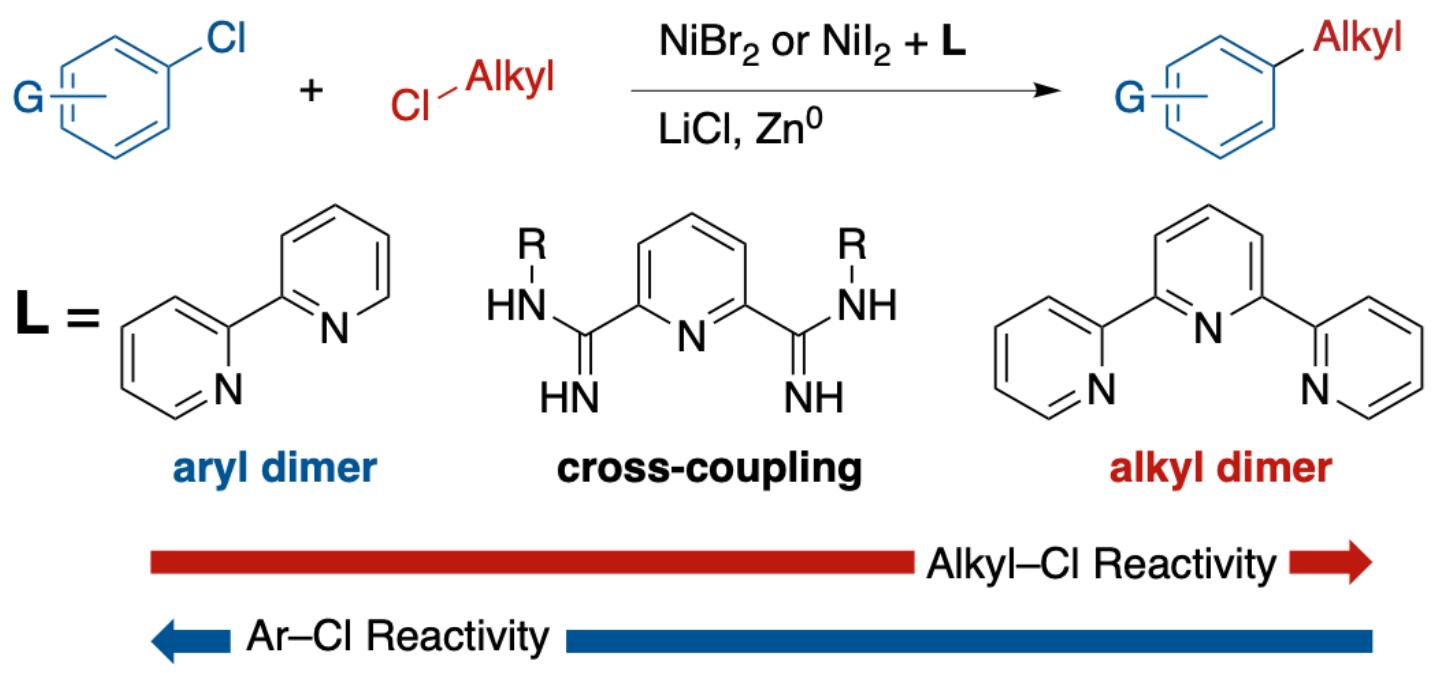
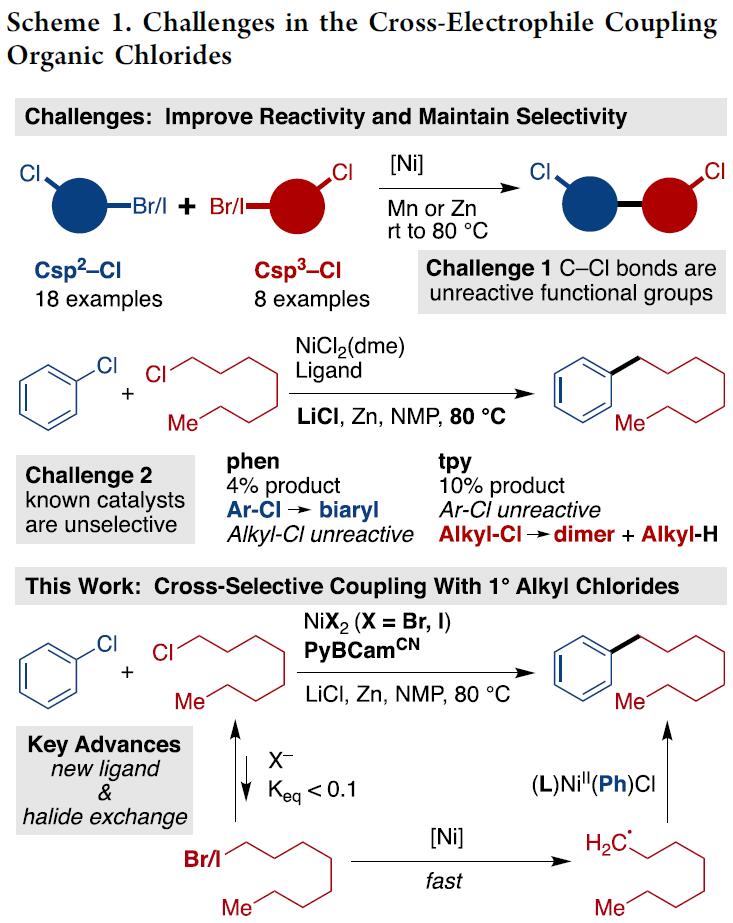
亲电偶联作为合成Csp2-Csp3键的重要方法,然而对于反应活性较低的C-Cl键活化一直具有一定的难度,同时,未活化的C-Cl键常常在交叉亲电偶联反应中具有良好的耐受性(Scheme 1)。此外,有机氯化物的偶联反应具有一定的优势,如有机氯化物比有机溴(碘)化物在自然界更为丰富。其次,由于C-Cl键具有较低的反应性,因此可将C-Cl键早期引入体系,后期再进行不同的修饰。在亲电偶联反应中,C-Cl键活化的主要挑战是,在不牺牲选择性的前提下提高反应性。尽管已有文献报道关于烷基氯化物和芳基氯化物的二聚化反应,但尚未发现一般选择性的方法。最近,Zhang报道了多种芳基氯的偶联反应,但仅与过量的ClCF2R试剂偶联。其他课题组也报道了芳基氯与烷基溴化物或草酸叔烷基酯的偶联反应。然而,使用氯苯与烷基溴的偶联仅获得小于25%收率的偶联产物。此外,根据提出的芳基碘化物与烷基碘化物偶联的反应机理,需要一种催化剂,可克服双重选择性的问题,首先与烷基-Cl反应生成烷基自由基,再与镍配位的Ar-Cl化合物反应。在此,美国威斯康星大学麦迪逊分校Daniel J. Weix教授课题组报道,使用少量二碘/溴化镍作为催化剂,以吡啶-2,6-双(N-氰基甲脒)(PyBCamCN)作为配体,即可实现芳基氯化物与伯烷基氯化物的亲电偶联反应。
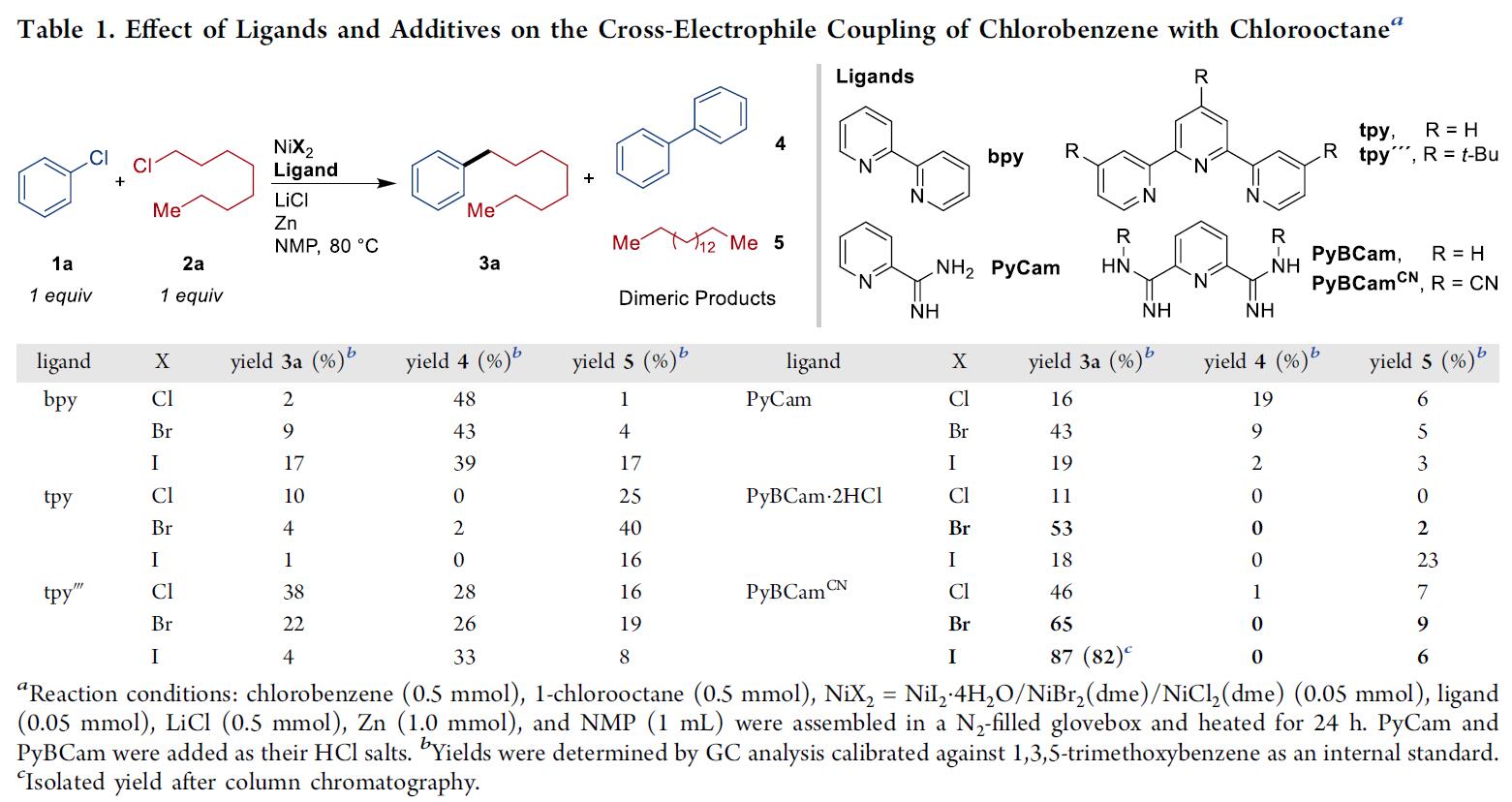
首先,作者以氯苯1a和伯烷基氯化物2a作为模型底物,进行了相关亲电偶联反应条件的筛选(Table 1)。通过实验对比后,作者发现催化剂与亚化学计算量(10-30 mol%)的溴或碘化物之间存在强烈的协同作用。当无溴或碘化物时,筛选的催化剂均未获得高收率的产物。而使用PyBCamCN配体和NiBr2(dme)或NiI2·4H2O催化剂时,可实现高选择性。使用bpy配体时,有利于芳基溴化物的自偶联。使用tpy配体时,有利于卤代烷烷烃的二聚。而使用tpy´´´配体时,有利于Negishi交叉偶联反应,同时消耗了两种底物,形成了约1:1:1的产物/烷基二聚体/芳基二聚体。随后,通过对PyBCam和PyBCamCN实验优化表明,PyBCamCN反应效果最好。此外,使用二溴化镍催化剂时,若缓慢通过注射器分批加入烷基氯时,反应收率最高,但使用碘化镍催化剂不能提高收率。在两种情况下,主要的副产物是烷基二聚体和芳基加氢脱卤化的产物。
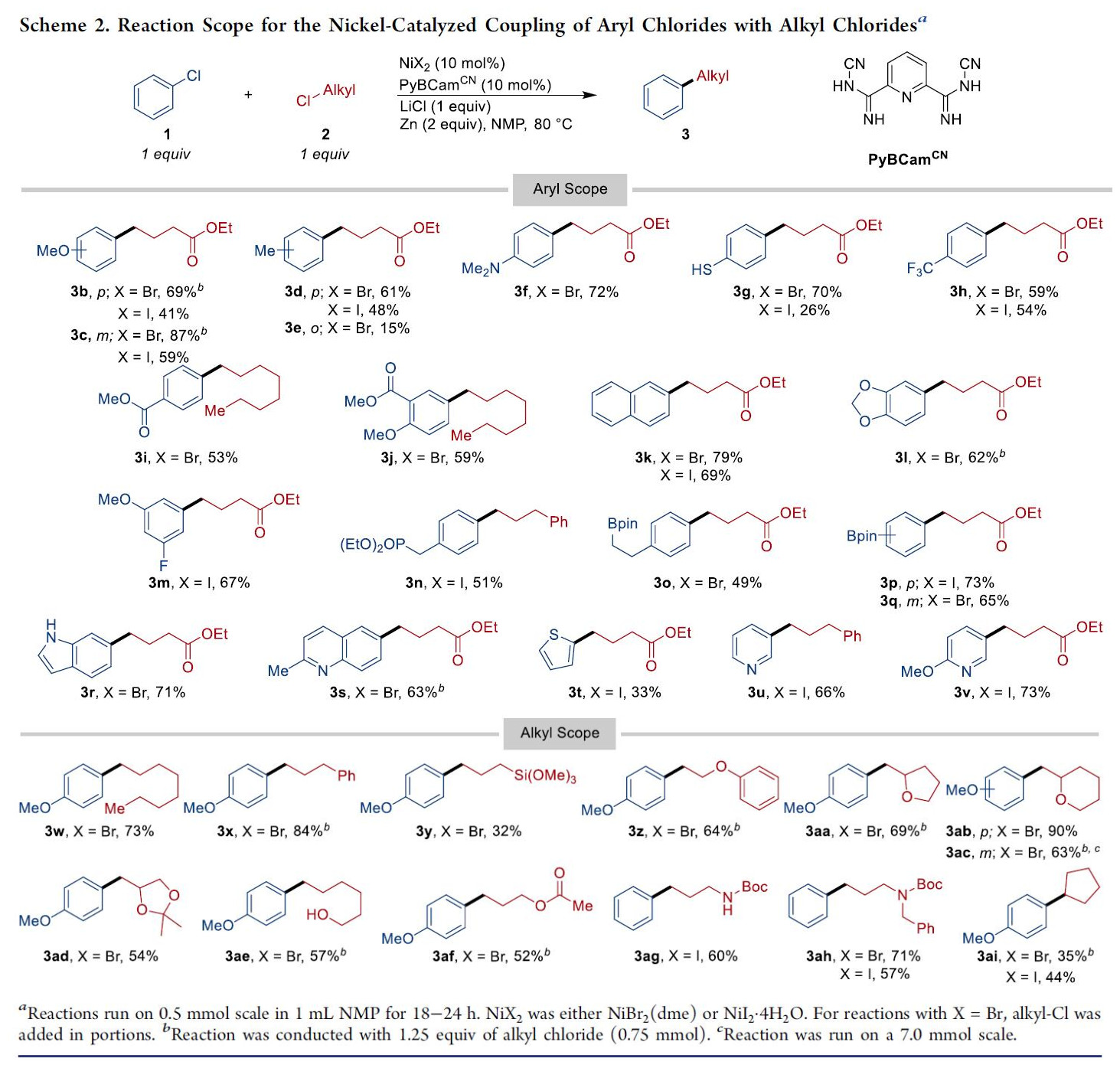
在获得上述最佳反应条件后,作者开始对氯代芳烃1和伯烷基氯2的底物范围进行了扩展(Scheme 2)。首先,作者研究了氯代芳烃的底物范围。反应结果表明,具有富电子的芳基氯化物,可获得相应的产物3b,3f,3g,3r(收率69-72%)。但是,使用空间位阻更高的2-氯甲苯仅获得15%收率的3e。此外,缺电子的芳基氯也可与烷基氯偶联,获得收率为53-73%的产物(3c,3h,3i,3s,3u,3v)。同时,各种杂环均与体系兼容,如缺电子喹啉(3s,63%)和吡啶(3u,66%和3v,73%),富电子吲哚(3r,71%)和噻吩(3t,33%)等。带有β-离去基团的卤代烷也可获得相应的产物3z–3ad,仲烷基氯同样获得目标产物3ai,但收率较低(44%)。芳基和烷基频哪醇硼酸酯也具有良好的耐受性,获得产物3o–3q(收率49-73%),为进一步精制产品提供了机会。同样,具有酸性N-H(3ag,60%)和O-H(3ae,57%)基团的底物(对于有机镁或有机锌试剂而言是一个挑战),而在此条件下,可耐受游离硫醇(3g,70%的收率),避免了SN2与烷基亲电试剂和S-芳基化反应。另一方面,尽管在60-80℃下存在路易斯酸(ZnII盐,Li+盐),但氮上的Boc基团仍然可以耐受(3ag-60%,3ah-71%)。同样,酯类化合物也可与体系兼容,如甲酯(3i,3j)、苄基二乙基膦酸酯(3n)和三甲氧基硅烷(3y)。此外,产物3ac的放大实验,同样获得较好的结果。
与芳基卤化物与烷基卤化物的其他亲电偶联反应相比,该反应的主要特征是能够以选择性的方式使两种相对不活泼的底物进行偶联。在此反应中,有三个关键性的因素。第一,LiCl对于(通过锌表面)有效还原镍催化剂至关重要。ZnCl2可以对镍催化剂的还原具有抑制作用,而LiCl是克服抑制作用的最佳试剂之一。同样,在无LiCl时,会形成3%的自偶联产物,并且主要返回两种底物。同时,两种有机氯化物均不会直接与锌反应形成有机锌试剂。
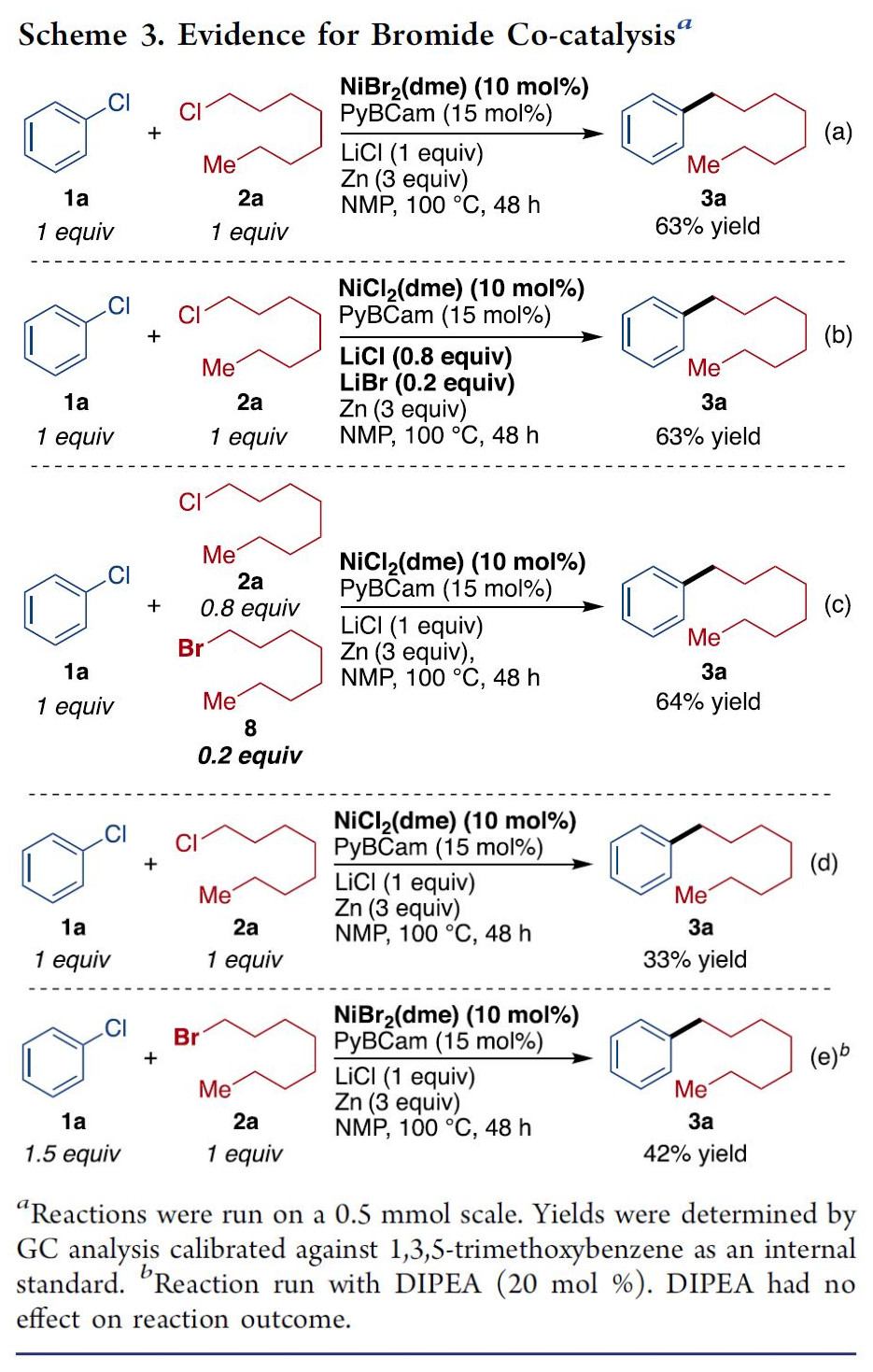
第二,通过增加烷基氯有助于促进卤化物交换。作者发现,无论采用何种方式引入溴化物或碘化物,对于合理的反应速率都是必不可少的(Scheme 3)。而低浓度的溴化物对于反应至关重要。在无任何溴化物(Scheme 3d)或仅在烷基溴化物时进行反应(Scheme 3e),仅获得较低收率的产物。
最后,对各种配体的研究表明,PyBCam镍催化剂的独特之处在于,即使通过卤化物交换活化,也能够以相似的速率与两种底物反应。同时,镍PyBCam催化剂完全避免了联芳基的形成,只形成少量的烷基二聚体。此外,PyBCam和PyBCamCN作为一种新型的三齿配体,适用于镍催体系。
总结
美国威斯康星大学麦迪逊分校Daniel J. Weix教授课题组报道了芳基氯化物与伯烷基氯化物的第一个选择性亲电偶联反应的例子。同时,该反应的关键之处在于,①新型的选择性配体(PyBCamCN)的使用;②LiCl可提高催化剂的转化率;③溴化物/碘化物的共催化作用。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!





















No comments yet.