本文作者:杉杉
导读
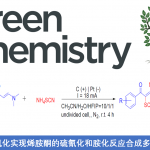
近日,北京大学深圳研究生院周建荣课题组在Angew. Chem. Int. Ed.上发表论文,报道了通过镍催化,实现环烯烃与芳基三氟甲磺酸酯、甲磺酸酯和甲苯磺酸酯的不对称分子间Heck反应。同时,也实现了2-环戊烯酮缩酮底物的不对称还原Heck反应。
Enantioselective Intermolecular Heck and Reductive Heck Reactions of Aryl Triflates, Mesylates and Tosylates Catalyzed by Nickel
Xiaolei Huang, Shenghan Teng, Yonggui Robin Chi, Wenqiang Xu, Maoping Pu,Yun-Dong Wu and Jianrong Steve Zhou*
Angew. Chem. Int. Ed. ASAP DOI: 10.1002/anie.202011036 https://doi.org/10.1002/anie.202011036
正文
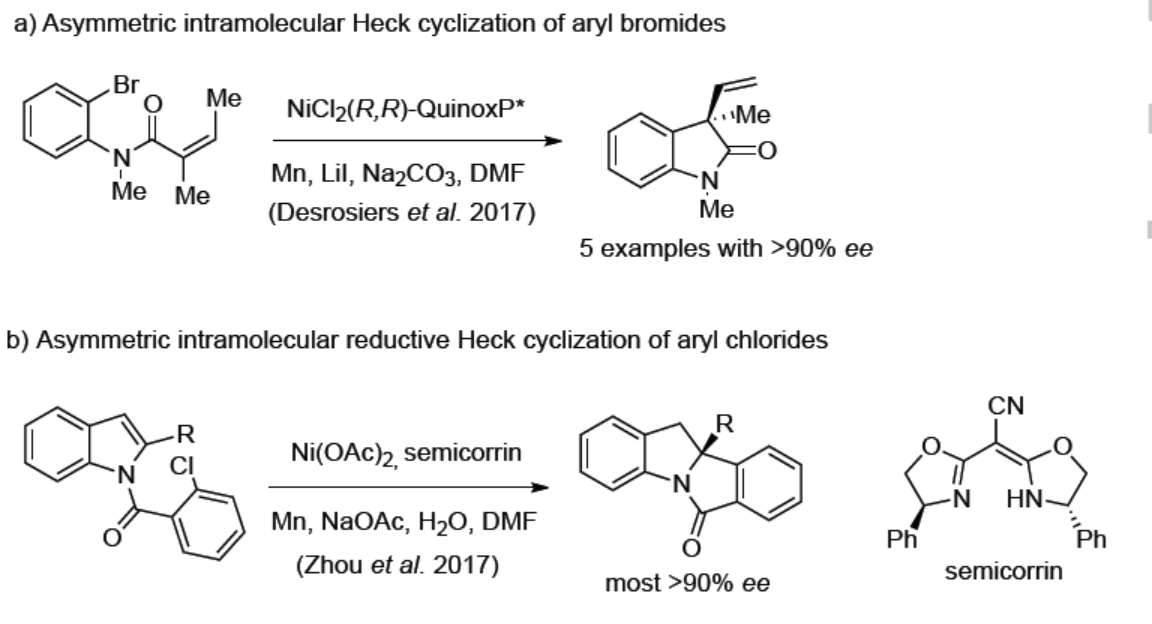
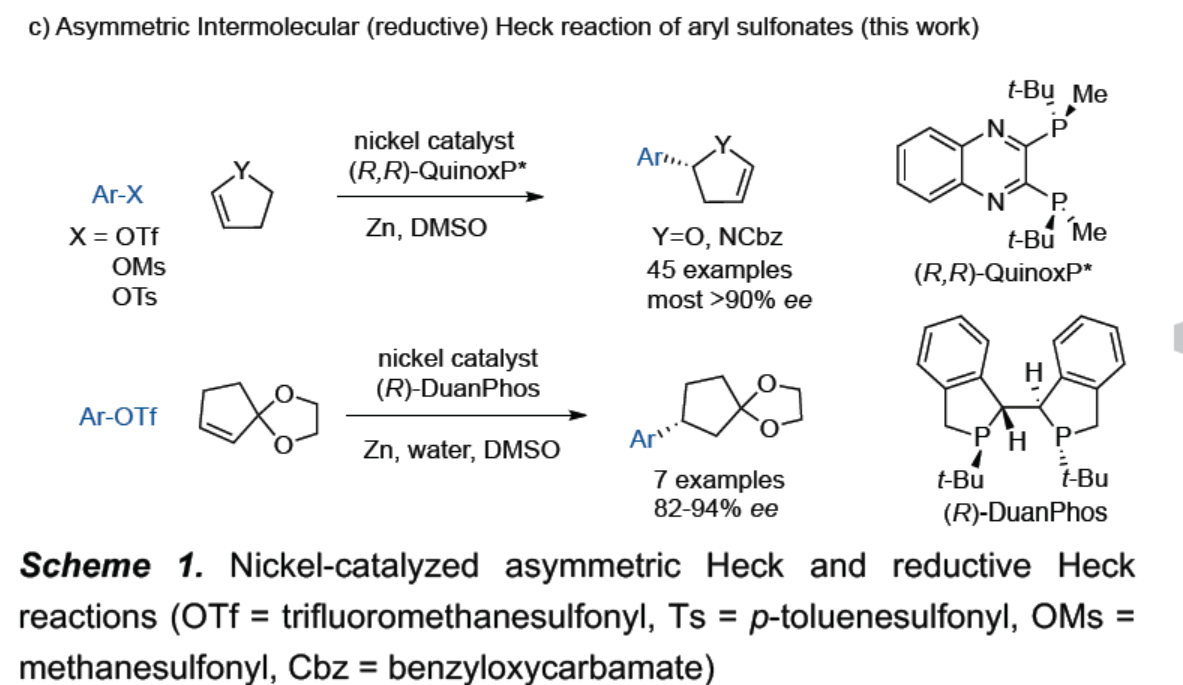
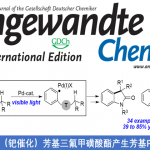
通过不对称Heck反应和还原性Heck反应,可实现以易得的芳基卤化物和磺酸盐使烯烃芳基化(Scheme 1)。因此,科学家已开发出了多种钯催化的方法,但钯作为一种昂贵的稀有贵金属,若能使用廉价的镍替代,则更具吸引力。此外,镍比钯更具电正性,因此,Ni(0)更易氧化加成到甲磺酸酯、甲苯磺酸酯和新戊酸酯的芳基C-O键中。在Heck反应中,芳基镍(II)配合物向烯烃的β-插入比Pd(II)具有较低能垒,但从烷基镍(II)配合物中去除β-氢化物比Pd(II)困难。迄今为止,钯催化的Heck反应中的甲磺酸酯和甲苯磺酸酯仅限于烯基和缺电子的杂芳基化合物。相反,镍催化的Heck反应,可与甲磺酸酯、甲苯磺酸酯和新戊酸酯平稳的反应。目前为止,对于镍催化的不对称Heck反应和还原性Heck反应仍未被开发,并仅限于分子内环化。2017年,Desrosiers和Kozlowski课题组[1]报道了使用NiCl2(R,R)- QuinoxP*催化剂,实现芳基卤化物分子内的不对称Heck环化反应,形成具有季碳立体中心的羟吲哚化合物(Scheme 1a),但ee超过90%的例子却很少。同年,周建荣课题组[2]报道了使用镍/半咕啉(semicorrin)催化剂,实现分子内芳基卤化物的不对称还原性Heck环化反应,获得二氢吲哚和茚满酮化合物(Scheme 1b)。最近,Wang课题组[3]使用镍/ PyrOx催化剂,实现未活化烯烃的不对称还原环化反应。在此,北京大学深圳研究生院周建荣课题组报道了第一个使用镍催化剂,实现分子间不对称Heck反应的实例。廉价或易制备的芳基甲磺酸酯和甲苯磺酸酯以及反应性更高的芳基三氟甲磺酸酯均为合适的底物。此外,不对称分子间还原性Heck反应还适用于缩酮底物(2-环戊烯酮)制备(Scheme 1c)。
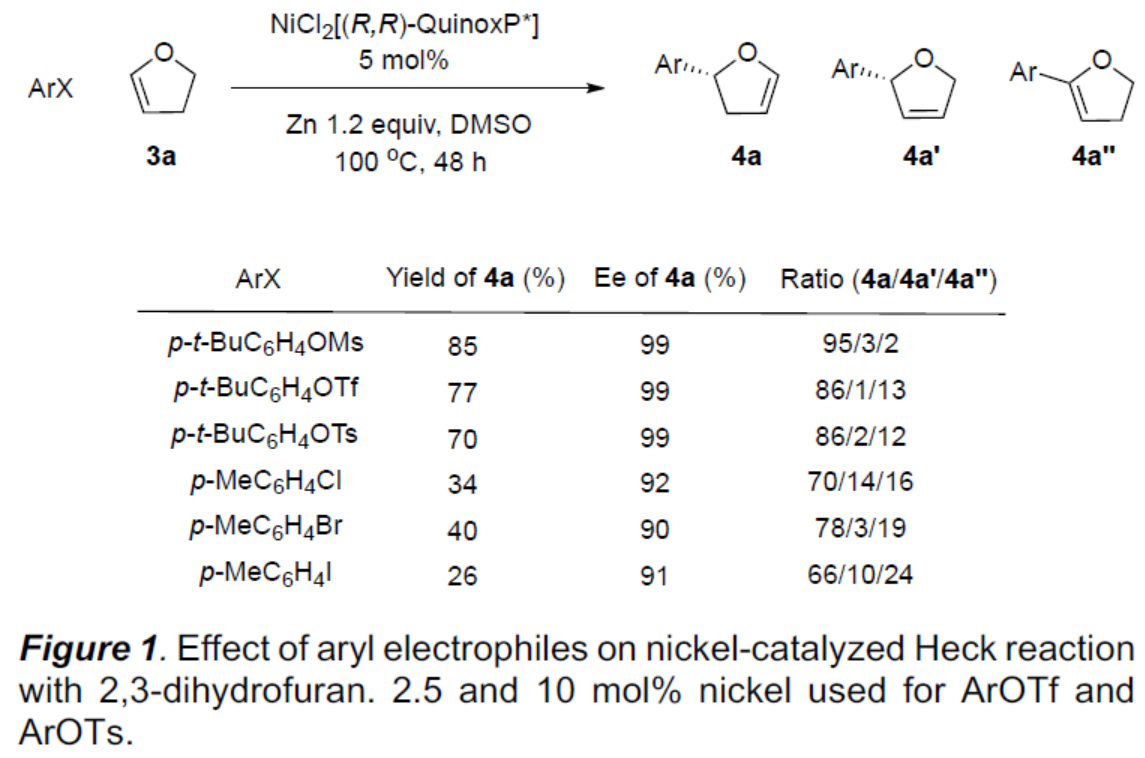
首先,作者以4-叔丁基甲磺酸酯1a和2,3-二氢呋喃3a作为模型底物,进行了不对称Heck反应条件的筛选(Fig. 1)。反应的最佳条件为:使用NiCl2[(R,R)-QuinoxP*]作为催化剂,Zn粉为还原剂,在100 ℃的DMSO溶剂中反应,获得85%收率和99%ee的目标产物4a。通过GC和GCMS分析,Heck产物的三种异构体的比例为95/3/2。
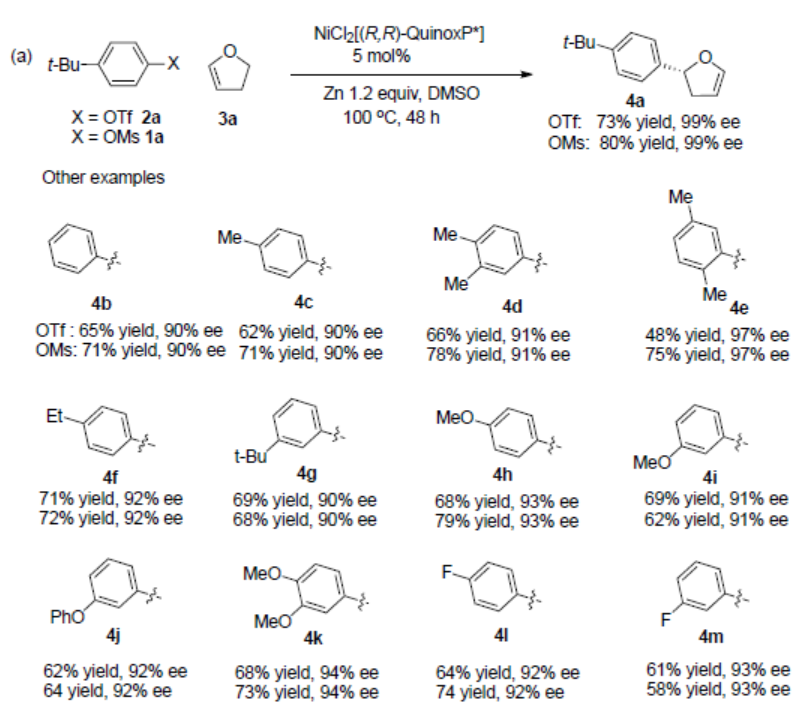
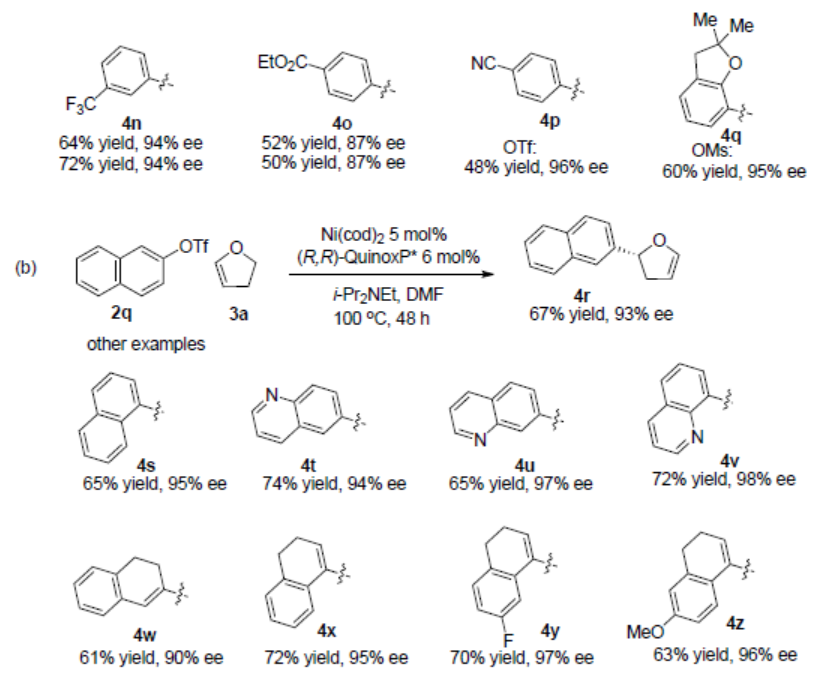
在获得上述最佳反应条件后,作者对ArOTf和ArOMs底物进行了扩展(Scheme 2a)。反映结果表明,各种芳基三氟甲磺酸酯和在芳基环上具有烷基的甲磺酸酯均可平稳的进行反应,获得相应的产物4a-4g。甲氧基醚(4h,4i和4k)、二芳基醚(4j)、氟化芳基(41-4m)、三氟苯甲醚(4n)和酯(4o)均与体系兼容。同时,对氰基苯基三氟甲磺酸酯(4p)以及受阻的二氢苯并呋喃-7-甲磺酸甲酯(4q)也可平稳的进行反应。然而,将其应用到π环体系时,反应结果较差,但使用Ni(cod)2和(R,R)-Quinoxp*时,并加入二异丙基乙胺还原剂时,也可实现相应的转化,从而获得产物4r-4z(Scheme 2b)。
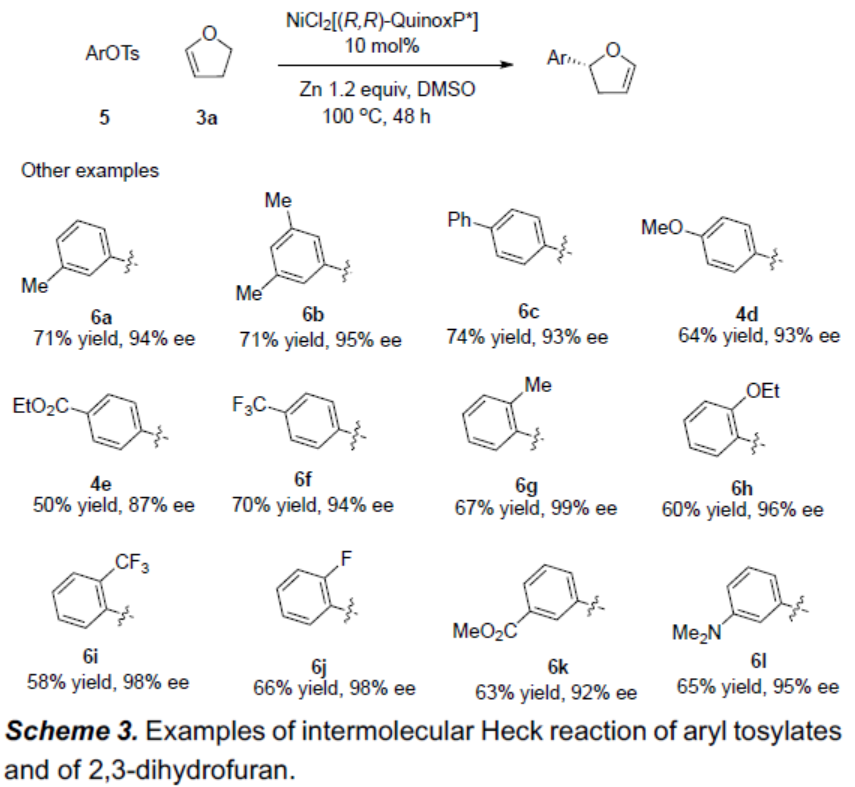
随后,作者对更稳定且廉价的芳基甲苯磺酸酯(ArOTs)进行了扩展(Scheme 3)。当使用NiCl2[(R,R)-QuinoxP*]作为催化剂,Zn粉为还原剂,可使反应有效的进行。反应结果表明,该反应不受电子效应和定位效应的影响,均可获得相应的产物6a-6l。
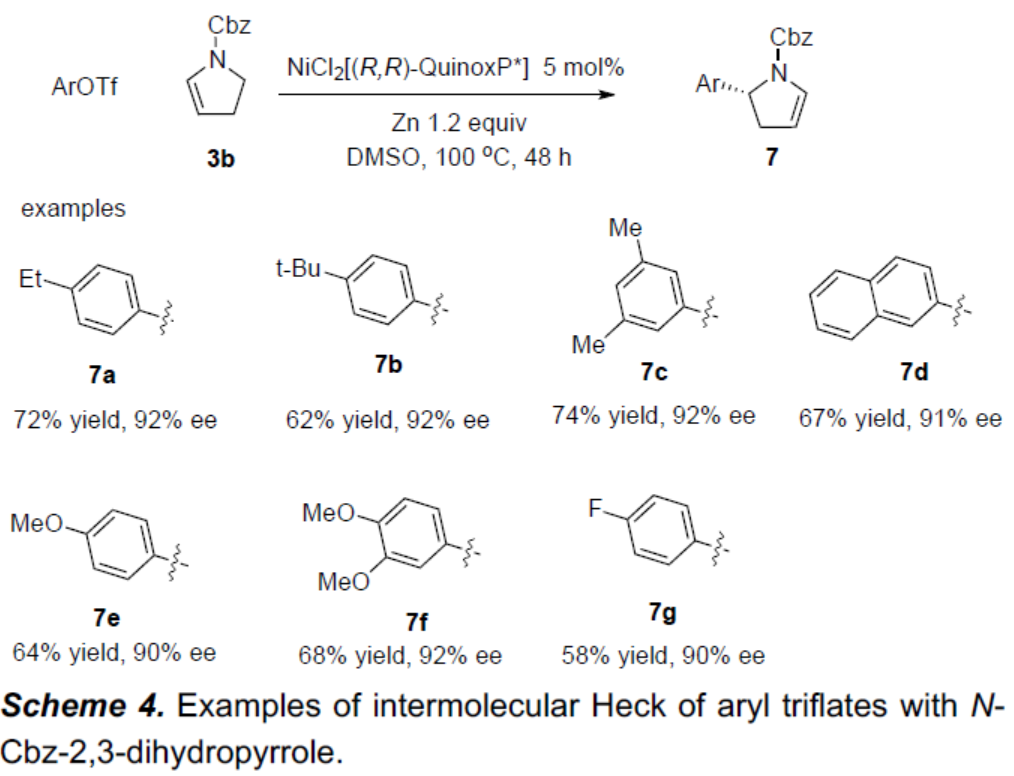
紧接着,作者研究了N-Cbz-2,3-二氢吡咯3b的芳基化反应(Scheme 4)。芳基上带有烷基的底物(7a-7c)或2-萘基取代的底物(7d)均可实现转化。尽管富电子芳基三氟甲磺酸酯可有效的反应,但除四氟苯基三氟甲磺酸酯(7e-7g)外的大多数缺电子芳基亲电试剂的收率均很低。
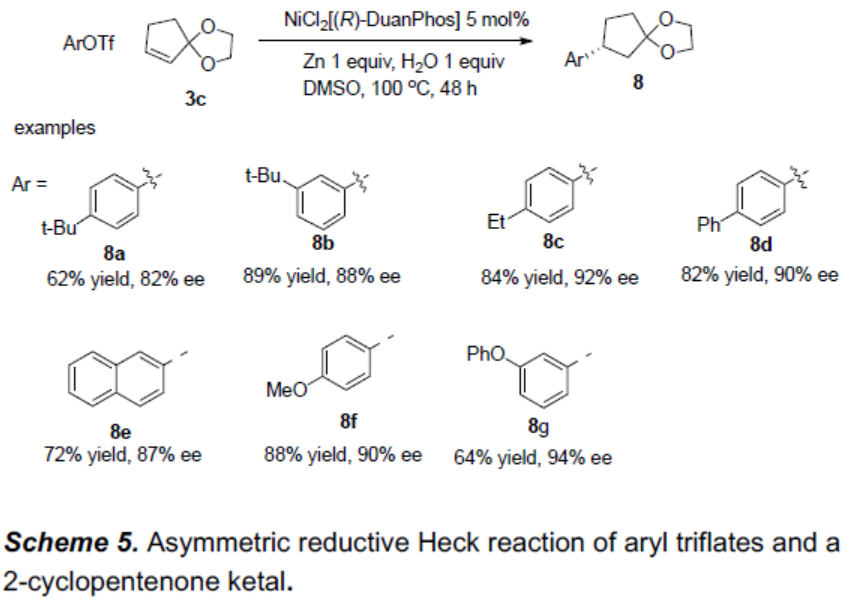
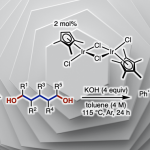
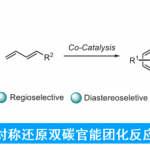
最后,作者还对2-环戊烯酮缩酮3c的底物进行了扩展(Scheme 5)。值得注意的是,需向反应体系中加入1当量的水,可将关键中间体中的镍碳键被水质子化以释放出最终产物。反应结果表明,富电子芳基三氟甲磺酸酯(8a-8c,8f-8g)、萘基(8e)和联苯衍生物(8d)均与体系兼容。然而带有三氟甲基和酯基的缺电子的芳基三氟甲磺酸酯只能提供痕量的产物。环己烯酮缩酮也没有反应。
最后,作者也进行了相关的实验研究以及DFT计算。通过实验表明,Ni(cod)2和QuninoxP*可形成预催化剂[Ni(cod)(QuinoxP*)],该催化剂在100 ℃时可促进某些芳基三氟甲磺酸酯的Heck插入,而无需还原剂,如锌粉。因此,作者认为该反应更倾向与经典的nickel(0)/(II)催化循环的过程。
总结
北京大学深圳研究生院周建荣课题组通过使用NiCl2[(R,R)-QuinoxP*]作为催化剂,实现了 Ar-X(X=OTf、OMs和OTs)与环烯烃的不对称分子间Heck反应以及2-环戊烯酮缩酮底物的不对称还原Heck芳基化反应。
参考文献
[1] J.-N. Desrosiers, J. Wen, S. Tcyrulnikov, S. Biswas, B. Qu, L. Hie, D. Kurouski, L. Wu, N. Grinberg, N. Haddad, C. A. Busacca, N. K. Yee, J. J. Song, N. K. Garg, X. Zhang, M. C. Kozlowski, C. H. Senanayake, Org. Lett. 2017, 19, 3338.[2] Examples: a) X. Qin, M. W. Y. Lee, J. S. Zhou, Angew. Chem., Int. Ed. 2017, 56, 12723; Angew. Chem. 2017, 129, 12897; b) X. Qin, M. W. Yao Lee, J. S. Zhou, Org. Lett. 2019, 21, 5990.
[3] F. Yang, Y. Jin, C. Wang, Org. Lett. 2019, 21, 6989.


















No comments yet.