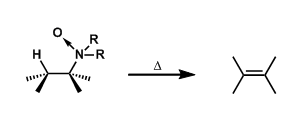
吡啶2,6-双(恶唑啉)(pybox)最早是由Nishiyama团队[1]提出的,它的手性来源于易得的手性2-氨基醇,可作为多种过渡金属的强配位三齿手性配体(Figure 1a)。因此,吡啶2,6-双(恶唑啉)广泛用于过渡金属催化的不对称化学反应中,但与该配体配位的金属必须与三个亚胺基团配位,这极大地降低了金属的电子密度,不利于过渡金属催化反应的进行。因此,德国马尔堡菲利普大学Meggers课题组提出利用环金属配体与pybox配体互补的策略来提高pybox配体在不对称催化中的作用。环金属N-杂环卡宾配体不仅可以调节Ru中心和催化中心的催化活性,还在不对称合成中发挥重要作用。(Figure 1b)。同时,Meggers课题组 (化学空间:Meggers教授介绍)成功报道了Ru-pybox/环金属N-杂环卡宾配合物催化异恶唑的不对称异构化反应以及磺酰叠氮化物和磺酰胺叠氮化物的不对称C(sp3)‒H胺化反应(Figure 1c)。相关研究成果发表于
“Complementing Pyridine-2,6-bis(oxazoline) with Cyclometalated N-Heterocyclic Carbene for Asymmetric Ruthenium Catalysis”
Li, L.; Han, F.; Nie, X.; Hong, Y.; Ivlev, S.; Meggers, E.* Angew. Chem. Int. Ed. 2020, Early View. DOI: 10.1002/anie.202004243
Figure 1 背景研究
论文概要
作者合成了一系列的新型Ru-pybox催化剂,然后以异恶唑1为模板底物,通过对催化剂、催化剂用量以及反应温度等反应条件反复筛选,确定最优反应条件(Table 1):0.1 mol% Ru5为催化剂,CHCl3为溶剂,在30℃条件下反应3小时,能以99%的收率和97%的对映选择性得到产物5a。
Table 1 条件筛选
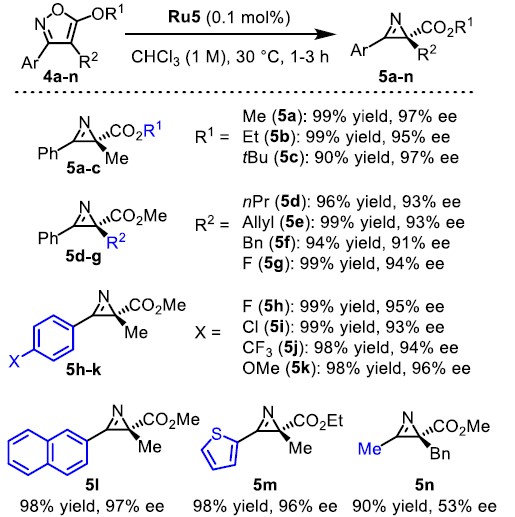
在最优反应条件下,作者对异恶唑的底物范围进行了考察。各种酯基取代或芳基、萘环以及杂环取代的异恶唑均能较好的适应反应条件,能以优秀的收率和对映选择性得到相应产物。
Figure 2 底物扩展
接着,作者将这种新型催化剂用于不对称C(sp3)‒H胺化反应(Figure 3)。Ru5能催化磺酰叠氮化物6发生环化反应,可以99%的收率和90%的对映选择性得到手性环状磺酰胺(R)-7。同时,在Ru5催化作用下,磺酰胺叠氮化物8会发生不对称C(sp3)‒H胺化反应,但只能以75%的收率和70%的对映选择性得到手性1,2-二胺的前体环状磺酰胺(S)-9,若将催化剂换成Ru7,相应产物的收率和对映选择则会提高很多。
Figure 3 催化剂在不对称C(sp3)‒H胺化反应中的应用
论文总结评价
德国马尔堡菲利普大学Meggers课题组提出简单高效的利用环金属N-杂环卡宾配体与Ru-pybox配体互补的策略,其中环金属配体不仅可以调节Ru中心和催化中心的催化活性同时还不对称合成中发挥重要作用。同时,Meggers课题组成功报道了Ru-pybox/环金属N-杂环卡宾配合物催化异恶唑的不对称异构化反应以及磺酰叠氮化物和磺酰胺叠氮化物的不对称C(sp3)‒H胺化反应。
参考文献
- [1] Nishiyama, H.; Sakaguchi, H.; Nakamura, T.; Horihata, M.; Kondo, M.; Itoh, K. Organometallics 1989, 8, 846-848. DOI: 1021/om00105a047
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.