在上回中,小编介绍了一种减压过柱法(DCVC)。
并且在以前的记事中,相关于色谱的记事也有过不少介绍,如果有需要的童鞋可以回顾下
1. 薄层色谱 thin-layer chromatography (TLC)
2. 这些年不清不楚的色谱柱的小Tips
3. 硅胶-你不知道的秘密
4. 含锡副产物的除去方法:碳酸钾/硅胶(分离纯化技巧系列专题)
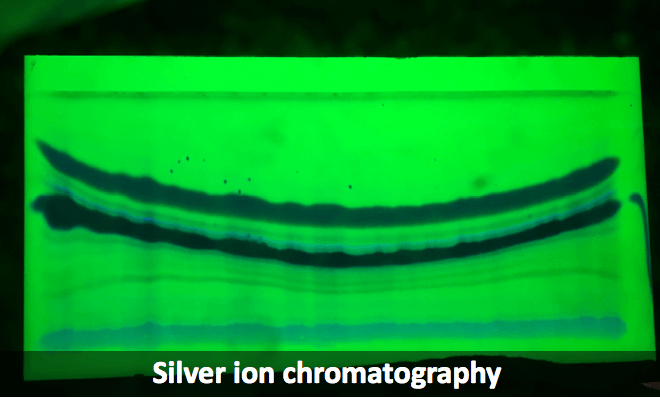
而这次介绍的主题是银离子硅胶色谱,也就是硅胶性质上的改变(银盐预处理过的硅胶)。而我们都知道,分离效果上,硅胶的好坏也是非常重要的。银离子硅胶色谱主要是用于分离含有不饱和键的有机化合物的一种色谱柱。
背景
可能大家对于trans脂肪酸,或者一些食用油中的脂肪酸都有所耳闻。我们身边很多分子都含有不饱和键,而很多情况下并不容易分离纯化。另一方面,很多报道表明银离子可以与很多不饱和键配位鳌合,1937年Lucas等人报道了银离子与C-C不饱和键之间形成的螯合物的性质1)、第二年,他有报道了利用平衡常数对螯合物进行的定量调查报告2)。在那之后、1961年~1962年通过银与多重结合键的鳌合配位的原理,Dutton等人开发出了银离子分离色谱3)、B. de Vries等人4)、Barrett等人5)、L. J. Morris6)等人也相继对该方面的研究有所报道。
在银离子分离色谱的方法报道后,脂质化学中关于脂肪酸或者脂肪酸酯的分离也随着有了发展7), 8)、通过对一般的烯烃、炔烃的分离纯化方法调查数据来看9)、多数研究人员都运用了银离子分离色谱进行分离。
原理
Dewar给出了他所提倡的银离子与碳-碳双键鳌合的轨道间相互作用的原理示意图,如下所示。
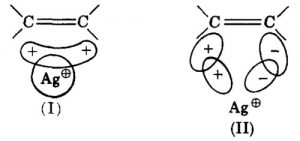
引用自参考文献7
硅胶上附载的银离子一般来源于硝酸银,其他的如高氯酸银,四氟硼酸银也有用到,根据他们的浓度不同,分离纯化的相互作用的序列也会改变。
这是由于与不同数量的银离子形成银-烯烃螯合物的相互作用的强度与形态的不同所导致的10)。
化合物与银离子形成的螯合物与硅胶载体的相互作用强度有如下倾向
- 双键等不饱和键的数量越多相互作用越强
- Z体比E体相互作用更强
- 非共轭的双键相互作用更强
- 存在多个双键的化合物、双键离的远的相互作用强
- 羧酸・羧酸酯的情况,不饱和键与羰基近的话更强
相互作用越强,那么在硅胶上滞留时间越久,也就是说TLC上看的话Rf值越小。
优点
- 可以分离酸性硅胶TLC等很难分离的E,Z异构体。
- 不仅仅只能用于TLC,也可以用于硅胶色谱柱,可以用于scale up。
- 已经有多数研究人员用到,所以其分离条件很容易查询。
缺点
- 有银的存在,所以废弃的时候要注意
- 试验台或者手上碰到硝酸银溶液的话,会变成氧化银附着,变黑(用稀硝酸洗的话可以洗去)
实验步骤
作为反应追踪用的TLC的场合
- 将硝酸银溶在乙腈中做成5~20%浓度的溶液。
- 将溶液移到小瓶中,点板后的TLC蘸着使用即可。
PTLC的情况下
- 与上述1.同样
- 爬板的方法都一样,在干燥的时候用铝箔纸盖着戳几个孔,在通风好的地方自然干燥。
硅胶柱分离使用的时候
- 与TLC一样
- 把硅胶(一般用普通的酸性硅胶)用硝酸银溶液浸润、在55℃~100℃下干燥
- 装柱,过柱与普通硅胶过柱一样。
总结
这一次小编介绍了下银离子附载的硅胶层析法。本手法不仅仅对含有立体差异性多重结合键的化合物分离有效,并且对于数量,位置差异的同样适用。
同时,HPLC column也有售,有兴趣的可以搜下看看。
本方法对于研究含有多个双键或者不饱和键的化合物的童鞋应该是一项利器,而且方法很简单,有兴趣的可以尝试一下!
参考文献
- W. F. Eberz, H. J. Welge, D. M. Yost, H. J. Lucas, J. Am. Chem. Soc., 1937. 59, 45-49. DOI: 10.1021/ja01280a011
- S. Winstein, H. J. Lucas, J. Am. Chem. Soc., 1938. 60, 836-847. DOI: 10.1021/ja01271a021
- H. J. Dotton, C.R. Scholfield, E. P. Jones, Chem. Ind.(London), 1961, 1874-1876.
- B. de Vries, Chem. Ind.(London), 1962, 1049-1050.
- C. B. Barret, M. S. J. Dallas, F. B. Padley, Chem. Ind.(London), 1962, 1050-1051.
- L. J. Morris, Chem. Ind.(London), 1962, 1238-1240.
- L. J. Morris, J. Lipid Res., 1966, 7, 717-732.
- G. Dobson, W. W. Christrie, B. N-.Damyanova, J. Chromatogr. B, 1995, 671, 197-222.
- C. M. Williams, L. N. Mander, Tetrahedron, 2001, 57, 425-447.
- W. Featherstone, A. J. S. Sorrie, J. Chem. Soc, 1964, no vol, 5235-5242.
- 新しい銀イオンクロマトグラフィー用HPLCカラム”Silver column KANTO”の開発(1)
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!




















No comments yet.