2022年2月16日,北海道大学李响课题组在专业杂志Advanced Materials上在线发表了题为 「Star-Polymer–DNA Gels Showing Highly Predictable and Tunable Mechanical Responses」的科技论文,该研究开发了以DNA双链结构为交联点的水凝胶材料,该材料的交联速率是易被控制的。
https://onlinelibrary.wiley.com/doi/epdf/10.1002/adma.202108818
01
—
研究亮点
- 制作以DNA双螺旋结构为交联点的水凝胶。
- 通过设计双螺旋结构的稳定性,可以预测和控制水凝胶的流动性。
- 该材料有望应用于医疗材料,如流动性接近生物体的细胞培养基和可注射凝胶材料等。
02
—
研究概要
【背景】
水凝胶是一种聚合物材料,由聚合物进行三维交联而成。由于含有大量水分,具有与活体组织相似的柔软性和流动性(粘弹性),因此有望用作医疗材料。最近的研究揭示了适当控制凝胶的柔软性和流动性的重要性。例如,在再生医学领域,凝胶被用作细胞生长的支架材料(培养基),但如果凝胶不具有与活体组织相同的柔软性和流动性的话,细胞就不会正常生长。凝胶也可用作注射药物保持介质,但已经发现,如果凝胶不具有适当的流动性,则注射功能和保持药物的功能是不相容的。凝胶的柔软度可以通过调节交联速率来控制,流动性可以通过调节交联的稳定性(解离行为)来控制。在本文中,研究小组聚焦于调节交联速率,开发了星形聚合物凝胶化法。该方法使合成具有设计柔软性的水凝胶成为可能。然而,交联的稳定性仍然难以按预期控制,在生理条件下还没有成功的案例。
示意图:DNA双链结构的凝胶(从左到右)
【结果与讨论】
DNA是一种存在于所有生物体中的物质,呈双螺旋结构。这种双螺旋结构的稳定性根据 DNA 的碱基序列变化很大,它可能会在不到1秒的时间内解离,也可能非常稳定。研究小组认为,可以通过合成包含这种DNA双螺旋结构的水凝胶来自由控制凝胶的流动性。在本研究中,研究人员合成了一种四足型高分子(四聚乙二醇)和DNA双螺旋结构交联而成的水凝胶。研究了DNA双螺旋结构与水凝胶稳定性的关系。使用DNA结构计算程序可以部分预测DNA双螺旋结构的稳定性;在本研究中,它在生理条件下是稳定的。为了使双螺旋结构可以简单地解离而无需经过复杂的半稳定结构,特意设计了DNA碱基序列(16个碱基对)。
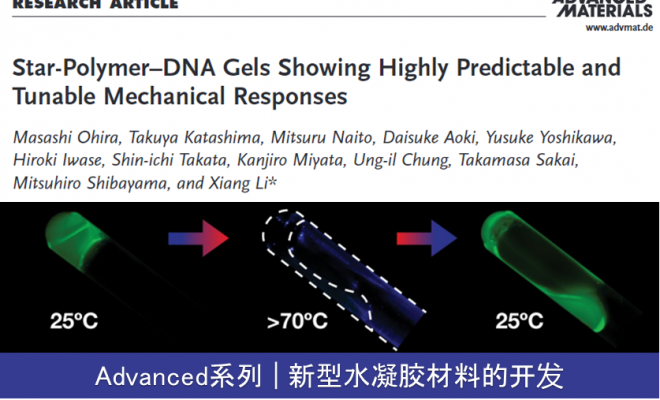
合成的 DNA 凝胶无色透明,加热至 70ºC 左右变为溶液(溶胶状态),冷却至生理条件后恢复凝胶状态(图1)。仅在存在DNA双螺旋结构的情况下将显示荧光的试剂添加到凝胶中时,仅在凝胶状态下观察到荧光,确认凝胶是由DNA双螺旋结构的形成形成的。
图1. (左)DNA水凝胶模式图。(右)形成的DNA双链反复进行解离与结合。放入试管的DNA凝胶;温度上升时DNA凝胶呈液体。被荧光色素标记的DNA发出绿色荧光。
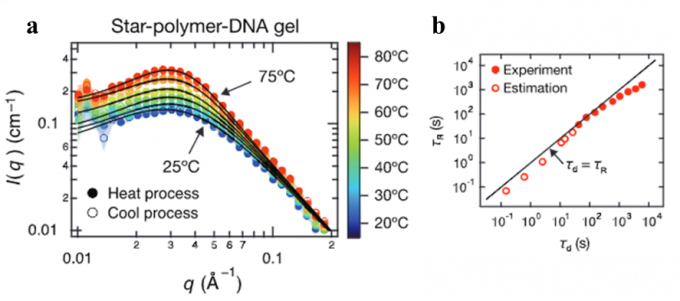
此外,使用小角中子散射法评估 DNA 凝胶的纳米结构时,DNA 间保持一定距离且原样存在于凝胶中,并形成了有序的网络结构(图2a)。
随后,当在各种温度条件下测量DNA凝胶的宏观流动性和作为交联点的DNA双螺旋结构的稳定性时,凝胶流动时间为DNA双螺旋结构的解离时间在 0.1 – 2000 秒的宽时域内一致(图 2b)。该结果表明:通过调节DNA双螺旋结构的稳定性,可以准确预测和控制凝胶的流动性。由于DNA双螺旋结构的稳定性可以通过设计DNA的碱基序列来自由调节,理论上,利用新开发的DNA凝胶制备方法可以在生理条件下获得任意流动性。未来,该课题组计划实际调整DNA碱基序列,开发具有各种流动性的水凝胶。
图2. (a) 小角中子散射图。(b)凝胶流动性与DNA双链结构的解离时间关系;两者在0.1-2000秒间广域范围内的变化是一致的。
【展望】
本次开发的凝胶流动性控制技术有望应用于细胞培养基和注射用凝胶材料。 此外,利用对温度和pH等外部环境有反应的DNA和肽等添加剂的特性,有望应用于传感器和软机器人开发。 另外,如果扩展DNA双螺旋结构稳定性的数据库,就可以利用计算科学从DNA的碱基序列直接计算凝胶的流动性,从而开发凝胶流动性计算算法。只需通过以上计算,我们就能提供按需流动性的凝胶材料。
本研究由北海道大学,东京大学,东京工业大学和日本综合科学机构中性子科学心中共同合作完成;第一作者为Masashi Ohira,通讯作者为李响(Xiang Li)副教授。本文受到JSPS 科研費・若手研究(JP17K14536,JP19K15628,JP20K15338),特別研究員奨励費 (JP20J22044),基盤研究A(JP16H02277,JP21H04688),学術変革領域研究 B(20H05733), 科学 技術振興機構(JST)創発的研究支援事業(JPMJFR201Z),センター・オブ・イノベーションプログラ ム(JPMJCE1304,JPMJCE1305)和戦略的創造研究推進事業(JPMJCR1992)的经费支持。
03
—
作者介绍
李响(Xiang Li),自2021年起任北海道大学先端生命科学研究院PI副教授。李教授致力于高分子软物质材料开发的基础研究,是高分子溶液物质和高分子电解质研究领域的新星学者。曾获2014年日本高分子凝胶学会优秀演讲奖,2016年亚洲–大洋洲中子散射协会青年学者奖,2019年日本高分子学会研究鼓励奖和2021年东京大学ISSP学术奖等奖项;在Advanced Material,Macromolecules,Nature系列 等国际知名科学杂志发表研究型论文40余篇。


————————————–华丽分割线———————————-
关注化学空间,追踪前沿方向!
文章投稿和合作请联系微信 ylyl5200
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载






















No comments yet.