作者:石油醚
导读:
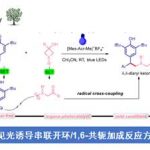
近日,华中科技大学钟芳锐教授团队在著名学术期刊Angew. Chem. Int. Ed.发表论文,报道酶催化不对称交叉氧化偶联反应新进展。该反应利用铜外排氧化酶(CueO)催化吲哚类底物的氧化交叉偶联反应,合成了一系列光学纯2,2-二取代吲哚啉-3-酮类化合物,具有条件温和、催化剂经济、选择性高、底物普适性好等优点,所制备的光学纯吲哚3-酮衍生物ee值高达99%。在此基础上,作者筛选了部分产物的生物活性筛选,得到了两个具有显著抗肿瘤活性分子。
“Expanding the Promiscuity of a Copper-Dependent Oxidase for Enantioselective Cross-Coupling of Indoles
Huan Guo, Ningning Sun, Juan Guo, Tai-Ping Zhou, Langyu Tang, Wentao Zhang, Yaming Deng, Rong-Zhen Liao, Yuzhou Wu, Guojiao Wu, Fangrui Zhong*
Angew. Chem. Int. Ed. 2023, ASAP. doi:10.1002/anie.202219034”
正文:
氧化交叉偶联反应是有机合成中发展的绿色高效工具,可以将两个富电子亲核试剂直接形成C-C键,具有显著的原子经济性(图 1)。已知的不对称催化主要是基于化学氧化或光化学/电化学氧化与手性过渡金属或有机催化剂的组合,其挑战在于同时控制氧化步骤的化学选择性和偶联步骤的对映选择性。氧化还原酶具有催化不对称氧化偶联的巨大潜力,如自然界中,漆酶催化的γ-萘酮同分异构体(M)-ustilaginoidin A的不对称同源二聚反应,具有专一的区域和对映选择性(图 1b)。然而,非天然底物的酶促对映选择性氧化偶联反应仍然很少。2022年,Narayan小组利用工程化P450酶实现了酚类分子生物催化交叉偶联反应,为轴手性联芳基分子的合成提供了有效策略 (图1c)。
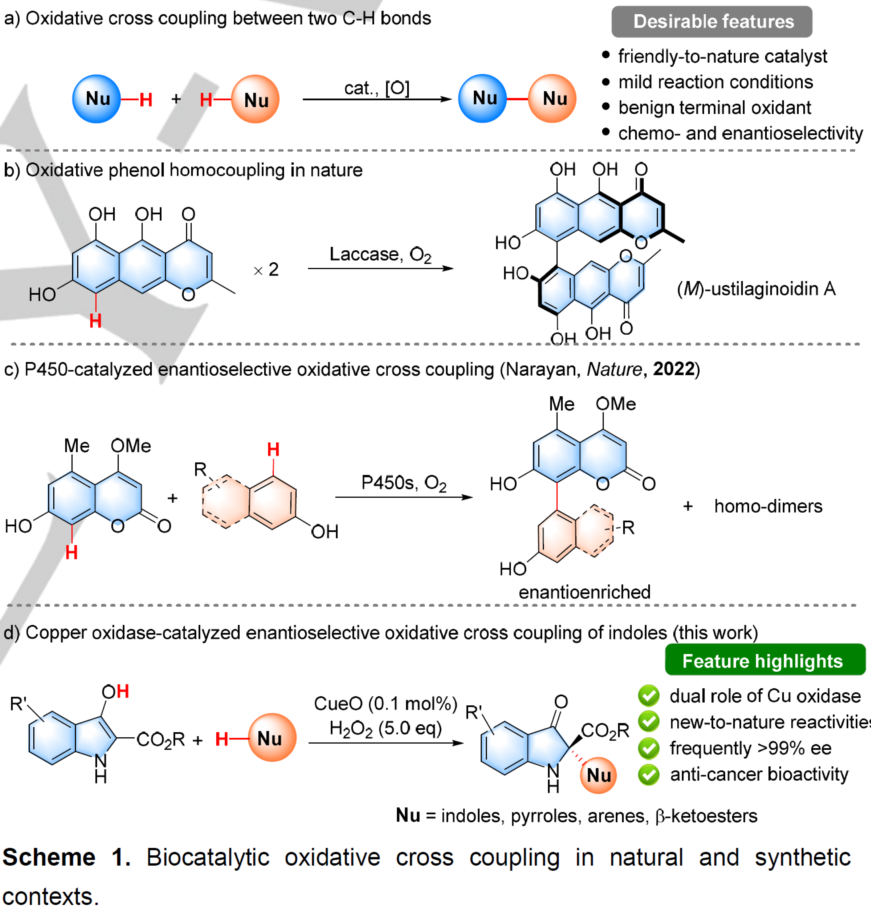
图1. 图片来源:(Angew. Chem. Int. Ed.)
钟芳锐教授长期致力于绿色仿生和生物催化领域的研究,利用化学原理驱动酶催化选择性合成的理念,基于铜催化氧化偶联反应的化学机制,发展了多铜氧化酶催化的多酚氧化环加成反应(Green. Chem., 2022, 24, 5598.);发展了含有非天然光敏活性基团的人工光敏金属酶(J. Am. Chem. Soc. 2021, 143, 617)和“三重态光酶”(Nature, 2022, 611, 715)。
在此前工作基础上,该课题组最近开展了铜酶催化非天然底物的不对称氧化交叉偶联反应的研究并取得重要进展,在温和的水相条件下实现了铜酶CueO催化吲哚酚与一系列亲核试剂的对映选择性氧化交叉偶联,成功应用于光学纯2,2-二取代吲哚啉-3-酮类化合物的手性合成(图 1d),并对酶促反应机理进行了初步探讨。
该团队以大肠杆菌培养表达的铜酶CueO裂解液为催化剂,以3-羟基吲哚-2-羧酸和吲哚为模型反应,最优条件下(0.1 mol% CueO,5.0当量双氧水,Tris/CH3CN为溶剂,25℃,24小时)可以得到目标产物,收率为92%,对映选择性为99%。酶的用量较低,反应转化数了920.
在最优条件下,作者探索了此类反应的底物普适性和官能团兼容性(图2)。苯环上含有不同电子和立体性质取代基的吲哚酚能顺利发生预期反应,收率为73-78%,立体选择性一般都为99%ee。此外,不同位置取代的吲哚亲核试剂、富电子类吡咯、1,3,5-三甲氧基苯和1,3-二甲氧基苯也同样适用。亲核试剂的范围还可以进一步扩展到sp3杂化的碳亲核试剂,如环状和非环状β-酮酸酯,相应的产物均具有极好的立体选择性。部分底物的放大实验(0.3-1.0 mmol)发现,产物的产率和光学纯度不受影响。

图2. 代表性底物
研究团队对该酶促反应的机理进行了深入的研究(图3)。首先通过控制实验捕获和验证了中间体分子的生成。在此基础上,通过铜的配位环境分析、中间体分子与酶的分子对接模拟等实验,提出了底物与酶的可能作用模型:中间体的酯基与CueO酶Asn240的酰胺N-H和Lys188的氨基存在着弱氢键作用;这些相互作用可能对交叉偶联反应的反应性和对映选择性至关重要。当将这两个氨基酸残基突变成丙氨酸,所得突变体CueO_K188A和CueO_N240A的催化效果显著降低。这一结果验证了上述推测的酶作用方式的合理性。
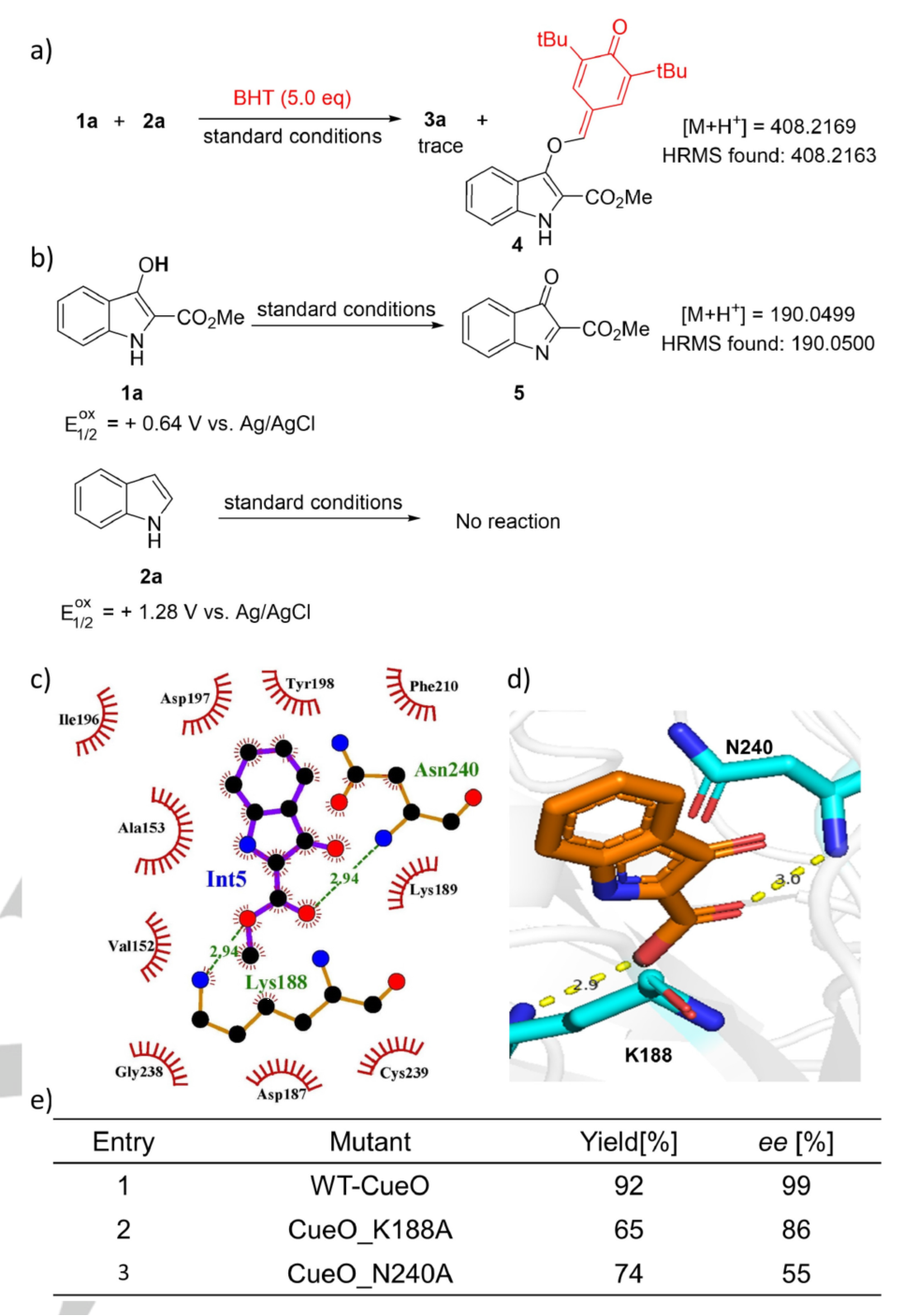
图3. 图片来源:(Angew. Chem. Int. Ed.)
相关文献表明,2,2-二取代吲哚啉-3-酮类分子可能具有显著的生物活性。该团队利用MTT法测定了部分产物对MCF-7肿瘤细胞系的毒性,得到了两个具有显著抗癌活性的化合物3f和4a(浓度为50μM)(图4)。进一步在不同浓度下的毒性测试实验拟合得到IC50值分别为34.31 μM和37.2 μM,均高于临床药物伊立替康和5-氟尿嘧啶。
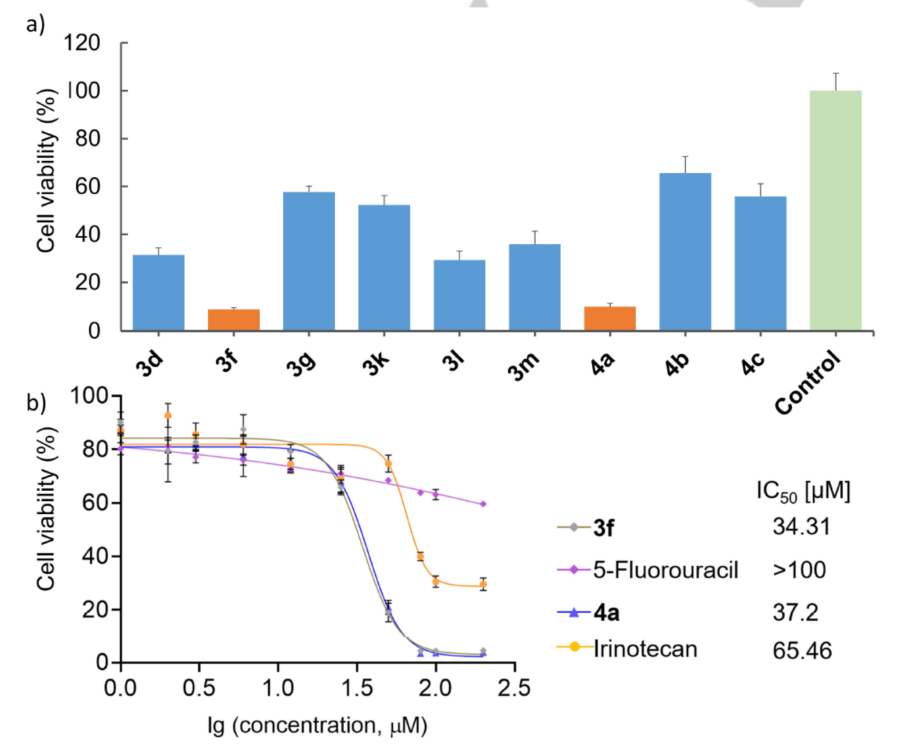
图4 图片来源:(Angew. Chem. Int. Ed.)
总结
总之,钟芳锐教授课题组以基于铜催化的交叉偶联反应化学机制,以铜酶CueO为生物催化剂,以H2O2为终端氧化剂建立了一种不同吲哚分子间的对映选择性氧化交叉偶联反应,具有操作简便、高原子经济性、较好的底物普适性等特点。该方法提供了一种光学纯2,2-二取代吲哚酮的绿色合成方法,并筛选得到了两个显著抗癌活性分子。这项工作显著拓展了多铜氧化酶的催化杂泛性,将为发展铜酶催化的其它非天然氧化反应带来启发。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载

















No comments yet.