作者:石油醚
导读
近日, 芝加哥大学的董广彬教授课题组和加州大学伯克利分校的Michael F. Crommie教授课题组在J. Am. Chem. Soc.上发表论文,报道了通过迭代的Suzuki–Miyaura偶联的合成策略(PAIS),成功地制备了一系列单分散的石墨烯纳米带,并使用基质辅助的直接转移技术(matrix assisted direct transfer,MAD transfer)和化学键分辨的扫描隧道显微技术(bond-resolved scanning tunneling microscopy,BRSTM)对这些产物进行了表征。文章第一作者为芝加哥大学博士后尹江亮和加州大学伯克利分校博士后Peter H. Jacobse。
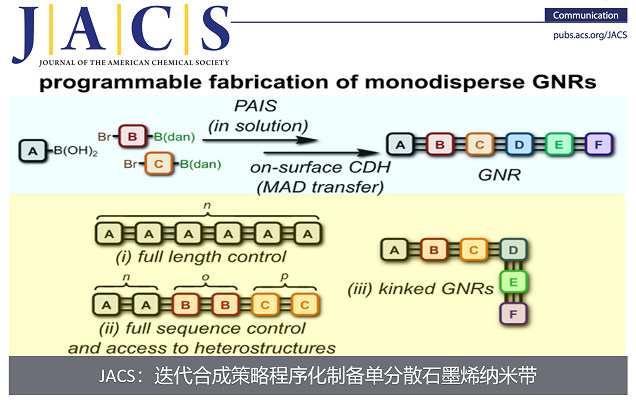
Programmable Fabrication of Monodisperse Graphene Nanoribbons via Deterministic Iterative Synthesis.
Jiangliang Yin,⊥ Peter H. Jacobse,⊥ Daniel Pyle, Ziyi Wang, Michael F. Crommie,* and Guangbin Dong*.
J. Am. Chem. Soc.2022, 144, 16012-16019. doi: 10.1021/jacs.2c05670.
正文
自从单层石墨烯问世以来,它所具有的优异性质如高的载流子迁移率、高比表面积、良好导热性、高杨氏模量、高光学透明性等使它在柔性光电器件等方面具有重要的应用前景。但是在半导体应用方面,石墨烯有它的局限性,因为石墨烯缺少带隙,其导电性本质上是半金属的。所以对石墨烯进行改造以引入带隙从而将其应用于半导体领域是十分必要的,此时,石墨烯纳米带(GNR)应运而生。石墨烯纳米带是宽度在纳米尺寸的条状石墨烯,由于量子限制效应,石墨烯纳米带具有可调的带隙,这使它有可能被应用于半导体领域。
众所周知,结构决定性质,石墨烯纳米带的物理性质主要取决于它的结构,如长度、宽度、边缘类型、缺陷等等,所以合成结构精准的石墨烯纳米带是十分重要的1, 2。制备石墨烯纳米带的方法主要有两种,一种是自上而下(top-down)的策略,由这种策略制备的石墨烯纳米带的结构不能够被精确地控制,从而导致性质的不稳定。另外一种是自下而上(bottom-up)的合成策略,这种策略能够较好地控制石墨烯纳米带的结构,包括宽度、边缘类型等。但是已有的自下而上的合成方法也有着很大的局限性,例如,利用已发展的聚合反应得到的石墨烯纳米带通常是一个长度不一的多分散的混合物,这势必会导致性质的不确定性。另外,传统的聚合反应只能够有次序地控制一种或两种单体的聚合,不能够有效控制三种或三种以上单体的聚合。这些局限性极大地限制了对石墨烯纳米带的性质及多样性的研究,所以发展一种可以完全控制石墨烯纳米带的长度以及单体顺序的合成策略是十分必要的,同时也充满了挑战(图1)。
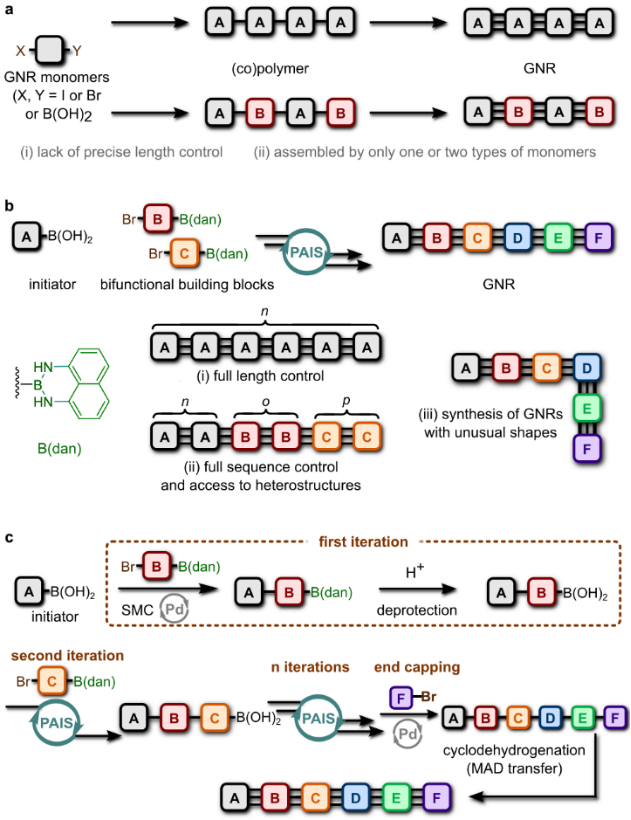
图1. 石墨烯纳米带的合成策略。a, 已有的GNR合成策略及其局限性;b,本文发展的PAIS策略合成结构多样的GNR;c,该合成策略的主要过程。
作者提出了迭代的Suzuki–Miyaura偶联的合成策略(PAIS)去实现单分散石墨烯纳米带的合成,该策略的核心是双官能化单体的使用,该双官能化单体可由二溴代物的顺序的硼化和1,8-萘二胺(dan)保护而得3。首先,起始单体A(苯硼酸)与第一个双官能化单体B进行偶联反应,得到末端为非活性B(dan)的偶联产物AB-B(dan),该产物在酸性条件下能够进行水解反应从而得到末端为活性硼酸的产物AB-B(OH)2,AB-B(OH)2接着与另外一个双官能化单体C进行反应,如此迭代,便可得到由多种不同单体连接的顺序可控的GNR前体。通过使用MAD transfer技术4,该前体可被转移到Au(111)表面上,接着进行表面脱氢环化得到最终的石墨烯纳米带(图1)。
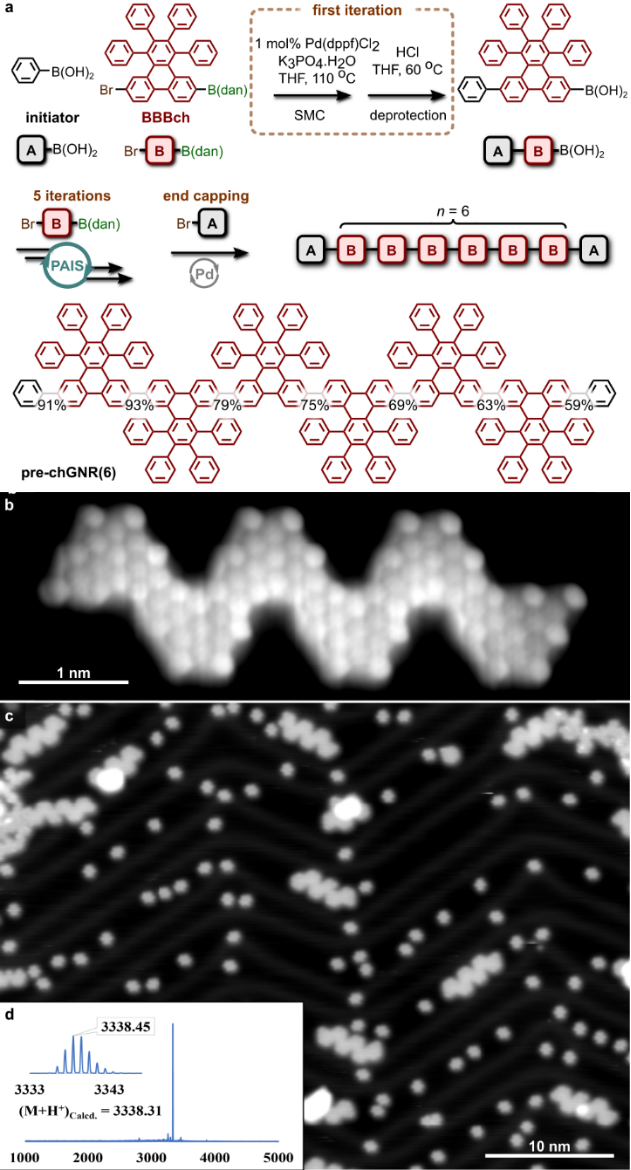
图2.利用PAIS策略合成chGNR(6)
利用该方法,作者首先合成了含有六个重复单元的波浪型的GNR前体pre-chGNR(6),如图2所示,每一步的迭代反应都能够以较好到优异的产率得到对应的产物,证明了该方法的高效性。pre-chGNR(6)的基质辅助激光解吸电离飞行时间质谱(MALDI-TOF-MS)表明该GNR前体的高度单分散性。接着,作者使用MAD transfer技术将GNR前体转移到Au(111)表面上,进行脱氢环化反应以得到最终的GNR。BRSTM图片直接显示出这些GNR的准确结构,大范围的STM图片证明了这些GNR的高度单分散性。
接着,作者合成了含有椅型(armchair)和波浪型(chevron)GNR前体的异质结组合体pre-9-chGNR(图3),基质辅助激光解吸电离飞行时间质谱显示出该GNR前体的高单分散性。BRSTM结果和大范围的STM结果证明最终的GNR的准确结构和高度单分散性。在表面合成该GNR的过程中,N = 9 椅型GNR部分出现了丢失苯环的缺陷,这可能通过溶液氧化环化的策略来避免。基于此,作者又合成了更加复杂的双异质结组合体pre-9-chevron-9AGNR(图4),该GNR前体的表面环化结果十分好,通过统计学分析,94% 的Au(111)表面上的GNR都是预期的结构,缺陷也特别少,这说明在表面合成N = 9 椅型GNR时,砌块BBBo3p表现比砌块BBBp3p好得多。
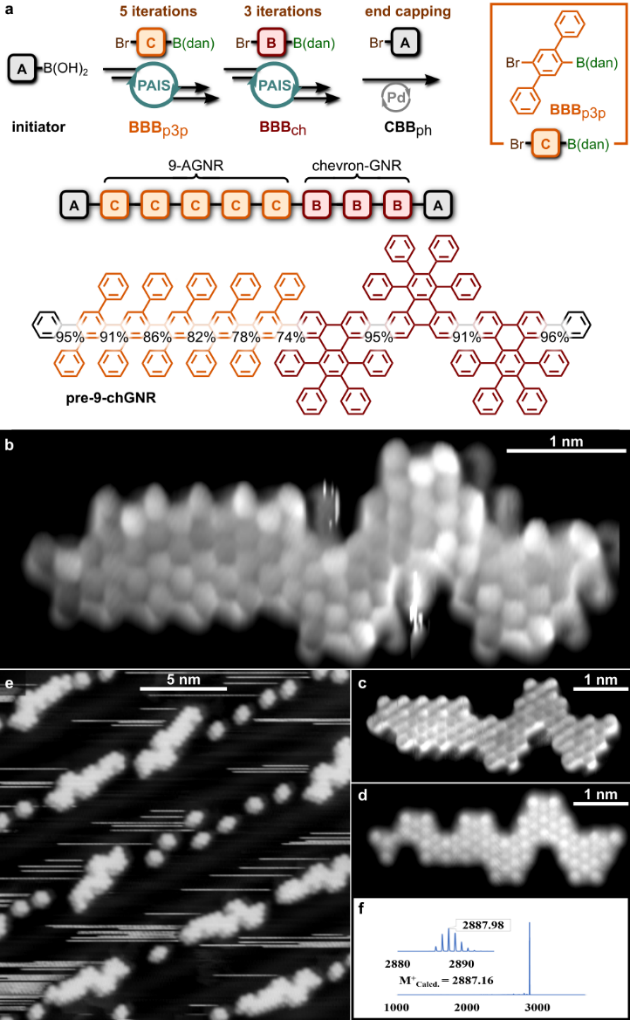
图3. 利用PAIS策略合成异质结的9-chGNR
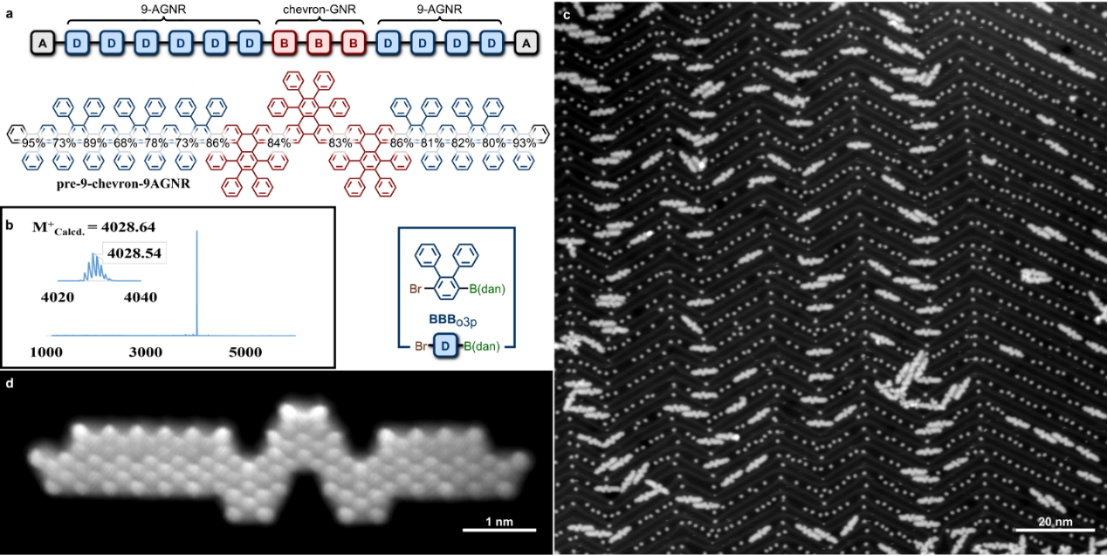
图4. 利用PAIS策略合成双异质结的9-chevron-9AGNR
为了探索PAIS策略在合成更复杂GNR的潜力,作者设计了两个有扭转角的GNR前体,分别为边缘结构为椅型(armchair)的“V”型GNR前体pre-6-V-6-AGNR和边缘结构分别为椅型(armchair)和波浪型(chevron)的“V”型GNR前体pre-9-V-chGNR(图5和图6)。利用该策略,作者能够顺利地得到单分散的两个前体。从STM测试结果来看,这两种GNR的单体顺序完全符合作者的设计,证明了该合成策略在合成复杂GNR的巨大潜力。对于6-V-6-AGNR来说,最后一步的表面环化容易产生一些苯环翻转的异构体,这个问题可以通过溶液氧化环化来解决5。同前面9-chGNR的结果类似,“V”型9-V-chGNR也产生了一些苯环丢失的缺陷,这一缺陷也是在表面环化过程中产生的。
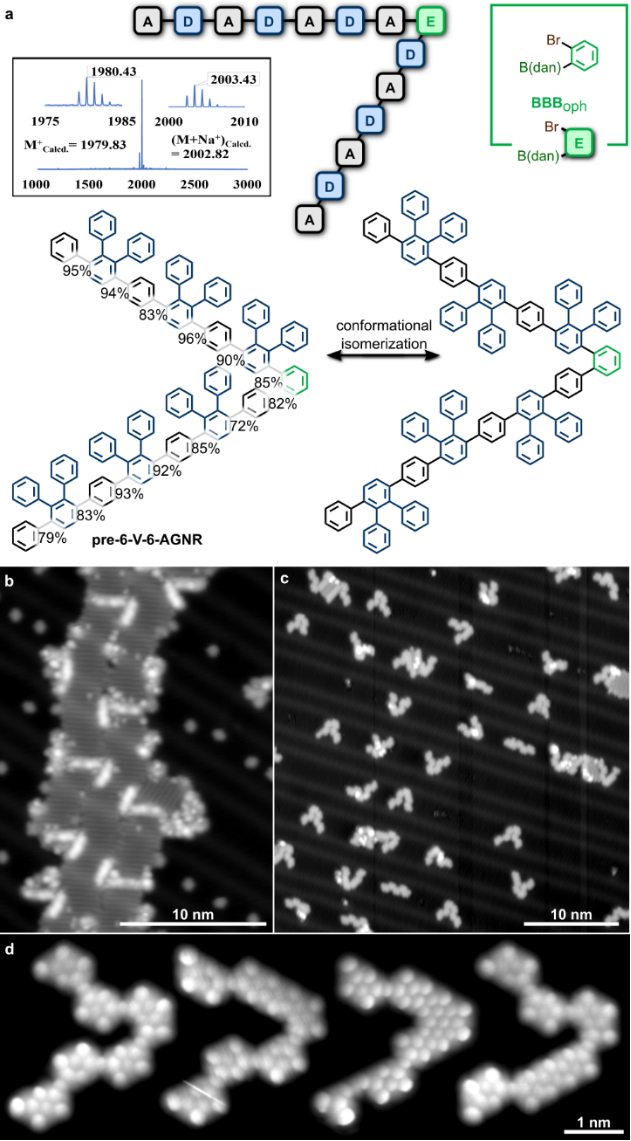
图5. 利用PAIS策略合成具有扭转角的6-V-6-AGNR
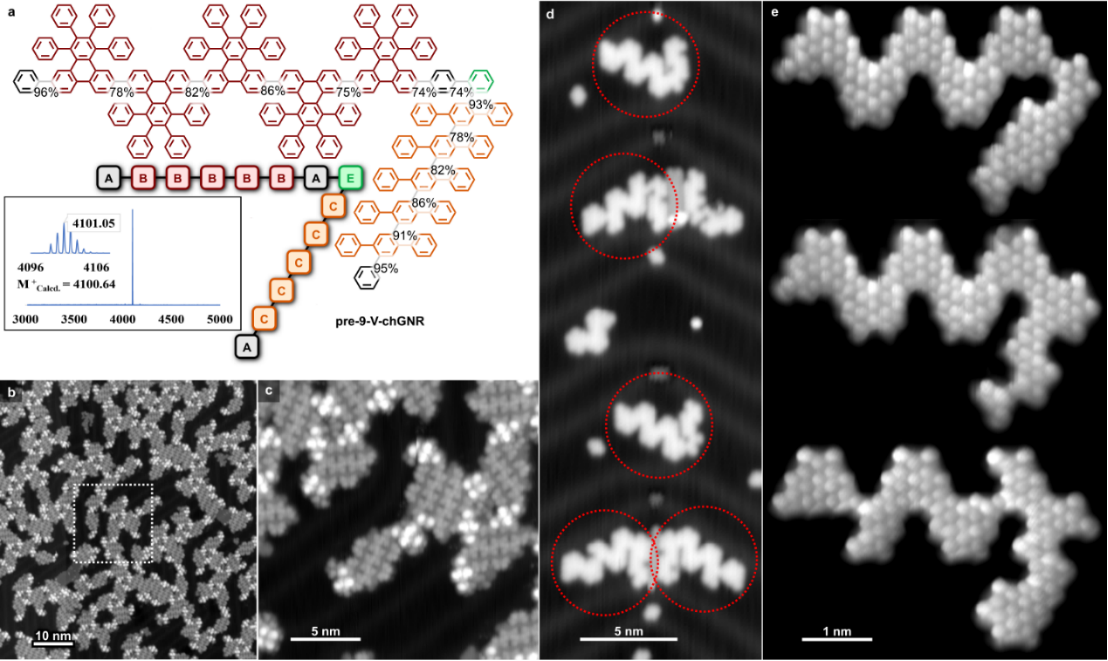
图6. 利用PAIS策略合成具有扭转角的9-V-chGNR
总结
芝加哥大学的董广彬教授课题组和加州大学伯克利分校的Michael F. Crommie教授课题组发展了一种迭代的Suzuki–Miyaura偶联的合成策略(PAIS),利用该策略合成了一系列单分散的GNR前体,并使用基质辅助的直接转移技术(matrix assisted direct transfer,MAD transfer)将这些GNR前体顺利转移到Au(111)表面,在金属表面进行脱氢环化,成功地制备了一系列单分散的石墨烯纳米带,作者利用化学键分辨的扫描隧道显微技术(bond-resolved scanning tunneling microscopy,BRSTM)对这些产物进行了表征。这些单分散性的GNR的成功制备证明了该策略在合成新型单分散GNR方面的巨大潜力,为合成具有优异物理性质的GNR奠定了坚实的基础。
(董广彬教授供稿)
参考文献
- Narita, A.; Wang, X.-Y.; Feng, X.; Müllen, K. New Advances in Nanographene Chemistry. Soc. Rev.2015, 44, 6616.
- Yoon, K.-Y.; Dong G. Liquid-Phase Bottom-Up Synthesis of Graphene Nanoribbons. Chem. Front.2020, 4, 29.
- Noguchi, H.; Hojo, K.; Suginome, M. Boron-masking Strategy for the Selective Synthesis of Oligoarenes via Iterative Suzuki-Miyaura Coupling. Am. Chem. Soc.2007, 129, 758.
- McCurdy, R. D.; Jacobse, P. H.; Piskun, I.; Veber, G. C.; Rizzo, D. J.; Zuzak, R.; Mutlu, Z.; Bokor, J.; Crommie, M. F.; Fischer, F. R. Synergetic Bottom-Up Synthesis of Graphene Nanoribbons by Matrix-Assisted Direct Transfer. Am. Chem. Soc. 2021, 143, 4174.
- Li, G.; Yoon, K.-Y.; Zhong, X.; Wang, J.; Zhang, R.; Guest, J. R.; Wen, J.; Zhu, X.-Y.; Dong, G. A Modular Synthetic Approach for Band-Gap Engineering of Armchair Graphene Nanoribbons. Nat. Commun. 2018, 9, 1687.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载






















No comments yet.