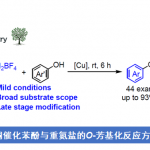
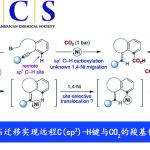
苯并三氮唑可以发生环链异构化形成重氮化物,然后可与不饱和烯烃或炔烃反应生成各种新的有价值的化合物。Nakamura课题组报道了Pd催化苯并三唑与内炔烃的脱氮环化反应[1]。然后,Glorius课题组报道了Ir-光催化苯并三唑与末端炔烃的脱氮反应[2]。最近,Tang课题组应用激活稳定策略实现苯并三唑与炔[3]或1,3-二烯[4]的脱氮反应。丙二烯和N-烯丙胺同样是不饱和烃类化合物,但到目前为止,还没有关于苯并三唑与丙二烯和N-烯丙胺的不对称脱氮环化反应的报道。在上述研究背景的基础上,复旦大学张俊良课题组报道了Pd催化苯并三唑与丙二烯或N-烯丙胺的不对称脱氮环化反应。为了实现该策略,作者需要解决以下几个问题:1)理论上该反应可以生成八种异构体(er, rr, Z/E),其立体选择性和对映选择性较难控制;2)需要防止丙二烯尤其是烯丙胺的二聚化; 3)需要考虑手性膦配体与重氮盐中间体的相容性问题4)需要考虑如何实现产物高对映选择性。相关研究成果发表于
Pd/PC-Phos-Catalyzed Enantioselective Intermolecular Denitrogenative Cyclization of Benzotriazoles with Allenes or N-allenamides
Zhang, P.-C.; Han, J.; Zhang, J.* Angew. Chem. Int. Ed. 2019, Just Accepted Manuscript
DOI: 10.1002/anie.201904805
论文作者介绍:
论文作者:张俊良教授
学习与工作经历:
- 1993年9月-1997年7月,天津大学化学系学习,应用化学专业,理学学士
- 1997年9月-2002年7月,中国科学院上海有机化学研究所,有机化学专业,理学博士,师从麻生明院士
- 2002年8月-2003年10月,中国科学院上海有机化学研究所工作,研究助理。
- 2003年11月-2005年1月,德国科隆大学化学系,洪堡学者,师从H.G.Schmalz教授
- 2005年2月-2006年10月,美国芝加哥大学化学系,研究助理。师从何川教授
- 2006年12月-2017年6月,华东师范大学化学系,教授,博导。
- 2017年9月起,复旦大学化学系,教授,博导。
获奖情况:
- 2007年: 曙光人才和浦江人才计划
- 2009年:中国化学会青年化学奖
- 2009年: 第十二届霍英东基金
- 2010年: 东方学者计划获得者
- 2012年:Thieme Chemistry Journal Award
- 2012年:上海市优秀学科带头人计划获得者
- 2013年:Distinguished Lectureship Award (Japan Chemical Society)
- 2014年:Asian Core Lectureship Award (Singapore)
研究方向:
- 1.新型手性配体的设计与应用
- 2.有机合成新反应设计与开发
- 3.有机功能材料的设计与合成
论文概要:
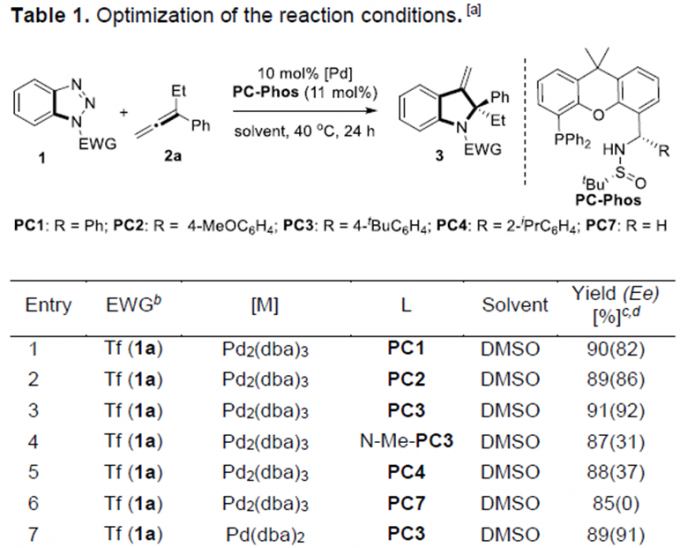
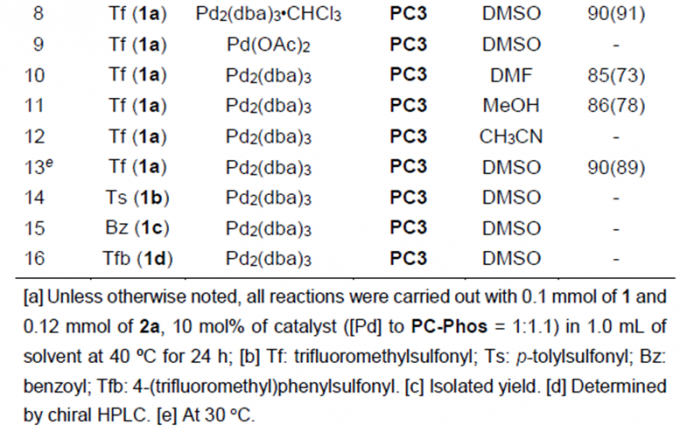
以N1-Tf的苯并三唑1a和丙二烯2a为模板底物,作者对反应条件经反复筛选,确定最优条件为(Table 1):5 mol% Pd2 (dba) 3和11 mol%手性亚膦磺酰胺配体(Sc, Rs)-PC3为催化剂,DMSO为溶剂,在40 ℃条件下反应24 h,能以91%的收率和92%的对映选择性得到相应产物。
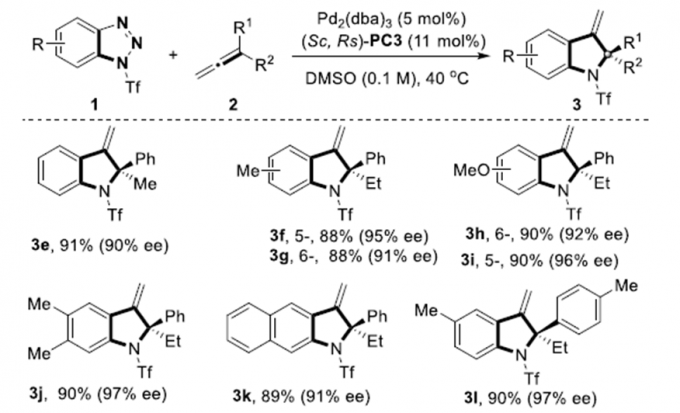
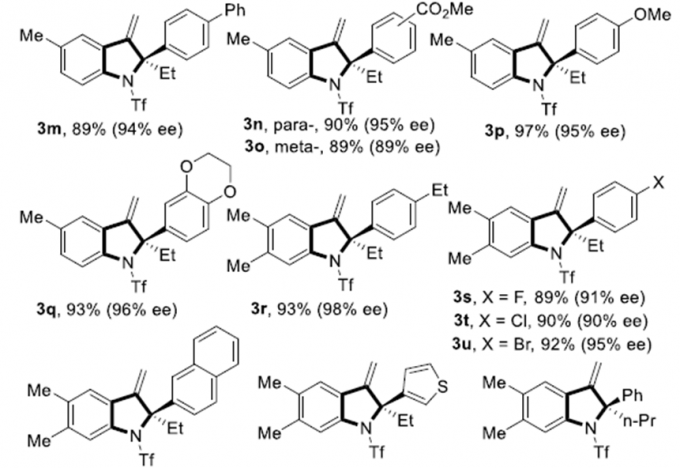
在最优反应条件下,作者对该不对称脱氮环化反应的底物范围进行了考察(Scheme 2)。各种芳环取代的苯并三氮唑和萘并三氮唑均能很好的适应反应条件,能以良好至优秀的收率和对映选择性得到相应产物。同时,各种亲电和吸电子取代的1,1-二取代联烯、2-萘基联烯以及3-噻吩取代的联烯均具有良好的耐受性,能以优秀的收率和对映选择性得到相应产物。
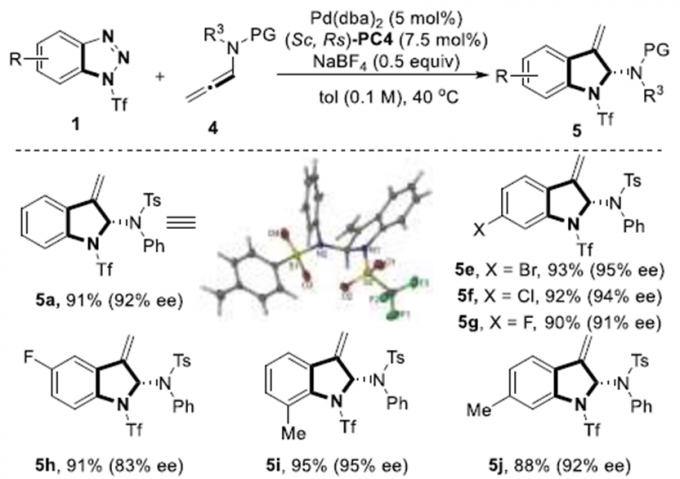
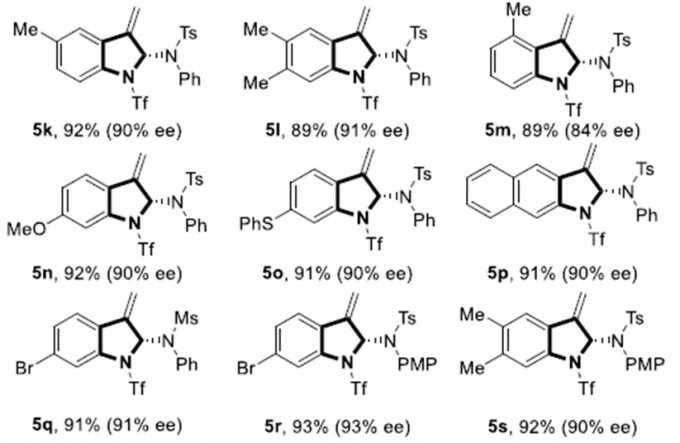
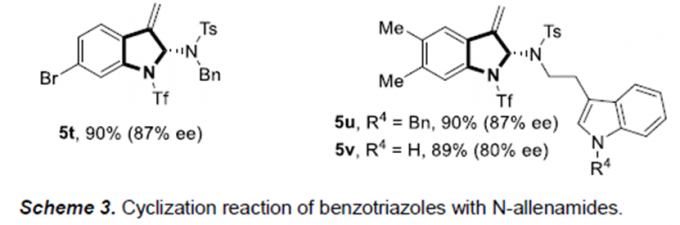
紧接着,作者对N-烯丙胺的反应情况进行了考察(Scheme 3)。在上述最优反应条件下,苯并三氮唑1a和N-烯丙胺4a反应,只能得到少量产物。通过调整反应条件,作者确定最优反应条件为:5 mol%Pd(dba)2和7.5 mol%手性亚膦磺酰胺配体(Sc, Rs)-PC4为催化剂,甲苯为溶剂,在40℃条件下反应48小时,能以91%的收率和92%的对映选择性得到产物5a。5a的结构和绝对构型通过X单晶衍射确定。同时,在最优反应条件下,作者考察了该反应的底物范围。各种芳环取代的苯并三唑以及萘并三氮唑具有良好的耐受性,能以良好至优秀的收率和对映选择性得到相应产物。改变N-烯丙胺上N的取代基以及将苯基换成对甲氧基和苄基,这些反应均能较好的适应反应条件,能以优秀的收率和对映选择性得到相应产物。
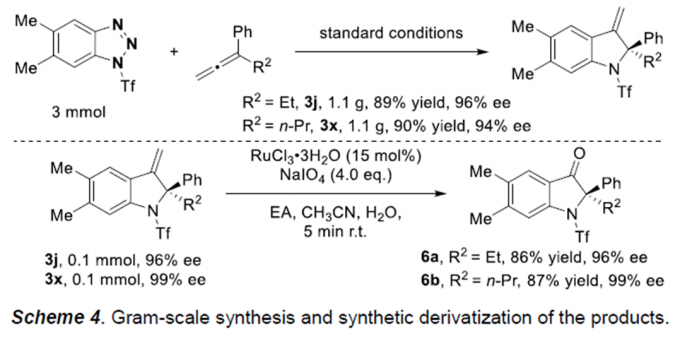
为了证明反应的应用潜力,作者进行了克级反应和衍生反应(Scheme 4)。作者分别对3j和3x进行了克级反应,该反应均能较好的进行,反应的收率和对映选择性变化不大。3j和3x在RuCl3 / NaIO4的作用下可生成相应的酮6。
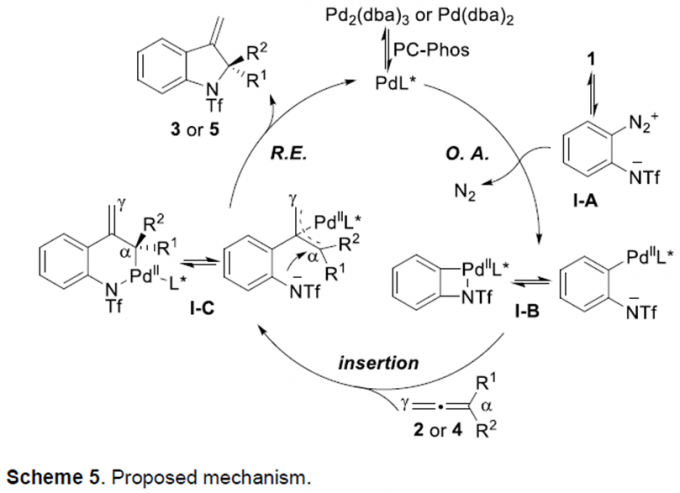
最后,作者进行了一系列的控制实验。通过控制实验的结果,作者推测可能的机理(Scheme 5):首先,苯并三唑1经历环链异构化过程生成重氮化合物I-A。然后,I-A与Pd作用,放出氮气和中间体I-B。紧接着,丙二烯或N-烯丙胺会插入到I-B的C-Pd键中生成π-烯丙基钯络合物I-C。最后,I-C发生烯丙基取代反应生成环化产物3或5,同时钯催化剂再生。
论文总结评价:
复旦大学张俊良课题组报道了Pd催化苯并三唑与丙二烯或N-烯丙胺的不对称脱氮环化反应,能以优秀的收率和对映选择性得到一系列具有光学活性的3-甲基-2-亚甲基吲哚啉。该策略具有操作简单、反应条件温和、不需要加碱以及合成效率高等有点,这为不对称3-甲基-2-亚甲基吲哚啉的合成提供了一种新的简便的方法。
参考文献:
- Nakamura, I.; Nemoto, T.; Shiraiwa, N.; Terada, M. Org. Lett. 2009, 11, 1055. DOI: 10.1021/ol900113f
- Teders, M.; Pitzer, L.; Buss, S.; Glorius, F. ACS Catal. 2017, 7, 4053. DOI: 1021/acscatal.7b01025
- Wang, Y.; Wang, Z.; Chen, X.; Tang, Y. Org. Chem. Front. 2018, 5, 2815. DOI: 10.1039/C8QO00778K
- Wang, Y. H.; Li, Y. H.; Fan, Y. J.; Wang, Z. G.; Tang, Y. Chem. Commun. 2017, 53, 11873. DOI: 10.1039/C7CC07543J
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!





















No comments yet.