烯丙基醇的不对称重排反应
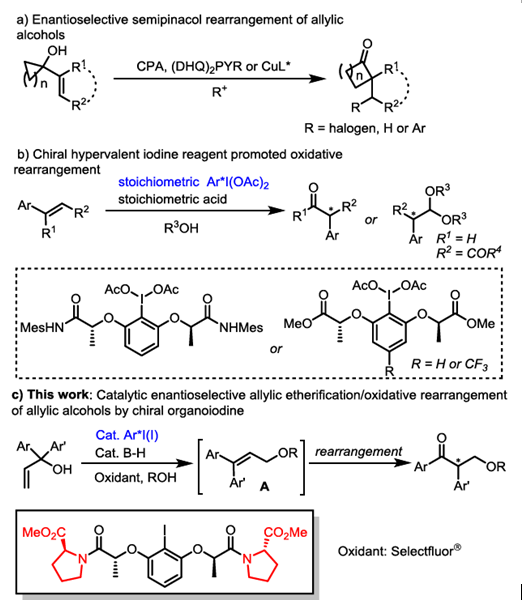
α-取代酮化合物广泛存在于天然产物和具有生物活性的化合物中,而烯丙基醇的不对称重排反应被认为是合成α-取代酮化合物最有效的合成方法之一。在过去的这几十年中,烯丙基醇的不对称重排反应已经取得了不错的进展,而该反应所用的催化剂主要局限于手性磷酸催化剂和二奎宁衍生的催化剂这两种催化剂(Scheme 1a)。[1]到目前为止,还没有关于有机碘催化烯丙基醇的不对称重排反应的报道。同时,关于有机碘催化的不对称重排反应的报道也很少。最近,Wirth课题组依次成功报道了手性高价碘催化剂催化查尔酮[2]和1,1-二取代烯烃[3]的不对称氧化重排,但为了保证反应的顺利进行必须要加入化学当量的手性碘催化剂(Scheme 1b)。
Scheme 1.烯丙基醇的不对称重排反应
基于这些背景研究,中国科学技术大学龚流柱团队报道了第一例(S)-脯氨酸衍生C2-对称手性碘催化剂催化烯丙醇的不对称烯丙基烷氧化/氧化重排反应(Scheme 1c)。相关研究成果发表于
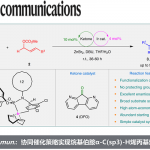
Organoiodine-Catalyzed Enantioselective Tandem Alkoxylation/Oxidative Rearrangement of Allylic Alcohols
Zhang D. Y.; Zhang Y.; Wu H.; Gong L. Z.*
Angew. Chem. Int. Ed.2019,early viewDOI: 10.1002/anie.201902903
论文作者介绍
研究者:龚流柱教授
研究者经历
1989.09-1993.07 河南师范大学化学系,化学教育专业,理学学士;
1993.09-1996.07 中国科学院成都有机化学研究所,有机合成,理学硕士;
1996.09-1998.06 中国科学院化学研究所,有机合成, 博士生;
1998.06-2000.06 美国弗吉尼亚大学化学系,访问学者(联合培养博士生)
2000.08-2000.11 中国科学院成都有机化学研究所,助理研究员;
2000.12-2001.11 中国科学院成都有机化学研究所,副研究员;
2001.12-2005.12 中国科学院成都有机化学研究所,研究员,博士生导师,不对称合成和手性技术四川省重点实验室常务副主任,主任;
2003.10-2004.09 德国慕尼黑大学有机化学研究所, 洪堡学者,访问教授;
2006.01-至今 中国科学技术大学化学系,合肥微尺度物质科学国家实验室(筹),教授。
研究内容; 有机合成方法学,不对称催化和天然产物合成。
论文概要
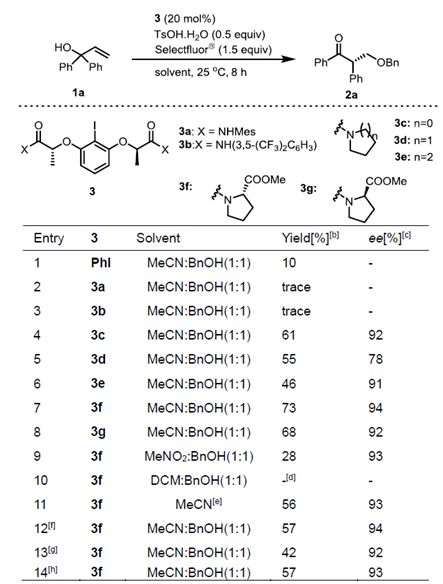
以1,1-二苯基丙-2-烯-1-醇1a作为模板底物优化条件后,作者最终选用的最优条件为:20 mol%的手性碘3f作为最优催化剂,0.5 equiv TsOH·H2O作为Brønsted酸,1.5 equiv Selectfluor®作为氧化剂,MeCN:BnOH = 1:1为最优溶剂,在25 ℃条件下反应8 h,能以73%的收率和94%的对映选择性得到目标产物。
Table 1. 烯丙基醇不对称重排反应的条件优化
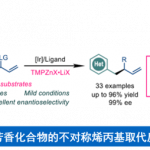
在最优反应条件下,作者考察了醇和烯丙基醇的底物范围。伯醇、叔醇、2,2,2-三氟乙-1-醇以及各种取代的苄醇均能很好地适应反应条件,能以良好的收率和较高的对映选择性得到相应的产物。值得高兴的是,对位或间位取代的苯基烯丙基醇也能很好的适应反应条件,能以良好的收率和优异的对映选择性得到相应的产物。对于两个芳基上具有不同取代基的烯丙醇,则只能以良好的收率、适当的区域选择性和较高的对映选择性得到相应产物。
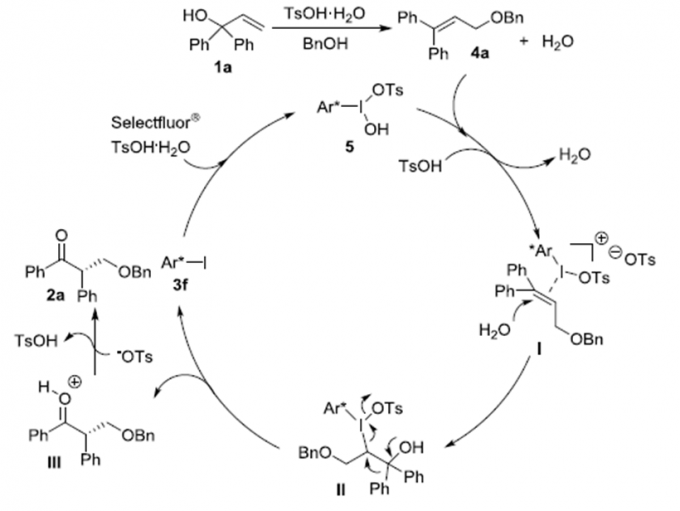
紧接着,作者进行了一系列控制实验。根据控制实验的结果,作者推测可能的机理:烯丙醇1a与苄醇发生烷氧化反应生成4a。同时,Selectfluor®氧化剂氧化催化剂3f得到活化的手性有机碘(III) 5。然后,5、二苯基烯烃4a以及TsOH三者反应生成碘(III)-底物复合物I。紧接着,水分子选择性进攻I的碳-碳双键生成中间体II,随后,II发生semipinacol-型重排反应得到中间体III,同时手性有机碘3f再生。最后,III发生去质子化作用得到产物2a。
Scheme 2. 反应机理解析
小结
中国科学技术大学龚流柱团队报道了第一例(S)-脯氨酸衍生C2-对称手性碘催化剂催化烯丙醇的不对称烯丙基烷氧化/氧化重排反应。该报道极大地丰富了不对称烯丙醇重排反应的催化策略,但底物范围和对映选择性还有待提高。
参考文献
- (a) Zhang Q.W.; Fan C. A.; Zhang H.J.;Tu Y.Q.; Zhao Y.M.;Gu P.; Chen Z.M. Chem. Int. Ed.2009, 48, 8572.DOI:10.1002/anie.200904565(b) Zhang E.; Fan C.A.;Tu Y.Q.; Zhang F.M.; Song Y.L. J. Am. Chem. Soc. 2009, 131,14626.DOI:10.1021/ja906291n
- Farid U.;Malmedy F.;Claveau R.; Albers L.; Wirth T.; Chem. Int.Ed.2013, 52, 7018.DOI:10.1002/anie.201302358
- Brown M.; Kumar R.;Rehbein J.; Wirth T.; Eur. J.2016, 22,4030.DOI: 10.1002/anie.201302358
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!




















No comments yet.