本文作者:芃洋雪
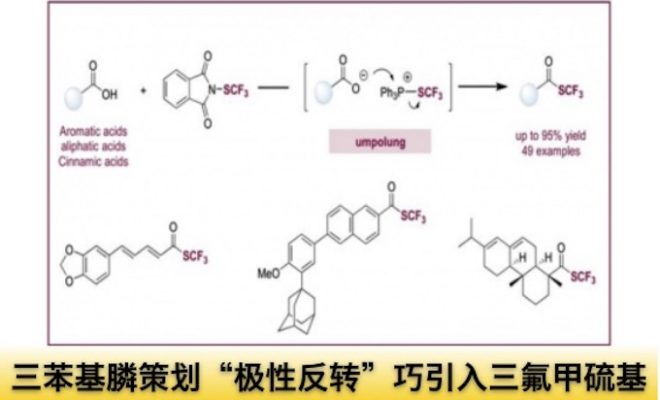
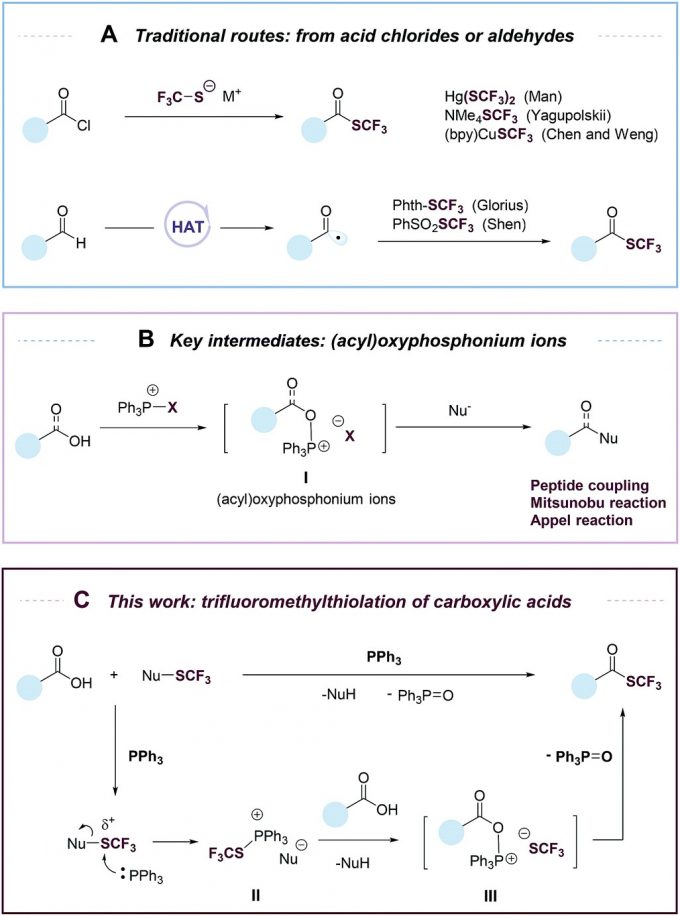
众所周知,含氟化合物在医药和材料领域有广泛应用。其中三氟甲硫基SCF3因高亲脂性和吸电子性质引起了研发人员的兴趣。目前虽然有直接向C-H和C-X中引入三氟甲硫基的方法,例如酰氯和Hg(SCF3)2、 NMe4SCF3 、(bpy)CuSCF3等试剂反应引入三氟甲硫基,但这些试剂都有毒性,反应还生成金属副产物,应用受限;也有报道醛通过氢原子转移hydrogen atom transfer (HAT) 转化为三氟甲硫基,底物醛一般不稳定,并且不易获得,如图1A所示。相比之下,羧酸的来源广泛,稳定而且无毒,羧酸的脱氧三氟甲硫化不失为高效的合成策略。
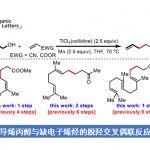
图1.(A)已报道的从酰氯或醛引入三氟甲硫基. (B)关键中间体(酰基)氧膦鎓离子.(C)本文工作:羧酸的脱氧三氟甲硫化反应. 图片来源:Chem. Sci.
最近来自洛桑联邦理工学院école Polytechnique Fédérale de Lausanne (EPFL)的 Xile Hu等实现了这个想法,相关论文:
Deoxygenative trifluoromethylthiolation of carboxylic acids
Runze Mao, Srikrishna Bera, Alexis Cheseaux and Xile Hu
Chem. Sci., 2019, DOI:10.1039/C9SC03396C.
Prof. Xile Hu(胡喜乐). 课题组主页:https://www.epfl.ch/labs/lsci/hu/
作者要实现这个反应并不容易,首先遇到的问题就是在羧酸中,CF3S–会失去 F–形成二氟硫化碳,再和羧酸反应形成酰氟。作者受到膦试剂和(酰基)氧膦鎓离子在多肽偶联、光延反应等的启发,这类中间体有可能在温和的条件下从羧酸转化为三氟甲硫基。因此,作者采用了极性反转策略umpolung,使用亲电性的三氟甲硫试剂,避免CF3S–分解,如图1B所示。
极性反转是这样实现的:三苯基膦捕获CF3S+阳离子,形成 SCF3–磷盐(Ⅱ),接着和羰基发生复分解反应形成氧膦鎓离子中间体(Ⅲ),脱氧,消除三苯氧膦PPh3=O,如图1C所示。
反应条件的优化
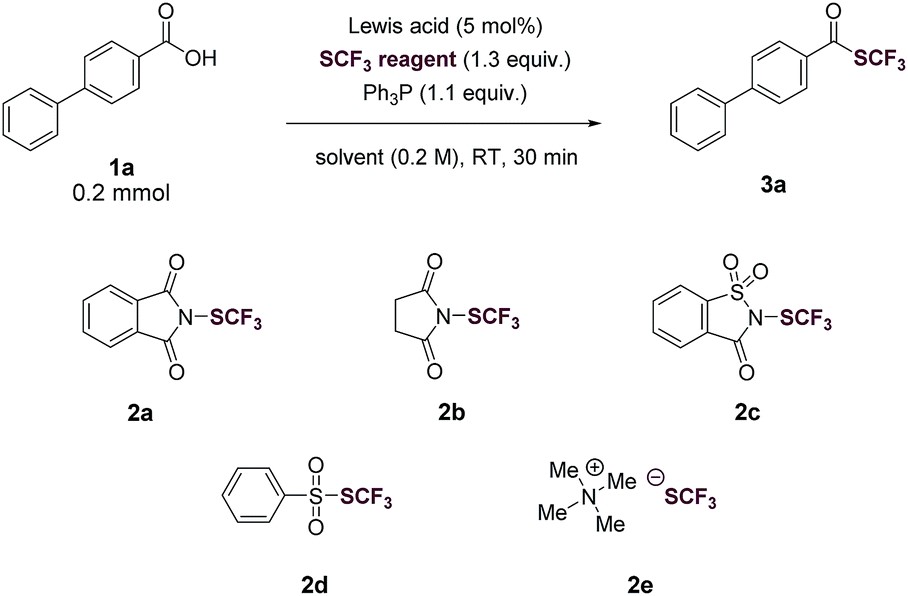
作者以底物4-苯基苯甲酸(1a) 和N-邻苯二甲酰三氟甲硫(2a)生成对应的三氟甲硫化产物(3a)为模版,初始条件为在1.1当量的PPh3在THF中(0.2M)反应,进行反应条件优化,工艺优化中对众多反应参数摸索,结果如表1所示:
表1 反应参数和条件的影响
研究发现,THF是最优溶剂,少量路易斯酸能促进反应(表1,entry2-6),邻苯二甲酰基和路易斯酸结合,可能极化N-(trifluoromethylthio)phthalimide (2a) N-邻苯二甲酰三氟甲硫,使亲核试剂易于进攻,从而生成关键中间体SCF3-膦盐(II),无水FeCl3表现最好,收率高达95%(表1,entry 2)。三氟甲硫化试剂中,2a优于其他亲电试剂2b-2d(表1,entry7-9)。使用亲核试剂NMe4SCF3(2e)时,居然没有产物生成。加入额外的碱,收率下降(表1,entry11-12),还有PPh3是最好的调节剂(表1,entry 2和13)。这个合成方法还有个突出特点,反应时间短,室温下仅需要30min就能反应完全。
底物范围
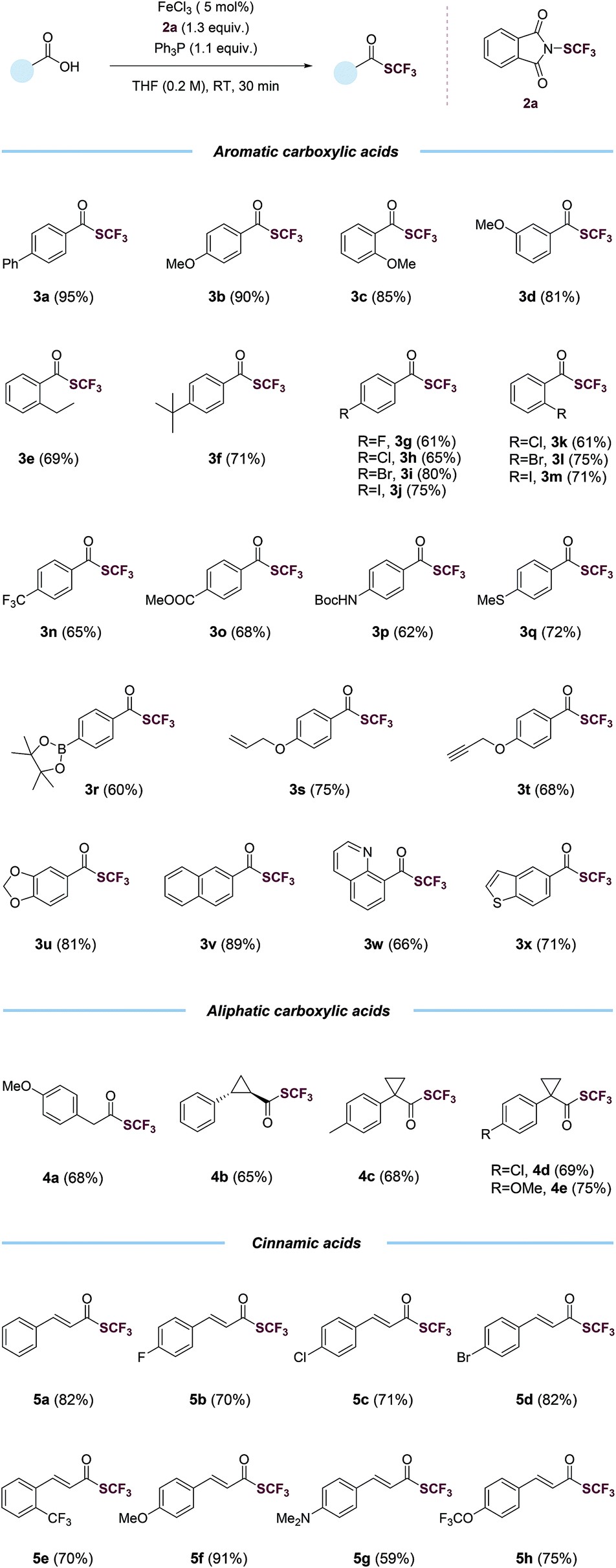
在手握最优条件后,作用研究了反应底物的范围,实验发现芳基卤化物,包括活泼的碘代物(3j, 3m)、三氟甲基(3n)、酯(3o)、(叔丁基羰基)氨基(3p、硫甲基(3q))硼酸酯(3r)、烯烃(3s)、炔烃(3t)、1,3-苯并间二氧杂环戊烯(3u)和萘(3v)等官能团都可以兼容,收率都较高。杂环羧酸都能顺利得到产物(3w-3x),值得关注的是脂肪族(4a-4e)也适合这个反应条件。此外还有多种电子效应的肉桂酸系列,不论是电中性(5a),吸电子基团(5b-5e,5h),供电子基团(5f-5g),都有较好的收率,反应底物结构和收率如表2所示。
表2 羧酸的底物范围
羧酸是存在最广泛的官能团之一,作为反应底物,适用于天然产物和药物的后期修饰。如芳基羧酸阿达帕林Adapalene(6a)、丙磺舒probenecid (6b)、 羊毛甾醇lanosterol (6c)、L-薄荷醇衍生物(6d)、胡椒酸piperic acid (6e)、咖啡酸异构体caffeic acid isomer (6f)。脂肪族的扎托洛芬 zaltoprofen (6g)、布洛芬ibuprofen (6h)、酮洛芬ketoprofen (6i)、奈普生naproxen (6j)、吉非罗齐gemfibrozil (6k)和松香酸abietic acid (6l)等。尽管这些底物含有多种官能团,并且结构复杂,但都有不错的收率,如表3所示。
表3 含羧酸官能团的天然产物或药物的后期修饰
拓展反应应用
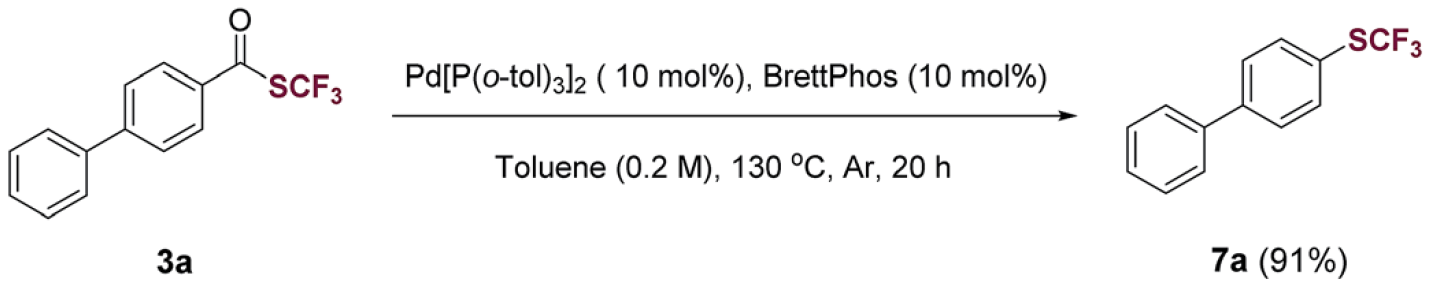
在Pd催化的脱羰基反应中,三氟甲基硫代酯可转化为更常见的三氟甲硫醚,如底物3a转化为7a,收率高达91%,从而拓展了反应范围,如图2所示。
图2. Pd催化的三氟甲基硫代酯(3a)转化为对应的三氟甲硫醚(7a). 图片来源:Chem. Sci.
反应机理
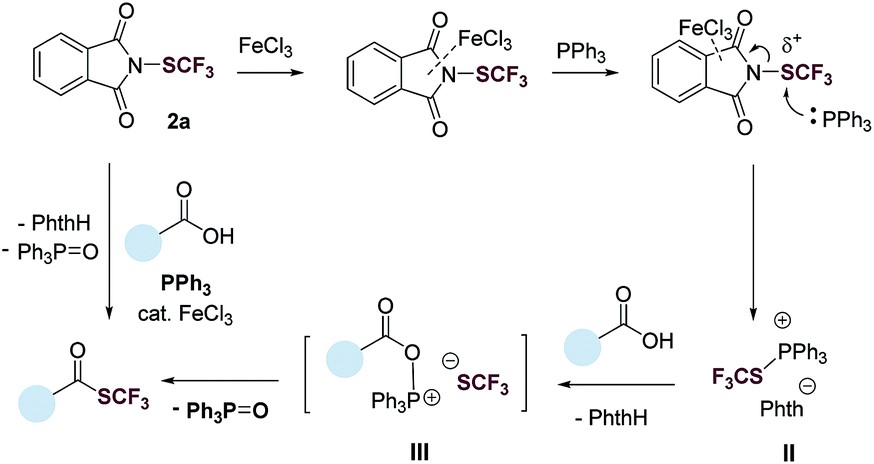
通过对照实验、31P NMR和文献报道,作者推测了反应机理。首先N-(三氟甲硫基)邻苯二甲酰亚胺(2a) 的邻苯二甲酰基团与 FeCl3配位,增加了SCF3的亲电性,促进了PPh3的亲和进攻,生成三氟甲基硫磷鎓离子Ⅱ,再与羧酸反应生成酰氧磷鎓离子中间体Ⅲ,随后CF3S–分子内进攻羰基碳,生成硫酯产物和三苯基氧化膦Ph3PO副产物,如图3所示。
图3. 可能的反应途径. 图片来源:Chem. Sci.
总结
作者通过使用三苯基膦这个斡旋者,使亲电试剂极性反转,将羧酸转化为三氟甲硫酯,开发了引入三氟甲硫基的新方法,具有反应速度快,应用范围广的特点,适合于天然产物和药物的后期修饰。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!





















No comments yet.