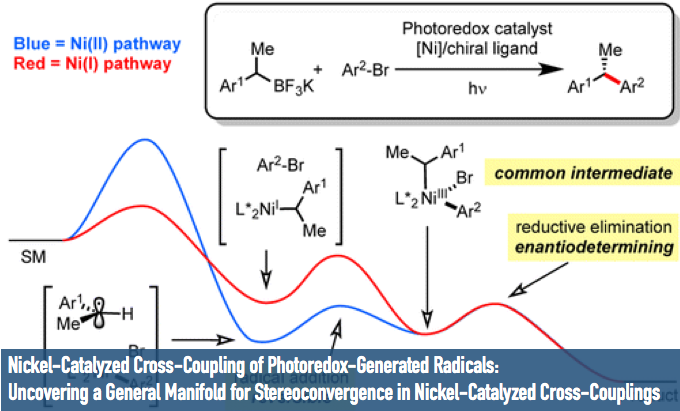
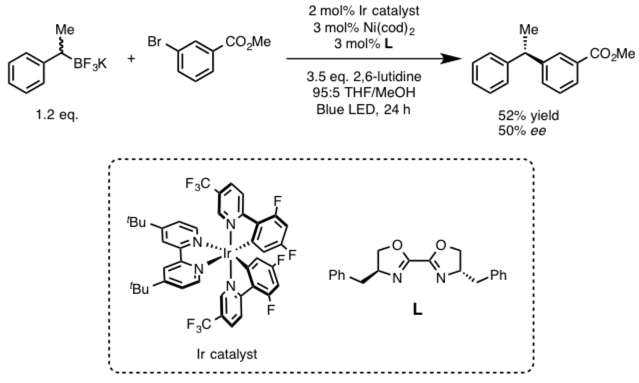
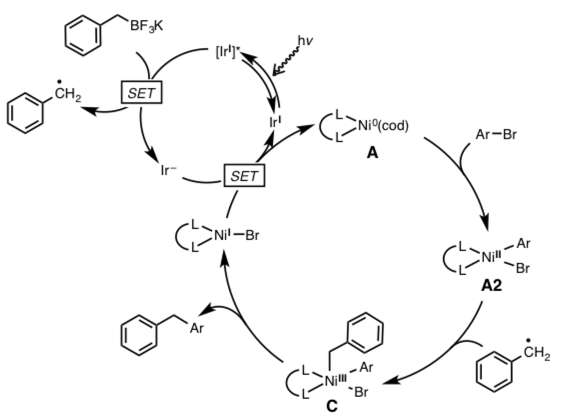
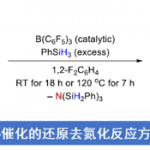
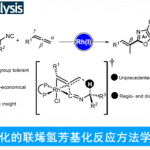
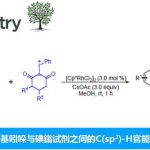
近年,过渡金属催化的sp3碳的偶联反应已经成为化学界追逐的热点课题,同时也得到了飞速的发展[1, 2]。例如,宾夕法尼亚大学的Molander等人,在2014年利用Ni/photoredox催化剂实现了卤代芳烃与烷基三氟化硼盐的手性偶联反应(图1) [3]。在这个反应中,Ir photoredox与烷基三氟化硼盐首先反应生成烷基自由基中间体,推动了整个反应的进行。但是,当时关于这个反应的详细机理还并不是特别明朗。最近,同是宾大的Kozlowski与原作者Molander合作,利用量子化学计算的方法,对该反应的机理进行了一系列的解析研究,以下这篇论文被近期发表在JACS上,接下来就让我们具体看一下这篇论文的经纬。
“Nickel-Catalyzed Cross-Coupling of Photoredox-Generated Radicals: Uncovering a General Manifold for Stereoconvergence in Nickel-Catalyzed Cross-Couplings”
Gutierrez, O.; Tellis, J. C.; Primer, D. N.; Molander, G. A.; Kozlowski, M. C. J. Am. Chem. Soc.2015, 4896. DOI: 10.1021/ja513079r
图1: Stereoselective cross-coupling of C(sp3) using Ni catalyst
MOLANDER等人假想的反应机理
在2014年报道的那篇文章中,作者提出了下图中的一个假想的反应机理。反应以Ni(0)→Ni(II)→Ni(III)的催化循环进行,而在其中自由基加成那一步(A2→C),产生并决定了立体选择性(图2)。
图2: Mechanism of stereoselective cross-coupling using Ni/photoredox catalyst reported by Molander
而这一次的论文中,通过DFT计算模拟最优化结构(UB3LYP/6-31G(d)与LANL2DZ),并且把溶剂的影响(SMD)也一并算入进行各种反应中间体的能量计算(M06/6-311+G(d,p))。如果不是专业搞计算化学方面这些研究的,还是很难懂的,所以接下来我们简要介绍一下论文中使用的量子化学计算方法及其一些基本知识。
量子化学计算的选定手法
这次文中用到化学计算方法是把结构的最优化模拟计算以及其能量计算分开进行的,相对于结构最优化的计算来说,一些结构能量的计算要求更高,更严格。
当然计算手法越严格,越容易预测出与实验数值相近的结果,但是另一方面,所花费的金钱跟时间相对来说也是巨大的,所以根据具体情况选择最合适的计算手法是很有必要的。
特别是在能量计算的时候,较低水准的计算手法往往得到的结果跟实验值差距特别大,数据的可信度也远远不尽人意[4]。正因为如此,所以往往能量的计算相对于结构最优化的计算来说要求更高,通常使用更严格的计算手法,比如MP2, MP4, CCSD等。这次的文章中实用的M06属于DFT计算的一种,但是可信度确是接近于MP2的高水准的计算方法,用它预测的能量值得十分可信的[5]。另外为了提高泛函数微分的水平,基底函数从6-31G(d)调整提高到6-311+G(d)。
实验论文中使用的计算手法
UB3LYP/6-31+G(d,p)
- B3LYP: DFT法中最常用的泛函。引入了电子相关的效果。
- U: 在能生成自由基的体系中,为了能够导入自旋不受限的功能而被使用
- +: 通过引入分散函数,可以估算出正负离子的局部化后大分子的电荷密度。
- (d), *: 引入重原子偏振函数,用于表示d轨道的分极情况。
- (d, p), **: 在(d)的基础上,再导入H与He偏振函数的基底函数。特别适用于第三周期含d轨道的分子的再现性研究。
- IRC: 从过渡状态的中间态结构来自动预测出反应底物与反应生成物。
- SMD, PCM: 加入溶剂效应的影响。
新的反应机理的发现
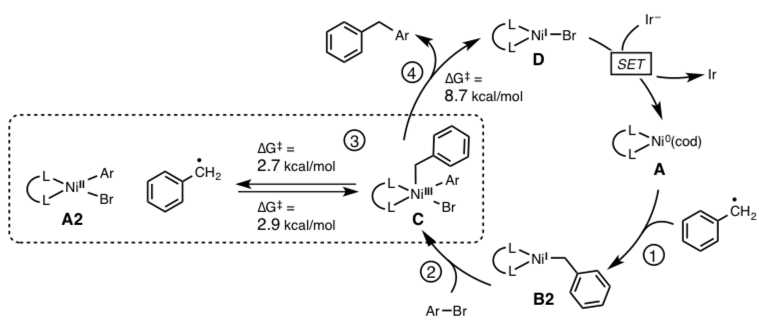
再回到最初的话题,通过计算结果作者发现,最初假定的反应机理(图1)并不正确,文中的反应其实是遵循下图(图3)所示的新的反应机理进行的。
图3 Possible alternative pathway indicated by computation.
每个阶段的活化能如下。
- 烷基自由基与Ni(0)的加成反应: A→B2 / [4.8 kcal/mol]
- Ni(I)与芳基溴化物的氧化加成: B2→C / [18.2 kcal/mol], 限速步骤(rate determination)
- Ni(III)络合物与[Ni(II)络合物+烷基自由基活性种]的平衡: C→A2 / [2.7 kcal/mol], A2→C / [2.9 kcal/mol]
- 还原消除: C→D / [8.7 kcal/mol]
通过计算可以发现,相比于氧化加成后生成的Ni(III)络合物C的还原消除所需活化能(8.7 kcal/mol),从Ni(III)络合物C通过平衡反应解离成A2与烷基自由基所需的活化能(2.7 kcal/mol)更低。这一个结果说明,相比于还原消除来说[Ni(II)络合物+烷基自由基活性种]与Ni(III)络合物C在反应体系中是同时存在的。
反应的立体选择性是在哪步实现的?
根据计算化学阐明的反应机理来看,作者表达了立体选择性是在还原消除的阶段产生的的设想。
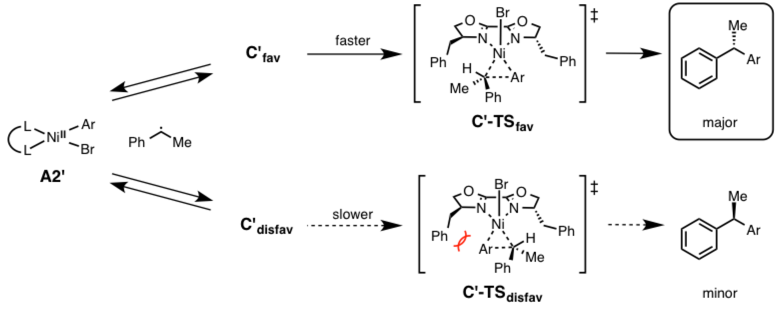
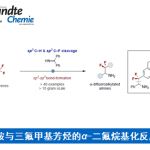
作者为了验证这个设想,作者引入手性配体与1-苯基乙三氟化硼对Ni(III)络合物与Ni(II)络合物+烷基自由基活性种的平衡反应以及Ni(III)络合物的还原消除阶段进行实验考察。结果显示:在A2′、C’fav/A2′、C’disfav之间存在平衡状态,经C’fav或者C’disfav形成的各自的过渡态C’fav -TS或者C’disfav-TS最终形成目标产物,由于C’fav -TS的活化能更小,所以反应更倾向于通过这个过渡态形成对应的寿星产物(下图major产物)。通过这个反应,立体选择性就可以自然通过Ni(III)錯体C, C’的速度论光学分割来进行说明了。(图4)
图4. Explanation of stereoselectivity caused by Dynamic Kinetic Resolution
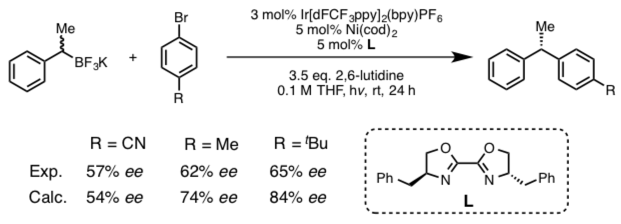
接着作者又尝试了各种底物,并且对决定立体选择性的过渡态(还原消除那步的过渡态C-TS)进行了计算。得到的结果是,在对位引入高位阻的取代基的话,可以提高立体选择性。通过这个计算结果,进行了实际的实验验证,并且得到了与计算相同的选择性倾向(图5)。
图5. Predicted and experimental reaction enantioselectivities.
这回的论文中,首次详细的解明了Ni/photoredox催化的sp3C的偶联反应机理以及其立体选择性的发现机理。计算化学脱离了实验支持往往显得并不可信,而实验结果少了计算化学的解析也往往抓不到最深处的机理。这篇文章把实验跟计算结合在一起,双剑合璧,十分有价值也很有意义。
关联论文
- Zhou, J. S.; Fu, G. C. J. Am. Chem. Soc. 2003, 125, 14726. DOI: 10.1021/ja0389366
- Jana, R; Pathak, T. P.; Sigman, M. S. Chem. Rev. 2011, 111, 1417. DOI: 10.1021/cr100327p
- Tellis, J. C.; Primer, D. N.; Molander, G. A. Science 2014, 345, 433. DOI: 10.1126/science.1253647
- Saito, B.; Fu, G. C. J. Am. Chem. Soc. 2008, 130, 6694. DOI: 10.1021/ja8013677
- Droogenbroeck, J. V.; Tersago, K.; Alsenoy, C. V.; Blockhuys, F. Chem. Phys. Lett. 2004, 399, 516. DOI; 10.1016/j.cplett.2004.10.065
- Bryantsev, V. S.; Diallo, M. S.; van Duin, A. C. T.; Goddard III, W. A. Chem. Theory Comput. 2009, 5, 1016.
外部链接
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载