本文来自Chem-Station日文版 分子の磁石 “化学コンパス” ~渡り鳥の磁場観測メカニズム解明にむけて~ ちおふぇん
翻译投稿 炸鸡 校对 肥猫
候鸟等许多动物能够准确掌握方向不迷路的重要手段之一是感知“地球磁场”。
虽然候鸟等生物能够感知“地球磁场”背后的生物物理机制尚未完全明了,但随着动物学家,化学家和物理学家多年来的积极研究,背后的生物物理学机制正逐渐一点点变得清晰。这次笔者想聊一聊一项用模型分子来解释生物体内复杂的磁场感知现象的研究。
鸟类感知磁场原理的假说
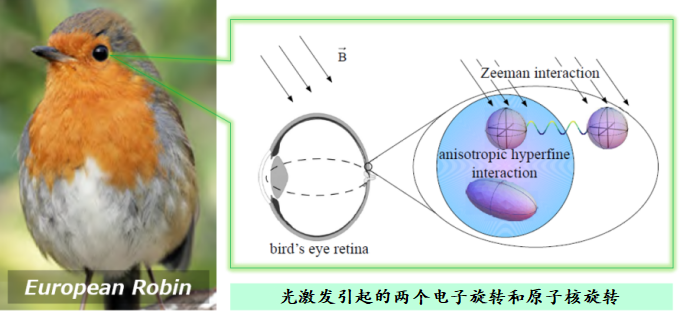
关于鸟类是如何感知磁场有许多假说。一个假说提出这与黄素腺嘌呤二核苷酸(FAD)有关,黄素腺嘌呤二核苷酸是一种存在于视网膜中的蓝色光受体隐色素蛋白[1,2]。在这之后,Schulten,K.等人在1978年提出了基于光电子转移反应产生的磁敏感自由基的假说,即所谓的自由基对机制(Radical Pair Mechanism; RPM)[3] ,该假说在动物磁场感知机制领域受到了极大的关注。
Fig. 1. RPM假说中鸟眼中磁场感应模式图。(出处:[4]部分改编详见此处)
除了“RMP”假说外,还有一个“磁石”假说,该假说主张动物体内存在有极小的磁石粒子充当磁针来帮助动物感知磁场[5],现在“RMP”假说和“磁石”假说都被承认是解释动物为什么能感知磁场的两个具有说服力的假说。
验证自由基对机制
与RPM相关的蛋白质是FAD受蓝光激发产生的空间分离的FAD与反自由基组成的蛋白质。[6] 要想验证RPM现象,就要在用光谱技术观测在与地球同样弱的磁场 (ca. 30-65 μT) 下的反应,但是因为试管中分离的完整蛋白质所处的磁场的强度大约是地球磁场强度的20倍,所以有关低磁场强度的实验证据几乎没有。
除了在试管中难以创造与地球磁场强度相同的磁场,还有两个主要的问题困扰着验证RPM现象:生成的自由基对寿命十分短和自由基之间距离太短。两个问题都会让证明(低)磁场敏感的自由基的存在十分地困难。
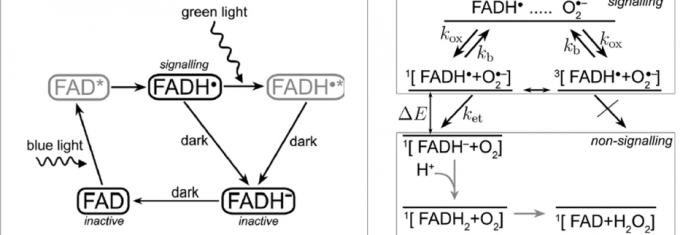
Fig. 2. FAD的光激发循环和分子状氧自由基的设想反应方案的概略图。(出处:[7])
因此,为了能证明光化学反应是候鸟能感应磁场的基础原理,最近一些研究开始采用模型分子来验证自由基对机制。
CPF分子的特征和优势
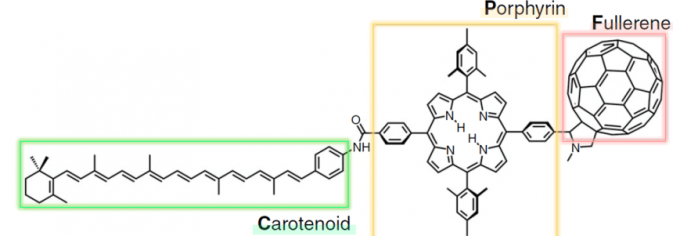
因为类胡萝卜素-卟啉-富勒烯分子(CPF)易于处理,光诱导的自由基寿命相对较长且对弱磁场(几乎和地球磁场一样弱)敏感,所以被选为模型分子。[1,8,9]
Fig. 3. 类胡萝卜素―卟啉―富勒烯模型系的分子(CPF)。(出处:[8]部分改编)
那么,让我们来看看这个CPF分子有什么特别之处。
供体和受体在溶液中自由扩散的自由基对系统或是分子内的自由基相互间通过柔性链结合在一起使得自由基可以大范围内运动这样的自由基对模式,这两者都可以使观测磁场效果更容易。CPF分子是一种模型分子,其特征在于利用多级电子转移,即通过光激发产生的初级供体通过分子中的供体-受体物种转移到最终受体,从而快速生成自由基对。[10,11]不仅如此,CPF分子的合成非常简单且易于溶于有机溶剂,具有优异的可操作性。
接下来,让我们走进CPF的自由基引发过程。
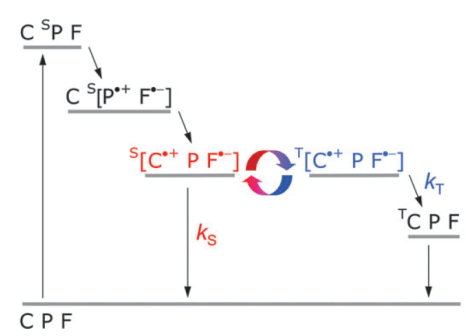
如下图所示,CPF首先在532 nm的光照射下被激发至CSPF状态,之后分子内电子迅速移动,首先产生寿命仅为皮秒的主自由基对CS[P•+F•-]。电子继续移动形成了第二个自由基对S[C•+PF•-],其寿命约为1微秒。第二个自由基对S[C•+PF•-]主要以单重态的形式存在,但因温度和溶剂等环境因素,会有少量的三重态自由基对出现。在这种情况下,磁场的存在会影响单重态和三重态之间的相互转换从而改变自由基对重组的比例。[9]
Fig. 4. CPF分子的能量图解和电子自旋状态。(出处:[9])
化学罗盘是怎么工作的
光化学形成的自由基对寿命会受磁场的变化而发生改变,这就是磁感应器,即化学罗盘,拥有各向异性的行为的背后缘由。正如文章一开头说过很多验证实验都是在比地球磁场强数个数量级的强磁场内进行的,关于弱磁场灵敏度的研究报告还很少。
Kerpal,C.等人以CPF为模型分子研究了化学罗盘在相对较弱的磁场条件(50-200μT)下的响应性,并于2019年在Nature communications上刊登了论文,首次证实了具有磁响应性的自由基对在与地球磁场强度相等的低磁场也能发挥作用[8]。
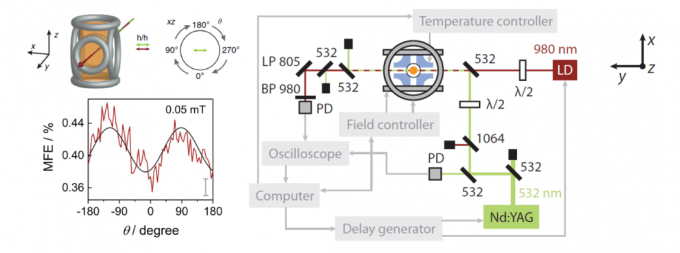
Fig. 5. 实验装置的概略图和磁场效果。(出处:[8]部分改编)
弱磁场主要提高S-T0互变效率,而强磁场则通过塞曼效应影响自由基的重组,从而抑制单重-三重的混合。[8,12]
结束语
本篇内容简单介绍了鸟类的磁场感知原理和最新研究进展。最近的研究开始通过采用CPF等模型分子来解析动物拥有的复杂“化学罗盘”。面临难以解决的困难问题,用替代法转而研究一些模型分子也不失为化学研究的一个好点子。
参考文献
- Maeda, K., et al., Nature, 2008, 453, 387. DOI: 1038/nature06834
- Ahmad, M., et al., Nature, 1993, 366, 162–166. DOI: 1038/366162a0
- Schulten, K., et al., Phys. Chem., 1978,111, 1–5. DOI: 10.1524/zpch.1978.111.1.001
- Gauger, EM., et al., Rev. Lett., 2011, 106, 040503. DOI: 10.1103/PhysRevLett.106.040503
- Beason, R C., et al., Nature, 1984,309, 151–153. DOI: 1038/309151a0
- 前田光憲, 化学と教育, 2016, 64.
- K., et al., Biophys. J., 2009, 96, 4804–4813. DOI: 10.1016/j.bpj.2009.03.048
- Kerpal, C., et al., Commun., 2019,10, 1-7. DOI: 10.1038/s41467-019-11655-2
- Maeda, K., et al., Commun., 2011, 47, 6563–6565. DOI: 10.1039/c1cc11625h
- Kodis, G., et al., Phys. Org. Chem., 2004, 17, 724–734. DOI: 10.1002/poc.787
- Kuciauskas, D., et al., Am. Chem. Soc., 1998, 120, 10880-10886. DOI:10.1021/ja981848e
- Lewis, A.M., et al., Chem. Phys., 2018, 149, 034103. DOI: 10.1063/1.5038558






















No comments yet.