在地壳中的含量仅次于氧。在我们身边,也使用了许多硅化合物产品,如玻璃和半导体。如果没有硅元素的应用,就可能不会有今天如此发达的电子设备。
硅的基本物理性质
| 分类 | 半金属・半导体 |
|---|---|
| 原子序号・原子量 | 14 (28.0855) |
| 电子配置 | 3s23p2 |
| 密度 | 2330kg/m3 |
| 融点 | 1410℃ |
| 沸点 | 2355℃ |
| 硬度 | 6.5 |
| 色・形状 | 暗灰色 |
| 存在度 | 地球26万7700ppm、宇宙 1.00 x 106 |
| 克拉克数 | 25.8%(2位) |
| 发现者 | 约恩斯·雅各布·贝尔塞柳斯男爵(1823年) |
| 主要的同位素 | 28Si (92.223%), 29Si(4.685%)、30Si(3.087%) |
| 用途例 | 玻璃,沸石,磨料(碳化硅),石棉,硅胶,半导体,水泥,太阳能电池,蜡,软性隐形眼镜 |
| 前后的元素 | 铝ー硅ー磷 |
含量仅次于氧气的元素
硅在地壳中大量蓄积,而主要以石英,水晶,云母的二氧化硅(SiO2)或者硅酸盐的形式存在。

硅酸盐矿物(水晶,辉石,角闪石,云母,长石,石英等)
1823年瑞典化学家贝尔塞柳斯、通过用金属钠还原氟化硅(SiF4)首次得到了单体硅。
约恩斯·雅各布·贝尔塞柳斯男爵(Jöns Jacob Berzelius)
1779-1848年。瑞典化学家。提出了使用字母表标记新元素符号、发现了硅,硒,钍和铈,被称为近代化学之父。他的弟子中最著名的有近代有机化学大家弗里德里希·维勒
硅与有机硅
硅的英文名为silicon。而有机硅的英文名区别于硅,为silicone,名字有细微的差别,有心得童鞋可以注意下。
而硅silicon是通常应用在半导体(高纯度硅结晶)领域。有机硅silicone则是硅与碳链通过氧连接。应用在硅油,硅橡胶等材料领域。

Silicon与Silicone
二氧化硅是玻璃和硅藻土的主要成分
硅的氧化物中的一种、二氧化硅是地壳的主要构成成分,因此在地壳中大量存在。同时,作为干燥机使用的硅胶的成分也是二氧化硅。二氧化硅与氢氧化钠加热可以得到硅酸钠(Na2SiO3),然后再加水加热得到水玻璃。水玻璃可以作为胶黏剂与耐火涂料。
水玻璃再经过碳酸钠或者碳酸钾混合加热,快速冷却后就变成了玻璃。水晶灯也是二氧化硅在加压下结晶制备而成的。

二氧化硅的化学反应
同时,很久以前被称为硅藻土的藻类化石的主成分也是二氧化硅。硅藻土由于具有比较高的耐火,隔热性能,因此最近也被广泛用于房屋的墙壁。而另一个比较有名的用途是,用在炸药中。诺贝尔在硝酸甘油中加入硅藻土以用来提高抓主要的稳定性。而在一段时间,成为话题的具有致癌性的石棉的主成分也是二氧化硅,这并不是因为二氧化硅自身是有害的,而是由于石棉是纤维状的,据说它会刺破肺部,引起肺癌和间皮瘤。
电脑,太阳能电池中的半导体材料
硅的代表性用途是半导体材料。半导体是介于导体与绝缘体中间的物质,利用该性质,半导体被广泛用于电脑,晶体管,半导体激光器等电子设备中。而美国的「硅谷」,它指的是位于旧金山湾区的半导体和高科技公司人口密集的地区,很多企业在进行半导体及相关部件的研究。

シリコンバレー
碳化硅ー新型新干线
碳化硅(Silicon carbide, SiC)是碳(C)与硅(Si)1对1结合的共价键化合物。硬度高(仅次于金刚石,碳化硼)、而且耐久性也非常好,被用于研磨剂与耐火材料。同时在半导体应用领域也备受关注,预计可以作为功率器件材料,性能有望超过硅的极限。今后的引用领域主要集中于日本新型新干线「N700S」(2020年登场)的驱动系统。通过使用SiC,驱动系统有望提高20%轻量化度,并且也有望实现更小型化。

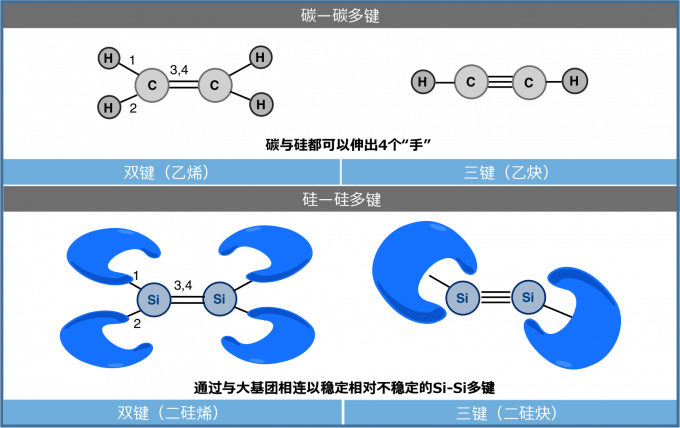
硅-硅多键化合物
碳与硅同属元素周期表的第14主族、性质虽然具有相似性,实际上差别还是很大的。在构造上差别最大的点事,多键结合体的稳定性。碳与碳之间可以很简单稳定的形成双键与三键。而硅-硅双键是天然中不存在的。
然而,1981年美国的Robert West等人首次人工合成了含有硅-硅双键的二硅烯,通过引入位阻大的取代基团进行保护,合成了普通不能稳定存在的二硅烯。
接着,直到2004年,驻波大学的関口章教授等人,成功合成了硅-硅三键化合物二硅炔。相比较于碳-碳三键的直线型结构,硅-硅三键是稍微倾斜的。这两种化合物要说具体有多大的实用性,真的很难说,但是作为基础研究还是非常值得肯定的。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!
























No comments yet.