概要
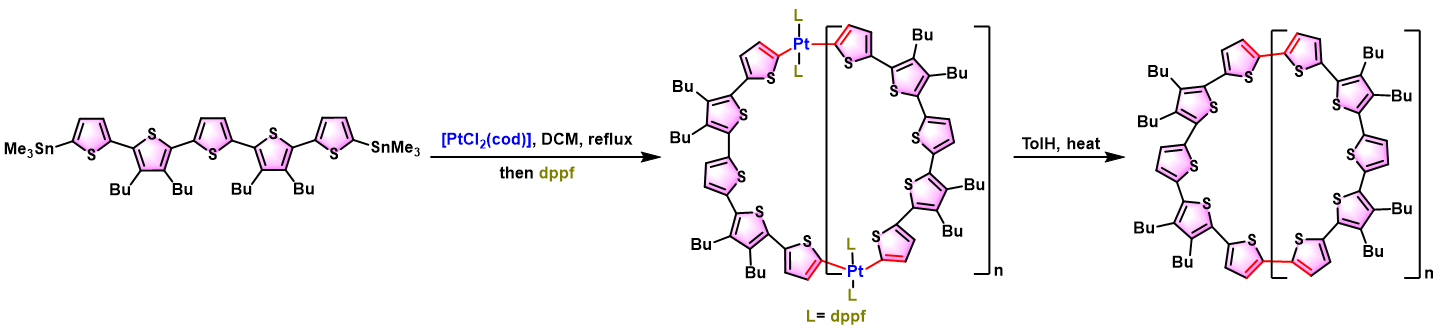
2009年,德国Ulm大学 (Universität Ulm)的P. Bäuerle首次报道了采用[PtCl2(cod)]与双锡基化五联噻吩 (bisstannylated quinquethiophene)的转金属化形成的环铂配合物的还原消除过程,成功实现了环[n]噻吩(CnT, cyclo[n]thiophenes)[1]的构建。然而,该研究组并未对环铂配合物进行完全表征,同时,P. Bäuerle也未对具有张力能的相关化合物如CPP的合成进行研究。
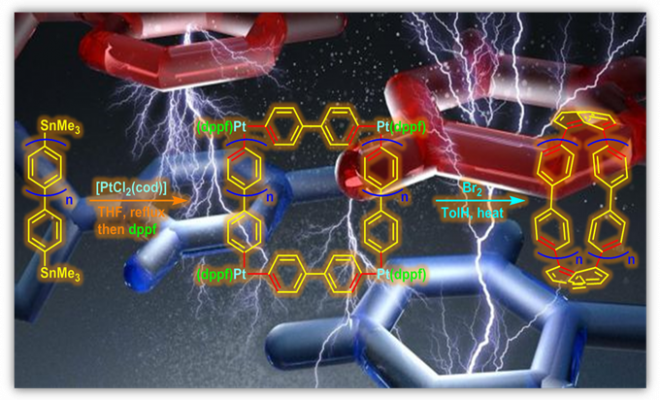
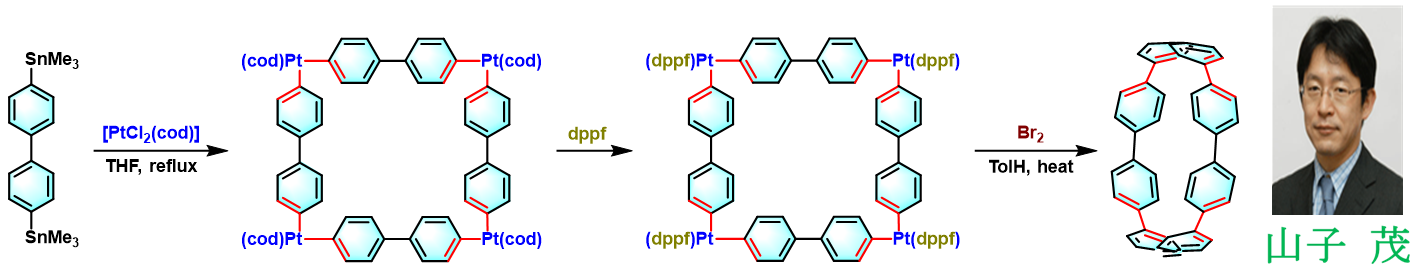
2010年日本京都大学工学研究科 (京都大学工学研究科,Institute for Chemical Research, Kyoto University)的山子茂 (山子 茂,Yamago Shigeru)研究组采用4,4ˊ-二(三甲基锡基)联苯与[PtCl2(cod)]作用,产生正方形铂配合物,随后与1,1′-二(二苯基膦)二茂铁 (dppf)配体进行配体交换后,经溴诱导的还原消除过程,成功实现最小的CPP (Cycloparaphenylene)类化合物[8]CPP的合成[2]。
之后,Yamago将该方法学应用于其它CPP分子的构筑[3],文献中现已将该方法学称为Yamago铂大环化 (Yamago Pt-macrocyclization)。Yamago铂大环化反应的所有步骤均在温和及中性的条件下进行,可以在芳环中引入多种官能团,因此适用于各类取代CPP的合成。然而,该反应的唯一缺点是产生高挥发性、恶臭及剧毒的三甲基氯化锡副产物。2011年,日本东北大学化学系 (東北大学化学研究科, Department of Chemistry, Tohoku University)的矶部宽之 (磯部 寛之,Isobe Hiroyuki)研究组采用无毒的有机硼试剂参与反应,产生正方形铂配合物,随后加入三苯基膦进行还原消除过程,成功完成了的CNT (carbon nanotube) 相应结构单元的构筑[4]-[6]。
目前,该方法学已经广泛应用于各类具有不同大小的三维环状π-共轭分子(cyclic π-conjugated molecules)的合成与CNT及SWNT (single-wall carbon nanotubes)中相应结构单元的构建[7]-[11],为三维芳香化合物的合成研究开辟了新的方法。
基本文献
- [1] F. Zhang, G. Götz, H. D. F. Winkler, C. A. Schalley, P. Bäuerle, Angew. Chem., Int. Ed. 2009, 48, 6632. doi: 10.1002/anie.200900101.
- [2] S. Yamago, Y. Watanabe, T. Iwamoto, Angew. Chem. Int. Ed. 2010, 49, 757. doi: 10.1002/anie.200905659.
- [3] T. Iwamoto, Y. Watanabe, Y. Sakamoto, T. Suzuki, S. Yamago, J. Am. Chem. Soc. 2011, 133, 8354. doi: 10.1021/ja2020668.
- [4] S. Hitosugi, W. Nakanishi, T. Yamasaki, H. Isobe, Nat. Commun. 2011, 2, 492. doi: 10.1038/ncomms1505.
- [5] S. Hitosugi, T. Yamasaki, H. Isobe, J. Am. Chem. Soc. 2012, 134, 12442. doi: 10.1021/ja305723j.
- [6] T. Matsuno, S. Kamata, S. Hitosugi, H. Isobe, Chem. Sci. 2013, 4, 3179. doi: 10.1039/C3SC50645B.
- [7] E. K ayahara, T. Iwamoto, T. Suzuki, S. Yamago, Chem. Lett. 2013, 42, 621. doi: 10.1246/cl.130188.
- [8] E. Kayahara, T. Iwamoto, H. Takaya, T. Suzuki, M. Fujitsuka, T. Majima, N. Yasuda, N.Matsuyama, S. Seki, S. Yamago, Nat. Commun. 2013, 4, 2694. doi: 10.1038/ncomms3694.
- [9] S. Yamago, E. Kayahara, T. Iwamoto, Chem. Rec. 2014, 14, 84. doi: 10.1002/tcr.201300035.
- [10] E. Kayahara, R. Qu, M. Kojima, T. Iwamoto, T. Suzuki, S. Yamago, Chem. Eur. J. 2015, 21, 18939. doi: 10.1002/chem.201504369.
- [11] E. Kayahara, Y. Cheng, S.Yamago, Chem. Lett. 2018, 47, 1108. doi: 10.1246/cl.180486.
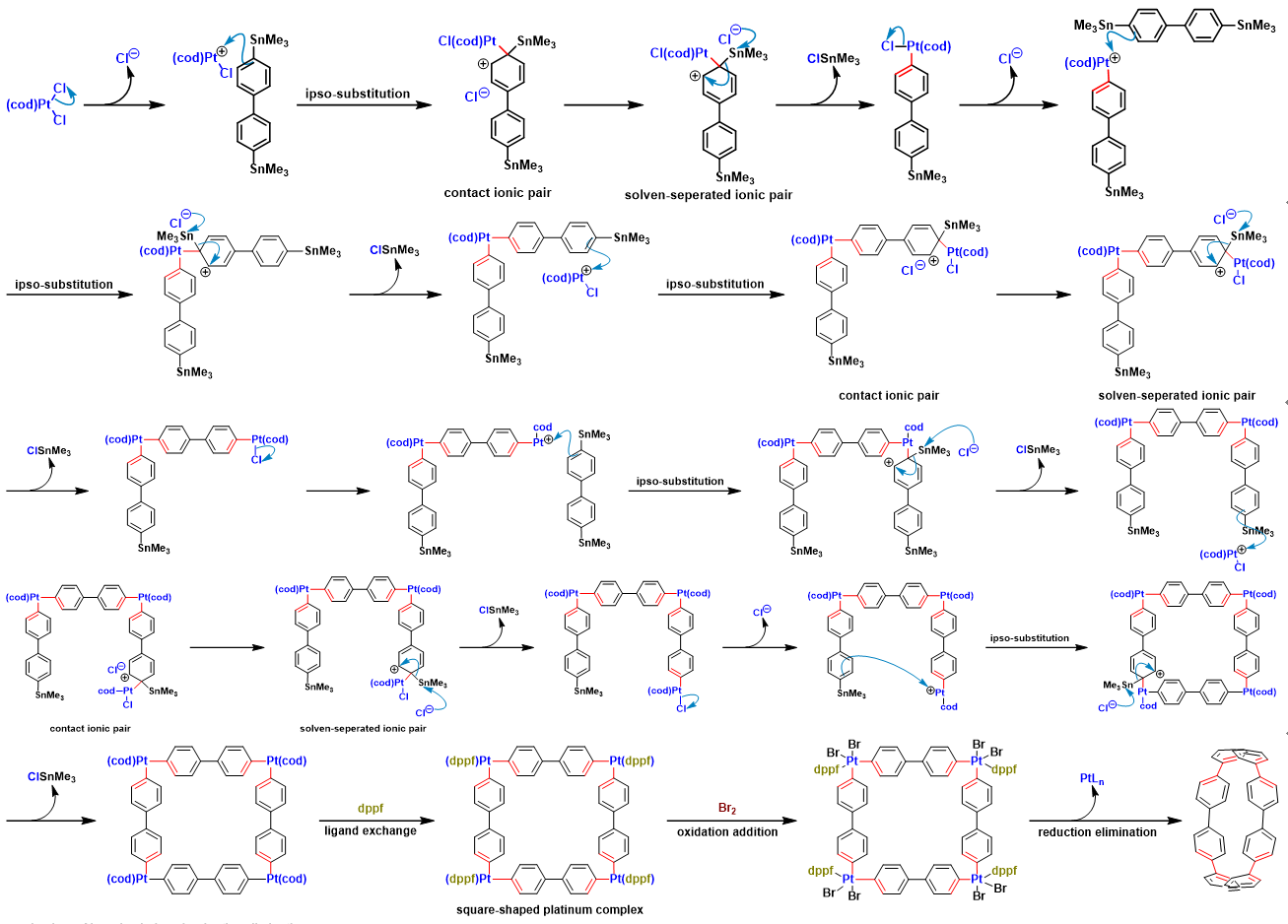
反应机理
参考文献
- [1] C. Eaborn, K. J. Odell, A. Pidcock, J. Chem. Soc. Dalton Trans. 1978, 357. doi: 10.1039/DT9780000357.
- [2] A. Yahav-Levi, I. Goldberg, A. Vigalok, J. Am. Chem. Soc. 2006, 128, 8710. doi: 10.1021/ja062166r.
- [3] K. I. Goldberg, J. Yan, E. L. Winter, J. Am. Chem. Soc. 1994, 116, 1573. doi: 10.1021/ja00083a054.
反应实例
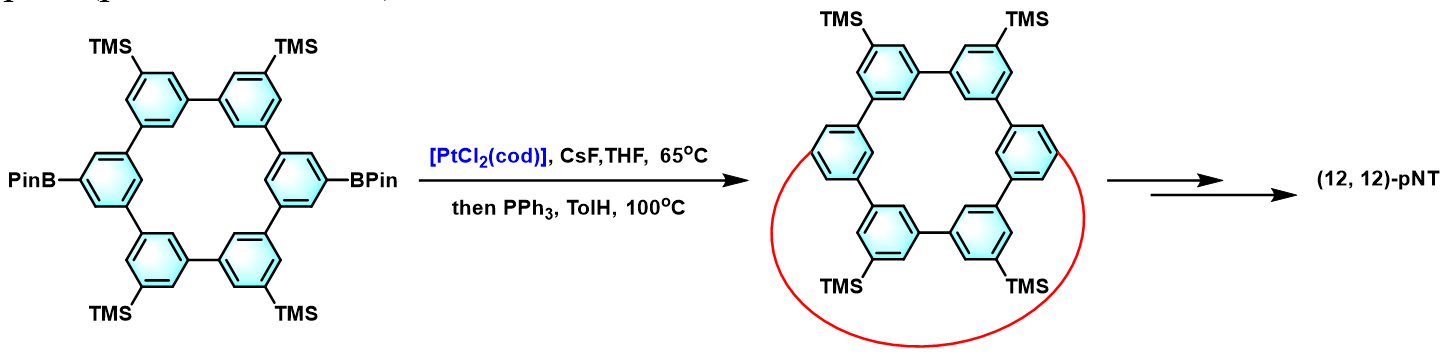
pNT (phenine nanotube)的合成[1]
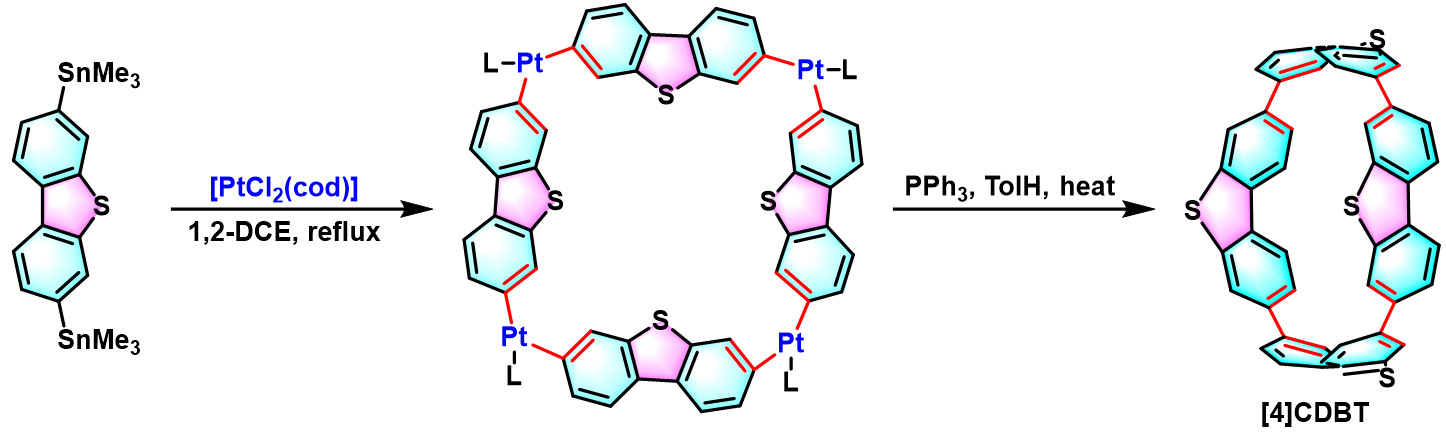
[12]CPP的合成[2] [4]CDBT ([4]cyclo3,7-dibenzo[b,d]thiophene)的合成[3]实验步骤
正方形铂配合物的合成:氮气气氛下,将 4,4′-二(三甲基锡基)联苯 (1 eq.)与[PtCl2(cod)] (1 eq.)溶解在THF (维持反应物浓度为0.004M)中,将上述混合物维持在氮气气氛下搅拌35 h。35 h后,观察到灰白色沉淀产生,随后采用过滤进行收集。将该沉淀首先采用正己烷洗涤,随后用少量DCM洗涤,获得纯净的正方形铂配合物。
与dppf的配体交换反应: 氮气气氛下,将正方形铂配合物 (1 eq.)与1,1ˊ-二(二苯基膦)二茂铁 (dppf, 4.2 eq.)的二氯甲烷悬浊液 (悬浊液浓度为1.7 M)在室温下搅拌6 h。减压除去溶剂,将残余物采用乙酸乙酯进行洗涤,获得淡橙色固体。
溴诱导的还原消除过程: 氮气气氛,并在搅拌下,将Br2 (7.3 eq.)加入至上述淡橙色固体(1 eq.)的甲苯悬浊液(悬浊液浓度为1.3 M)中。将上述反应混合物在 95oC下搅拌17 h,随后将不溶物进行过滤。减压除去滤液中的挥发性物质。将残余物依次采用制备凝胶渗透色谱(prep-GPC, preparative gel permeation Chromatography, 三氯甲烷作为洗脱剂)及硅胶柱色谱进行纯化 (三氯甲烷/正己烷洗脱剂,体积比1:4到1:1进行梯度洗脱),获得相应目标产物CCP。
实验安全须知
小编郑重提示:低级三烷基锡试剂,尤其三甲基锡试剂具有较高的挥发性与极高的神经毒性,中毒后无特效解毒剂 (通常在涉及锡试剂反应如Stille-Kosugi-Migita反应的后处理过程中需要首先除去相应的有机锡副产物,具体方法参看:D. C. Harrowven, D. P. Curran, S. L. Kostiuk, I. L. Wallis-Guy, S. Whiting, K. J. Stenning, B. Tang, E. Packard, L. Nanson, Chem. Commun. 2010, 46, 6335. doi: 10.1039/c0cc01328e. 及Chem-station分离纯化技巧系列专题:含锡副产物的除去方法:碳酸钾/硅胶),整个实验过程建议在通风效果极为优良的通风橱内仔细操作。另外,本反应第一步正方形铂配合物合成完成后的过滤过程中,产生的滤液中存在恶臭及剧毒的三甲基氯化锡,建议采用上述方法彻底除去滤液中三甲基氯化锡之后,再倒入废液桶。
参考文献
- [1] Z. Sun, K. Ikemoto, T. M. Fukunaga, T. Koretsune, Science 2019, 363, 151. doi: 10.1126/science.aau5441.
- [2] T. Iwamoto, Y. Watanabe, Y. Sakamoto, T. Suzuki, S. Yamago, J. Am. Chem. Soc. 2011, 133, 8354. doi: 10.1021/ja2020668.
- [3] E. Kayahara, X. Zhai, S. Yamago, Can. J. Chem. 2017, 95, 351. doi: 10.1139/cjc-2016-0474.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!





















No comments yet.