本文作者:海猫
导读
近日,南京大学雷建平教授课题组在分析化学杂志上发表论文,报道了一种基于封端修饰来调节铜纳米团簇(CuNCs)的聚集诱导发光(AIE)策略,两种分子识别模式相继进行,可以用于酶的高特异性检测。作者使用了对巯基苯硼酸(MBA)作为还原剂和稳定配体,在碱性溶液中制备了具有AIE特征的CuNCs。该CuNCs通过其中的硼酸与葡萄糖上的一对顺式二醇快速反应生成硼酸酯而特异性连接。而封端调控的AIE策略是通过使用D-葡萄糖6-磷酸酯(P-Glu)作为封端剂和底物修饰CuNCs来实现的。作者在P-Glu/CuNCs复合物中加入碱性磷酸酶,诱导磷酸基团的水解,从而激活了葡萄糖上的5,6-二醇。去封端的复合物可以通过两个CuNCs的5,6-二醇和硼酸之间的进一步结合而聚集,从而发出强的红色AIE荧光。酶促裂解与顺式二醇/硼酸结合的双重识别使得高特异性检测与酶活性的细胞成像得以实现。因此,这个封端调控的AIE策略为痕量分析中AIE现象的调控提供了一种通用的方法。
Cleancap-Regulated Aggregation-Induced Emission Strategy for Highly Specific Analysis of Enzyme
Yuanyuan Huang, Longyi Zhu, Jiahao Ji, Yang Li, Tianrui Liu, and Jianping Lei
Anal. Chem., Just Accepted Manuscript • DOI: 10.1021/acs.analchem.0c00217
正文
聚集诱导发光(AIE)是通过限制聚集状态下的分子内运动,从而使荧光显著增强的现象。AIE现象因其增强信号响应的能力和出色的光稳定性,被广泛应用在发光器件,生物传感器,细胞成像还有药物递送中。溶解性的变化,静电相互作用,靶点反应与环境刺激都可以促进AIE分子的聚集。大多数因亲疏水性或者静电相互作用的AIE聚集都是不规律的,而研究AIE体系的受控组装不仅可以高效传导信号,也可以进一步用于识别位点的设计。因此,在AIE分子的聚集过程中加入分子的特异性识别,或许可以建立一类通用且高性能的AIE生物传感器。
分子结构域之间的特异性识别在生物系统中起着至关重要的作用(例如酶-底物,抗原-抗体,硼酸-二醇,生物素-亲和素等)。高亲和度的生物分子识别是在体内外建立生物探针选择性的基础。然而,由于结合过程中相似结构的竞争和复杂基质中的信号干扰,探针与靶标之间仅有一种识别模式是不够的。如果设计两种识别,相继进行,就可以显著提高检测系统的可信度和选择性。在本篇工作中,作者将酶促裂解和顺式二醇/硼酸结合在一起,设计了一个针对癌细胞中酶的高特异性分析策略。
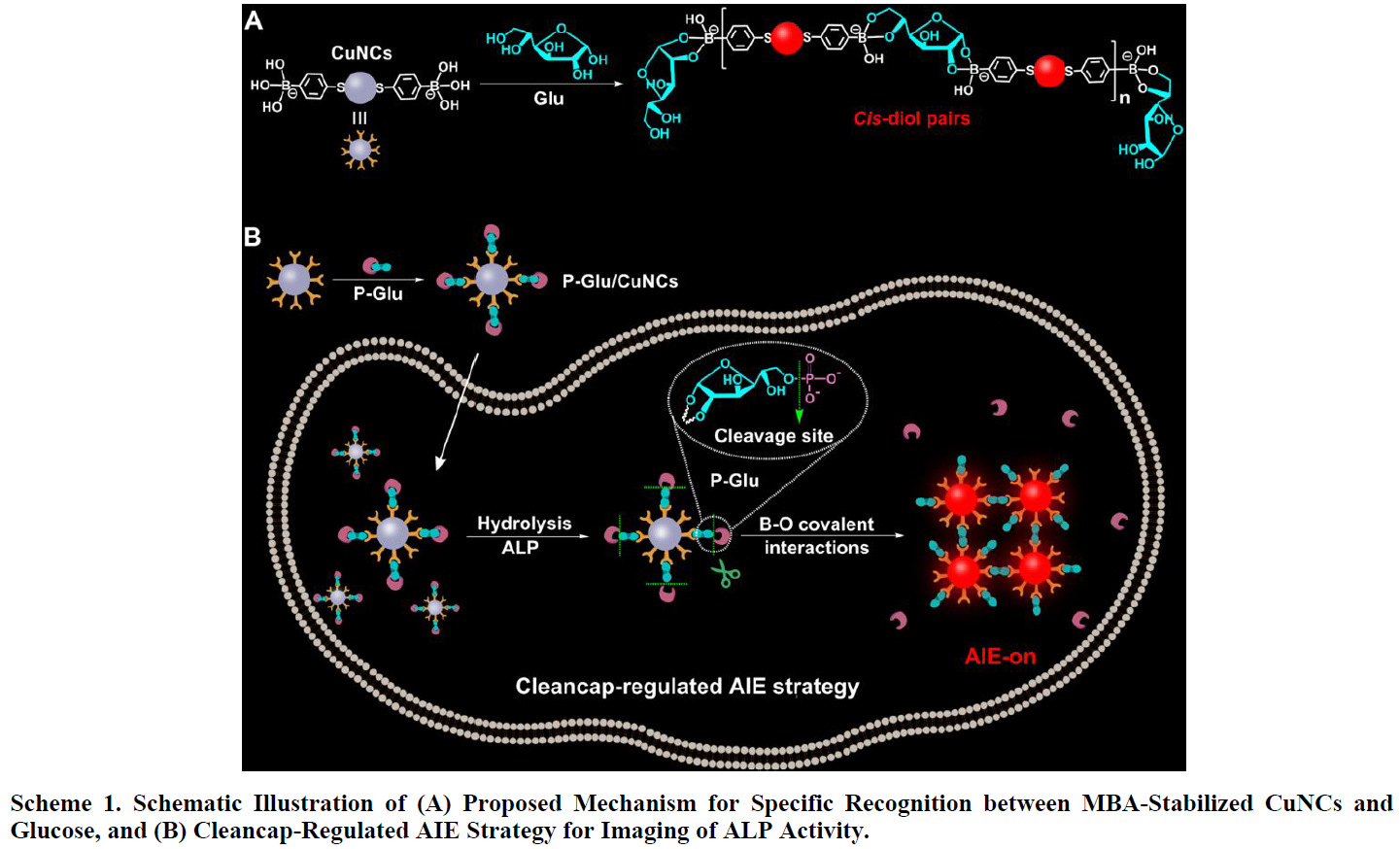
具有AIE特性的发光铜纳米团簇(CuNCs)在聚集态可以高强度发光,因此成为一种有前途的传感和成像材料。在本篇文章中,作者报道了一种基于封端修饰来调节铜纳米团簇(CuNCs)的聚集诱导发光(AIE)策略,两种分子识别模式相继进行,用于碱性磷酸酶(ALP)的高特异性检测(Scheme 1)。作者使用对巯基苯硼酸(MBA)作为还原剂,并通过Cu-S键使之作为稳定配体。硼酸和顺式二醇的结合可以快速稳定的生成环状硼酸酯键,从而使CuNCs和葡萄糖连接在一起。在碱性介质中,结合葡萄糖的CuNCs会聚集产生强的红色荧光,证明了它的AIE特性(Scheme 1A)。将D-葡萄糖6-磷酸酯(P-Glu)修饰在被MBA稳定的CuNCs上,得到P-Glu/CuNCs复合物。因葡萄糖的5,6-二醇被6-磷酸酯封装,P-Glu/CuNCs在碱性介质中可以很好的溶解而不会发出荧光。而在固定细胞中,ALP会识别复合物上的P-Glu并裂解掉磷酸基团,使得5,6-二醇重新被活化。去封端的复合物就会和另一个纳米粒子上的MBA配体通过B-O共价作用结合,诱导CuNCs的聚集,并使荧光产生(Scheme 1B)。该策略通过ALP/P-Glu与5,6二醇/MBA的双重识别,为ALP活性的高特异性检测提供了一种方便可信的检测方法,并且可以广泛应用在固定细胞中酶活性的原位定位。
首先,作者对制备好的铜纳米粒子进行了一些光学检测。在紫外-可见吸收光谱中,MBA在262 nm处的特征峰消失;在傅立叶变换红外光谱中,1010 cm-1和1350 cm-1的峰对应于B-OH键的振动和拉伸。这两个结果都证明了MBA在合成CuNCs的过程中被用作了还原剂和稳定配体。CuNCs的X-射线光电子能谱(XPS)表明该纳米粒子中的铜离子已经彻底从Cu(II)还原成低价态的铜。此外,在XPS谱图中191.4 eV的硼峰也证实了在CuNCs中硼酸的存在。
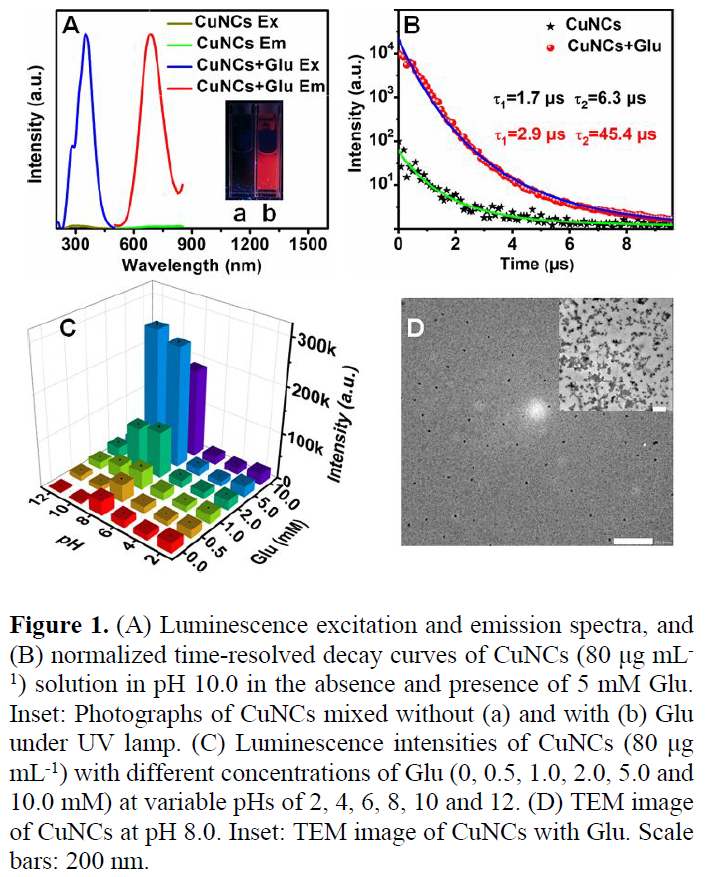
接下来,作者做了荧光分析,来评估通过硼酸/葡萄糖识别控制的AIE现象。当将经MBA稳定的CuNCs与葡萄糖进行混合时,在688 nm的荧光强度提高了一百倍,并伴随很大的Stokes位移(超过330 nm,Figure 1A)。因为CuNCs聚集,亮红色的荧光随之产生,这一现象通过动态光散射得到了证实。为了进一步探索机理,作者使用了两个指数拟合计算了不存在与存在葡萄糖时,CuNCs的时间分辨衰减拟合曲线(Figure 1B),数据分别为1.7微秒(89.5%),6.3微秒(10.5%)和2.9微秒(96.8%),45.4微秒(3.2%)。由此可以看出聚集的CuNCs的平均荧光寿命(17.39微秒)明显比分散的纳米颗粒(3.09微秒)要长。CuNCs在溶解状态下,发射较弱,寿命较短,这是因为非辐射弛豫、分子运动导致的能量损失,而在聚集状态下,该过程被禁止,从而使荧光寿命提高,发射效率增强。pH值也会对AIE现象产生影响。在pH值高于8.0时,将葡萄糖的浓度提高至5.0 mM可以看到显著的荧光增强(Figure 1C),这是因为碱性介质有利于硼酸的酯化,从而产生较强的聚集作用。而pH低于8.0时,提高葡萄糖的浓度不会产生明显的荧光信号变化,这是因为酸性环境有利于硼酸酯的水解反应。这些结果也被CuNCs的TEM图像(Figure 1D),尺寸分布与zeta电位证实。
然后作者在CuNCs中连续添加葡萄糖,发现葡萄糖浓度从0增加到1.0 mM时,荧光发射强度只增加了很少。这是因为单个的顺式1,2-二醇与MBA之间的共轭效果比较好,聚集效率较低。但是,当葡萄糖浓度超过1.0 mM的时候,荧光强度显著增加,这是因为一对顺式二醇单元与不同纳米簇之间的结合限制了聚集状态下的分子运动。
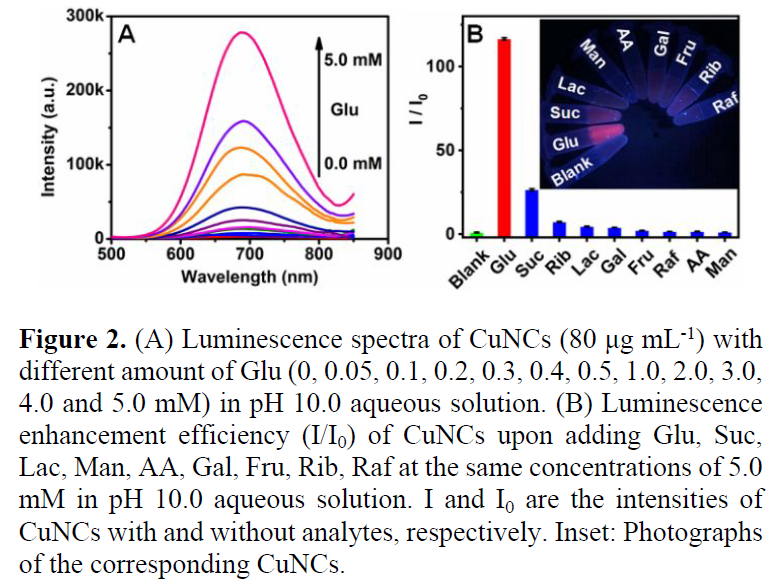
作者在两个线性模式关系下,计算葡萄糖的检测限分别是5.15 μM和303.03 μM,在pH值为9.0和10.0的水溶液中也可以获得相似的结果(Figure 2A)。这个结果优于之前基于硼酸的葡萄糖检测器。接下来,作者在pH值为10的水溶液中评估了CuNCs和葡萄糖的特异性识别。结果表明,添加葡萄糖后,CuNCs的发光强度增加了超过100倍,这比与其他类似结构混合导致的光强升高要高得多(Figure 2B)。这证明了像葡萄糖和麦芽糖这样有一对顺式二醇的分子对CuNCs的聚集是必不可少的。
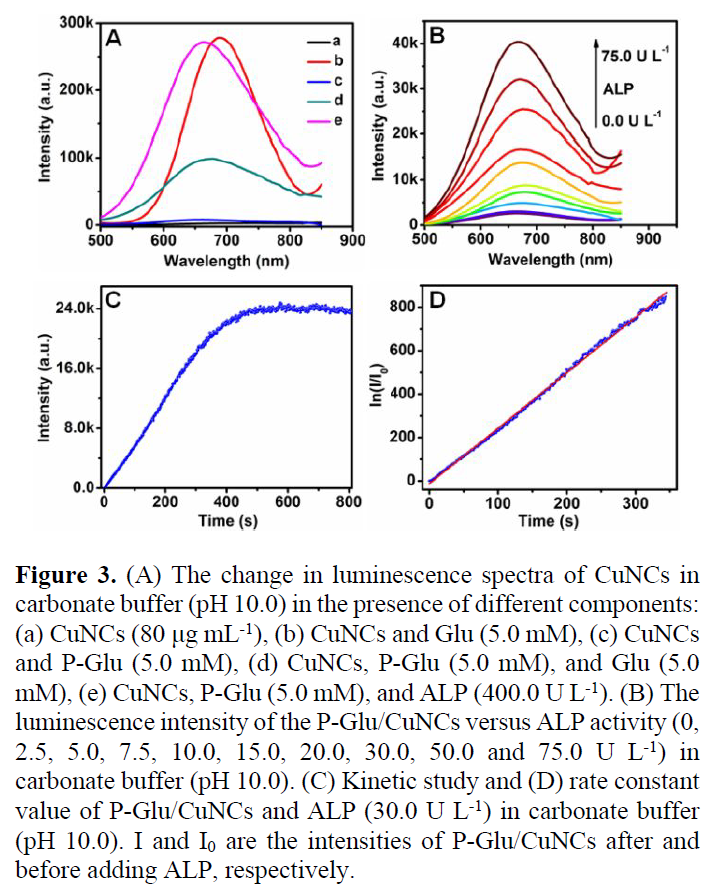
为了分析ALP的活性,作者在CuNCs表面修饰了P-Glu,以设计一个封端调节的AIE策略(Figure 3A)。未修饰葡萄糖的和修饰了P-Glu的CuNCs(line a和c)荧光发射强度很低,表明他们在溶液中未发生聚集。而加入ALP(400 U/L)之后,葡萄糖表面的磷酸基团被水解掉导致CuNCs聚集,导致荧光强度显著增加。由图中的line b和d可以看出,与P-Glu与葡萄糖混合的CuNCs的发射要比仅与葡萄糖混合的CuNCs的发射强度弱,这表明P-Glu可以与铜纳米粒子竞争性结合,从而降低AIE效率。接下来,作者优化了用于修饰的P-Glu的量(Figure 3B),因为这会影响检测系统的性能。由Figure 3C和3D可以看出,复合物的发光强度随孵育时间的增加而增加,并在500秒达到稳定,一级速率为2.55 s-1。在优化后的条件下,随着ALP含量从0.56 U/L增加到30.0 U/L,复合物的荧光强度增加,检测限低至0.17 U/L,比其他基于纳米材料的方法要低。并且,该检测策略可以在多种干扰下高特异性的检测ALP,并可以进一步检测酶抑制剂Na3VO4的效率,IC50值为16.8 μM。因此,作者证明了他们设计的策略确实是可以快速、实时,且高特异性检测酶的。
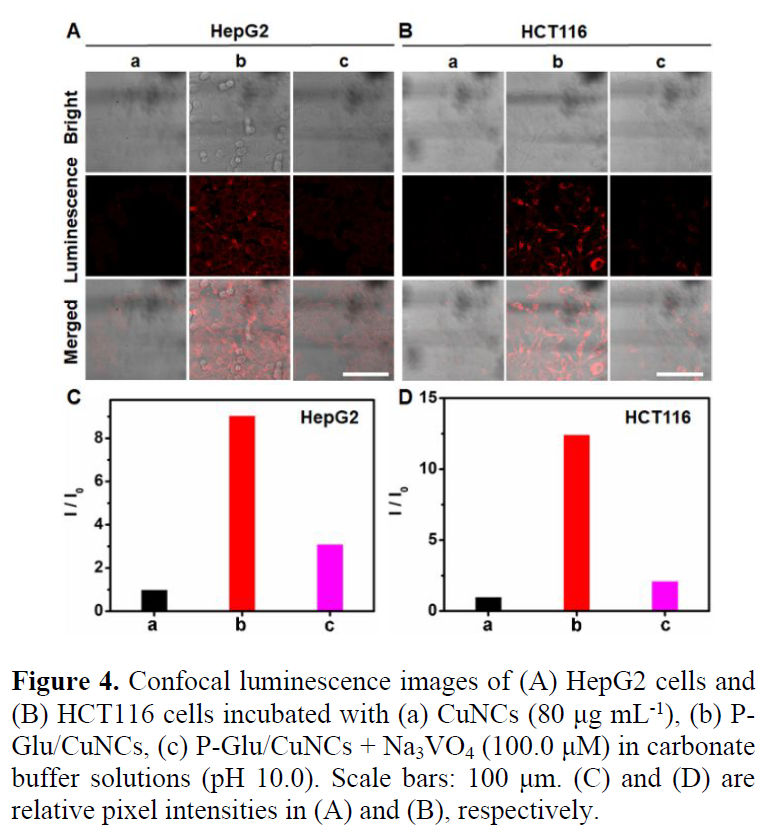
最后,作者将该策略应用在于固定细胞中检测ALP的活性。在HepG2细胞中,MBA稳定的铜纳米颗粒被内吞后,显示的荧光可以忽略不计(Figure 4A,a),但将细胞与P-Glu/CuNCs孵育后,ALP水解P-Glu使得CuNCs聚集,将HepG2细胞的荧光强度提高了9倍(Figure 4A和C)。在孵育前加入抑制剂Na3VO4会抑制内源性ALP活性,导致荧光的减弱(Figure 4A,c)。使用HCT116细胞也观察到了类似的结果,证明该检测内源性ALP活性的方法具有普遍性。
总结
南京大学雷建平教授课题组报道了基于P-Glu修饰来调控CuNCs的AIE现象的策略,可以对ALP活性进行高特异性的分析。P-Glu/CuNCs配合物在碱性溶液中溶解的比较好,没有聚集发光现象,而当P-Glu的磷酸基团被ALP水解掉之后,两个纳米粒子会因为5,6-二醇与MBA配体的结合而聚集,从而产生强烈的AIE发射。与其他聚集方法不同,由于ALP水解与顺式二醇/硼酸结合的相继进行,使得该策略针对不同的干扰都具有出色的选择性。该复合物也可以在不同种类的固定细胞中对ALP进行成像。因此,这个封端调节的AIE策略可以广泛的应用于准确、灵敏的检测细胞中的酶。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.