概要
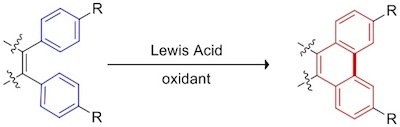
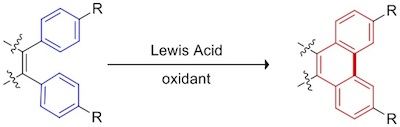
Scholl反应也称氧化偶联,指两个或两个以上芳环间在路易斯酸、氧化剂的共同作用下C-H键直接生成C-C键的反应,主要用作扩展芳环共轭体系、延长碳链。通常分子内氧化偶联较分子间氧化偶联好,芳环富电子也有利于发生氧化偶联[1][2]。该类反应是特定条件下对heck、Suzuki等传统经典偶联反应的有力补充。
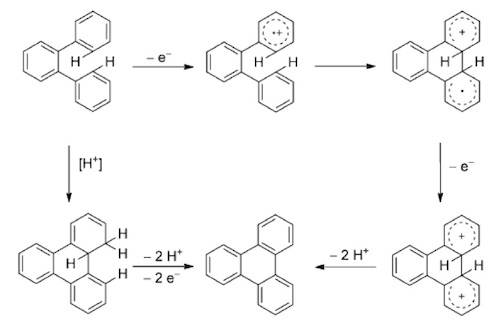
反应机理
反应实例
常用的反应体系有氯化铁/硝基甲烷,二氯甲烷;三氟氧钒的二氯甲烷溶液;(双(三氟乙酰氧基)碘)苯(PIFA)和三氟化硼乙醚的二氯甲烷溶液,以及DDQ/三氟甲基磺酸的二氯甲烷溶液等。
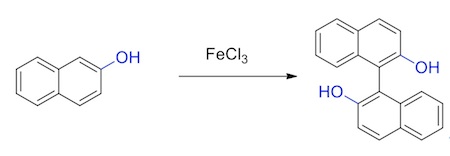
1.三氯化铁条件下,发生分子间氧化偶联生成联萘类化合物[3]
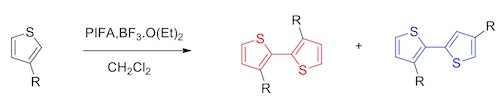
2.PIFA/三氟化硼乙醚条件下,发生分子间氧化偶联形成联噻吩类化合物[4]
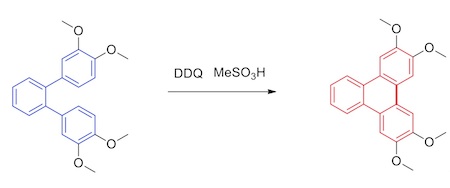
3.DDQ/甲烷磺酸条件下,发生分子内氧化偶联形成大芳环体系化合物[5]
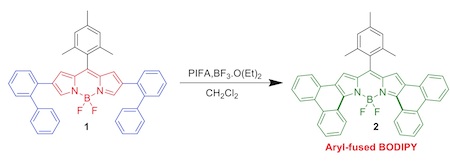
4.在功能染料BODIPY上的运用[6],[7]
分子1通过氧化偶联比较便捷的合成了分子2,同时分子1的最大吸收波长从573nm增加到分子2 的673nm。
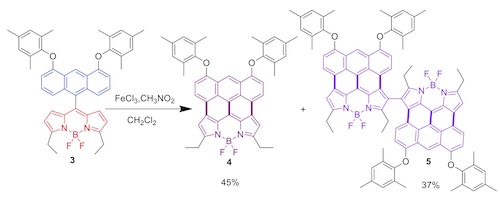
从分子3氧化偶联合成分子4的过程中,部分发生了分子间偶联反应得到了分子5。从这个反应可以明显看出:Scholl 反应受到芳香环的电子云密度影响,吡咯环较苯环优先,且受到芳环相连基团的导向(包括电荷导向、空间导向)。特别有意思的是分子3上的2,4,6-三甲基苯氧基,既可以增加蒽环电子密度,又可以减少蒽环上发生偶联的几率,还可以减弱分子间的π-π堆积从而增加分子4和分子5在有机溶剂中溶解度。与吡咯环相连的乙基也起类似作用。这也说明了Scholl 反应的一些局限性,特定条件下才能使用,比如从分子设计上讲一般要一些富电子基团进行电荷导向,一些位阻基团进行空间导向,当然从实验操作上讲还与反应液浓度,温度等有关。
实验步骤
实验技巧
参考文献
- Grzybowski, M.; Skonieczny,K.; Butensch, H.; Gryko, D.T. Angew. Chem. Int. Ed. 2013, 52, 9900–9930. DOI: 10.1002/anie.201210238
- Lewtak , J.P.; Gryko, D. T. Chem. Commun., 2012, 48,10069–10086. DOI: 10.1039/C2CC31279D
- Jiao, S.J.; Lu, J.M.; Zhu, X.L.; Yang, J.; Lang, J.P.; Wu, L. Syn. Commun., 2002 , 32, 3069 – 3074. DOI: 10.1081/SCC-120013000
-
Tohma, H.; Iwata, M.; Maegawa, T.; Kiyono, Y.; Maruyama, A.; Kita, Y. Org. Biomol. Chem., 2003, 1, 1647-1649. DOI: 10.1039/B302462H
- Linyi, Z.; Ruchi, S.; Shriya, H.; Rajendra, R. J. Org. Chem., 2010, 75, 4748-4760. DOI: 10.1021/jo100611k
- Hayashi, Y.; Obata, N.; Tamaru,M.; Yamaguchi, S. et al. Org. Lett. 2012, 14, 866–869. DOI: 10.1021/ol2033916
- Zeng, L.T.; Jiao, C.J.; Huang,X. B.; Huang, K. W.; Wu, J. S. Org. Lett. 2011, 13, 6026–6029. DOI: 10.1021/ol202493c
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!























No comments yet.