译自Chem-Station网站日本版 原文链接:MALDI-TOF MSを使用してCOVID-19ウイルスの鼻咽頭拭い液からの検出に成功
翻译:炸鸡 校对:Jojo
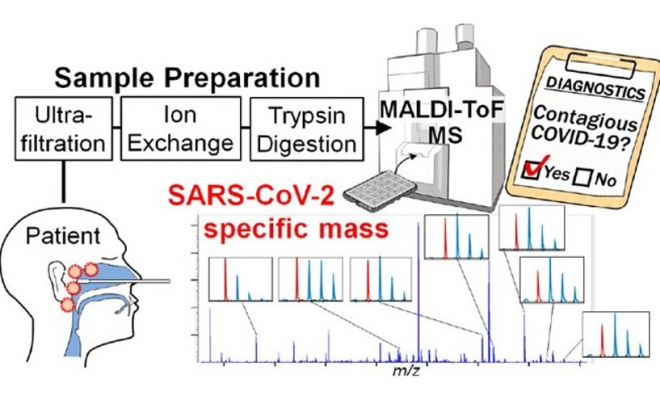
2020年3月18日,《Analytical Chemistry》杂志上刊登了一篇来自日本国立医药食品卫生研究所的一篇论文,该论文介绍了日本电子公司(JEOL)的JMS-S3000 SpiralTOF™-plus基质辅助激光解析离子化串联飞行时间质谱仪能成功从人的鼻咽拭液中检测出新冠病毒。(引用:JEOL3月28日新闻稿)
在检测新冠病毒感染的方法中,目前较为流行的都是PCR法,即通过扩增病毒的DNA来检测病毒,这属于生物手段检测;而在化学上一般用于推测分子结构的质谱也被发现能成功检测出新冠病毒了,下面进行详细介绍。
研究背景:目前检测病毒普遍采用的都是实时PCR检测方法,即使用逆转录PCR(RT-PCR)来判别个体是否感染了新冠病毒。但PCR检测有不少缺点。如必须使用复杂的器材和试剂,检测过程对温度十分敏感,必须密切注意检测过程是否被污染等。尽管曾经有出现过用LC-MS/MS和LC-QTOF MS来代替PCR检测SARS-CoV-2(新型冠状病毒(2019-nCoV)的正式名称)的特有蛋白质,但结果准确性不是很高。虽然随后开发出一种经过免疫亲和精制后能用LC-MS检出的方法,但免疫亲和精制需要特别的抗体。它最突出的缺点是由于使用了LC,每一个样本都需要花费时间在色谱柱分离上。
用MALDI-TOF MS检测新冠病毒不需要蛋白质多肽等复杂试剂,污染风险也很低。虽然此前有通过分析SARS-CoV-1病毒或流感病毒的蛋白质或胰蛋白酶分解酶来判别,但需要用到经过培养的样品,这样就无法做到即时检测出病毒。针对SARS-CoV-2病毒虽然也有MALDI-TOF MS或MALDI FT-ICR MS的检测手段,但准确性较低,且没有经过临床试验,所以并不能算是真正有意义且可靠的检测方法。本期的主角论文中研究人员研究了从鼻咽拭液中如何纯化SARS-CoV-2病毒并用MALDI-TOF-MS检测SARS-CoV-2病毒的方法。
下面来看论文的实验结果。首先,对失活的SARS-CoV-2进行聚丙烯酰胺电泳(SDS-PAGE)分离,并确认了主带在大约50kDa的位置。然后,研究人员通过MALDI-TOF MS对这50kDa中的胰蛋白酶肽进行质谱分析并与病毒多肽数据库进行对比,检测到了20个来自SARS-CoV-2核衣壳蛋白(NP)的多肽。 并将这20个多肽作为以后MALDI-TOF MS检测中检出病毒的指标分子。
其次是关于SARS-CoV-2的核衣壳蛋白(NP)的纯化,由于病毒鼻咽拭液中含有多种蛋白质,它们可能会干扰检测过程,因此检测前的纯化操作是必不可少的。关于如何提纯病毒,论文首先参考了已知的能够以高回收率回收病毒的超滤法。将失活的SARS-CoV-2病毒与已知COVIS-19阴性患者的鼻咽拭液混合在一起,以不同的分馏分子量进行纯化,结果证实了300 kDa MWCO超滤盒的分离效果很好,此外,论文中证实了聚丙烯酰胺电泳(SDS-PAGE)的阴离子交换可以除去不慎被掺杂进来的蛋白质。
SDS-PAGE纯化结果 A:浓缩SARS-CoV-2用不同MWCO超滤盒纯化的结果B:鼻咽拭液用不同MWCO超滤盒纯化的结果 C:SARS-CoV-2和鼻咽拭液的混合物用300 kDa MWCO超滤盒和阴离子交换纯化的结果 CF= Concentrated Fraction, FF = Flow-through Fraction(摘自原论文)
如此建立了一种可靠的病毒纯化方法。使用上述建立的纯化方法对SARS-CoV-2和COVID-19阴性鼻咽拭液的混合物进行纯化,将提取物通过MALDI-TOF MS进行分析。
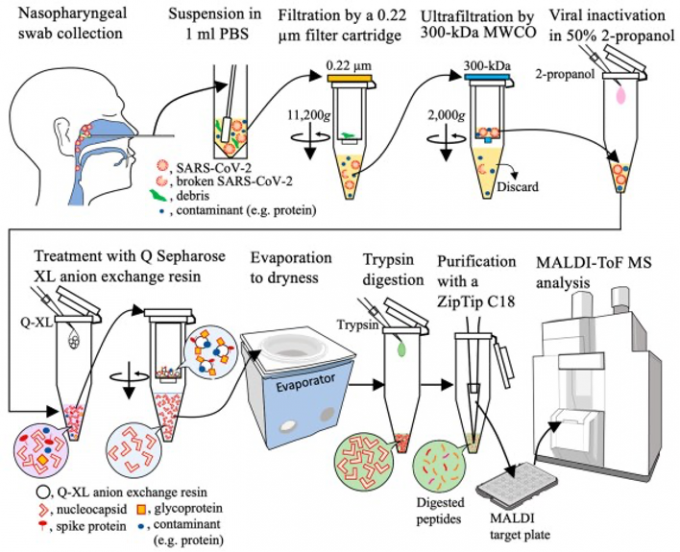
测定方法(摘自原论文)
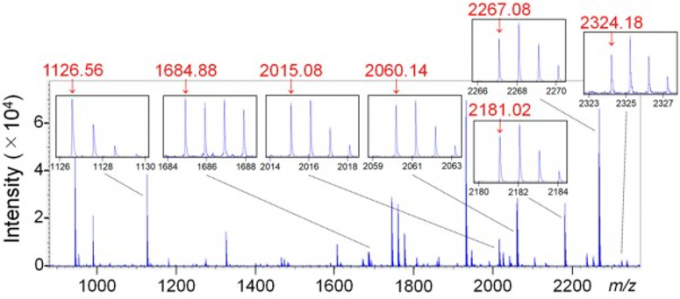
从浓度为108.7 的样品中检测到7个来源于核衣壳蛋白(NP)的多肽。不含SARS-CoV-2病毒的鼻咽拭液样品里的这7个多肽的S/N比在0.86到1.10之间,而来源于核衣壳蛋白(NP)的多肽的S/N值临界值为2.0。
MALDI-TOF MS谱图(摘自原论文)
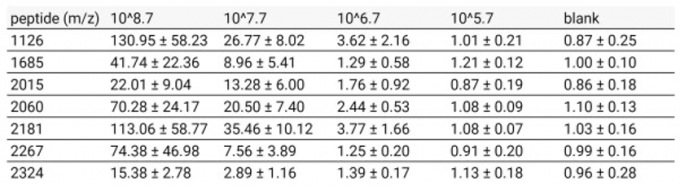
经过比较不同浓度样品的多肽峰的S/N比值后,将能检验出SARS-CoV-2的最低样品浓度确定为106.7。这一最低浓度不仅参考了数学模型分析结论,也考虑到了临床上能检验出病毒的最低精度要求。前人的研究需要借助超滤精制+MALDI-FT-ICR MS检测技术才能从高浓度的样品中检测出指标多肽,然而本研究利用的超滤和阴离子交换精制+MALDI-TOF MS检测技术能从低浓度样品中检测出指标多肽。
各浓度的各峰的S/N比
最后实地检验研究所开发的方法能否用于检测新冠病毒。检验方法:采集19位新冠阳性患者的鼻咽拭液样本和4位RT-PCR和TCID50都显示新冠阴性的患者的鼻咽拭液样本,按照上述研究出的精制方法纯化,然后用MALDI-TOF MS检测多肽的出峰情况。如果是阳性患者,2到7各多肽的峰值都在临界值以上,如果是阴性患者,所有的多肽峰值都在临界值以下。阳性患者的样品的TCID50值也佐证了MALDI-TOF MS也能从新冠感染患者的鼻咽拭液样品中检测到来自SARS-CoV-2核衣壳蛋白的多肽。
此外,研究人员还注意到m/z 2060附近检测到的峰的精密质量会受到变异毒株的影响而改变。这说明论文的检测病毒的方法可以拿来应对现在肆虐的SARS-CoV-2的变异毒株。
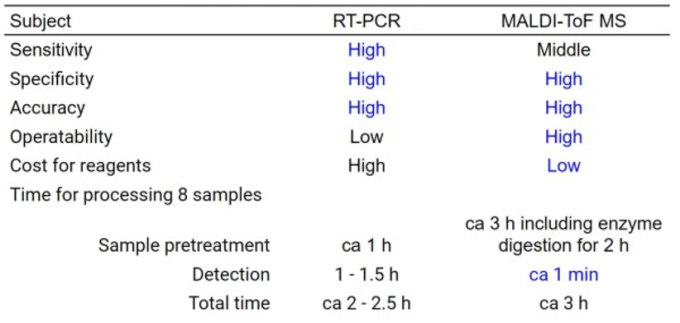
最终结论:本研究开发的适宜多样本的纯化方法联合MALDI-TOF MS成功地检测出了衍生自SARS-CoV-2核衣壳蛋白的多肽。本方法较RT-PCR的优势与劣势如下:优势是极大缩短了检测时间与检测成本,劣势是检验灵敏度不如RT-PCR,但能准确判别出阳性患者。论文的方法可以帮助控制SARS-CoV-2的感染扩大。
本方法与RT-PCR方法的比较
本篇论文提出了用MALDI-TOF MS检测新冠病毒,研究十分有意义。由于RT-PCR的检测方法需要样品在机器中的停留较长时间,因此如果想要同时测量多个样品,就需要更多的RT-PCR装置,本篇论文的方法的一个很大的优点是只需要一台MALDI-ToF MS就可以满足同时检测多个样品的需求。虽然现在检测SARS-CoV-2的需求会不会增大尚不清楚,但本论文的方法可以对未知病毒的研究以及防控病毒疫情做出贡献。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载





















No comments yet.