本文作者:杉杉
导读
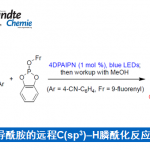
杂芳烃作为生物活性化合物和功能材料中的基本骨架,而杂芳烃与脂肪族C-H键的脱氢偶联可直接获得官能化的杂芳烃衍生物。近日,厦门大学徐海超教授课题组在德国应化杂志(Angewandte Chemie-International Edition)发表论文,通过将电化学和光化学相结合,无需金属催化剂或化学氧化剂,即可实现杂芳烃和C(sp3)-H供体的脱氢交叉偶联。反应机理表明,C(sp3)-H供体与氯自由基经氢原子转移从而合成关键的C-自由基中间体,再与质子化的N-杂芳族化合物反应,从而获得烷基化的杂芳烃产物。
Scalable Photoelectrochemical Dehydrogenative Cross-Coupling of Heteroarenes with Aliphatic C-H Bonds
Pin Xu, Peng-Yu Chen, Hai-Chao Xu*
Angew. Chem. Int. Ed. ASAP DOI:10.1002/anie.202005724
正文
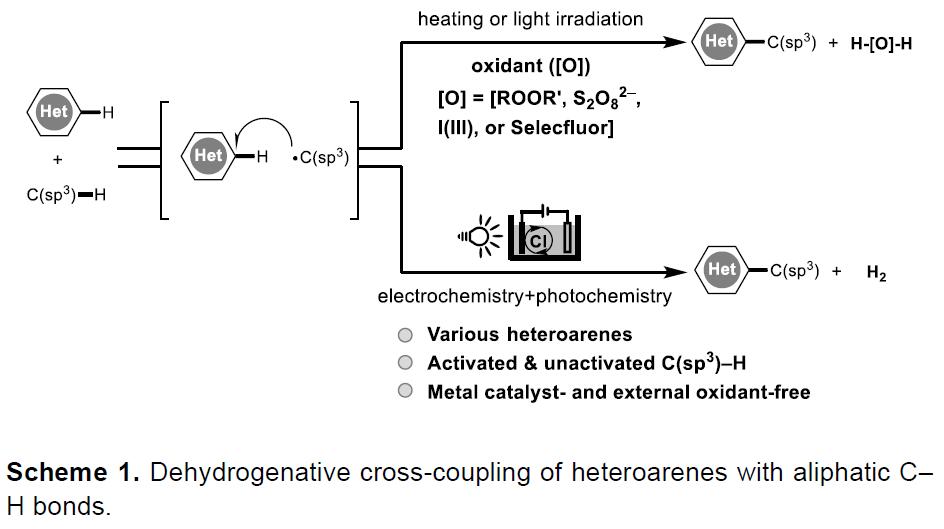
C-H键之间的脱氢交叉偶联是构建C-C键最有效方法之一,具有高原子经济性、原料易得等特点。此外,杂芳烃化合物广泛存在药物、天然产物和功能材料中。因此,很多课题组开始对杂芳烃与脂肪族C-H供体的交叉偶联进行了研究(Scheme1, top)。这些方法通常涉及一种Minisci型机理,通过在杂芳烃中添加一个以碳为中心的自由基,即可形成C-C键。而关键的C-自由基中间体,可由脂肪族的C-H供体通过氧或氮原子为中心自由基(由热或光诱导的化学不稳定氧化剂的裂解产生,如过氧化物(ROOR’),过硫酸盐(S2O82-),I(III)试剂或Selectfluor试剂)经的氢原子转移(HAT)产生。但是,化学氧化剂的使用会降低整个过程的原子经济性。
在过去的几年中,由于电流可代替氧化剂或还原剂实现氧化还原反应,从而使有机电化学受到了广泛的关注。阳极氧化和阴极质子还原的同时释放H2进行脱氢反应,从而消除了对化学计量的电子或质子受体的需要。尽管已经实现了电化学促使的自由基C-H氟烷基化和杂芳基的酰化反应,但对于缺电子的杂芳烃与各种C(sp3)-H供体的有效电化学偶联仍然未知,可能是因为两个偶联体都很难氧化,并且在典型的电化学条件下,富含电子的烷基容易氧化成碳正离子。
尽管已有文献报道通过H2的释放进而发生光化学脱氢交叉偶联反应,但钴催化剂会导致烷基自由基的还原消除,从而限制了光化学方法的范围。电化学与光化学的结合,可能实现仅使用电化学或光化学很难实现的反应。最近,Lambert课题组报道了光电催化下杂芳烃与醚的交叉偶联反应。此外,基于对无化学氧化剂Minisci型反应的研究以及相关前期工作的总结,在此,厦门大学徐海超教授课题组报道了通过光电化学方法,实现了杂芳烃与各种活化和未活化的C(sp3)-H供体的脱氢交叉偶联(Scheme 1, bottom)。
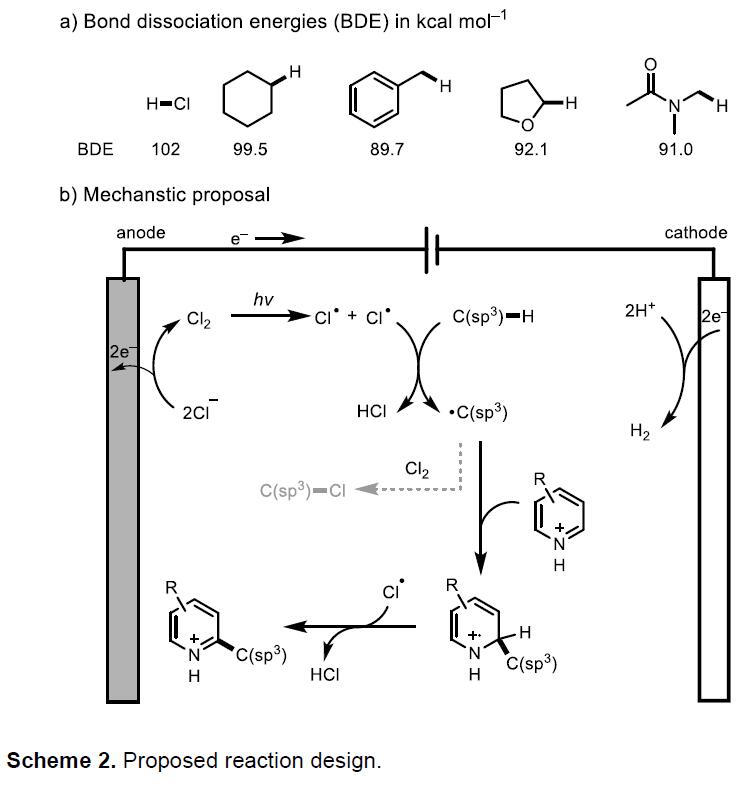
在该光电催化循环体系中,Cl•可将C(sp3)-H转化为C-自由基。而HCl的BDE相对较大(102 kcal mol-1),确保Cl•可以与多种活化和未活化的脂肪族C-H键反应(Scheme 2a)。具体反应过程如下(Scheme 2b),首先Cl–阳极氧化产生Cl2,经光催化促进了发生均质裂解,从而形成Cl-自由基。随后,再与C(sp3)-H供体经氢原子转移产生的C-自由基。紧接着,再与质子化的N-杂芳族化合物反应,从而获得自由基阳离子中间体。最后,在Cl•进行重新芳构化。此外,在阳极上连续生成低浓度Cl2,避免了有害气体的使用。同时,在C-C交叉偶联过程中损失的电子和质子在阴极结合产生H2。
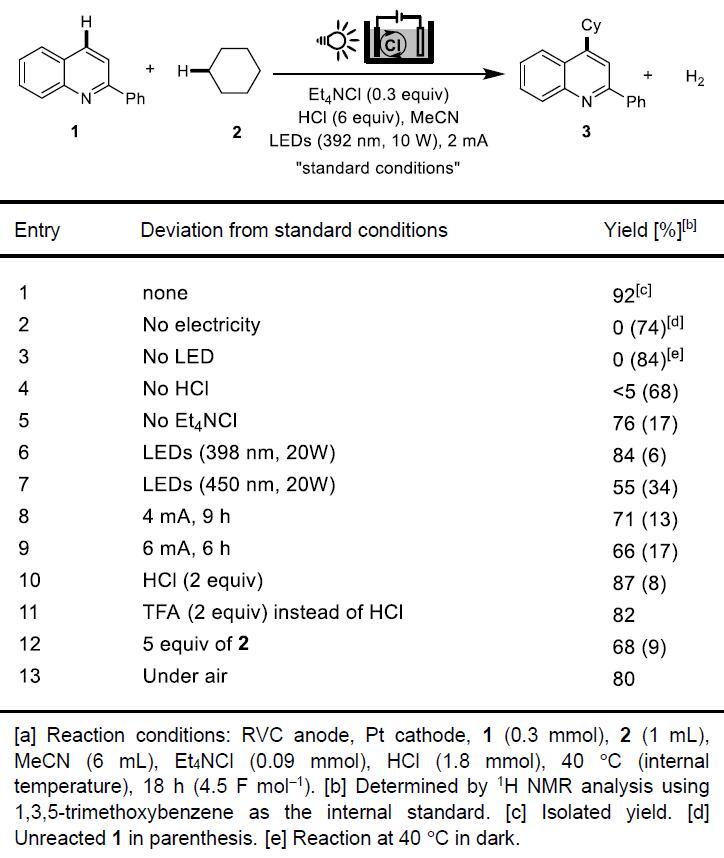
首先,作者以2-苯基喹啉(1)和环己烷(2)作为模型底物,进行了相关脱氢交叉偶联反应条件的筛选(Table 1)。通过大量条件筛选后,当在使用网状玻璃碳(RVC)阳极和Pt阴极的无隔膜电解槽中,通过LED(392 nm,10 W)照射下,于含有Et4NCl和HCl的MeCN溶剂中进行光电化学反应时,可获得92%收率产物3(entry 1)。而在无光、电、酸时,基本不发生反应,但在不使用Et4NCl收率有所下降(entries 2-5)。若将LED的波长和功率增加到398 nm(20 W)或450 nm(20 W)或将电流增加到4或6 mA,收率均有所下降(entries 6-9)。此外,若将HCl的量降低至2当量、环己烷降低至5当量、用TFA代替HCl均不利于反应(entries 10-12)。尽管没有必要严格地除去氧气,但是在空气下进行反应会使收率降低至80%(entry 13)。
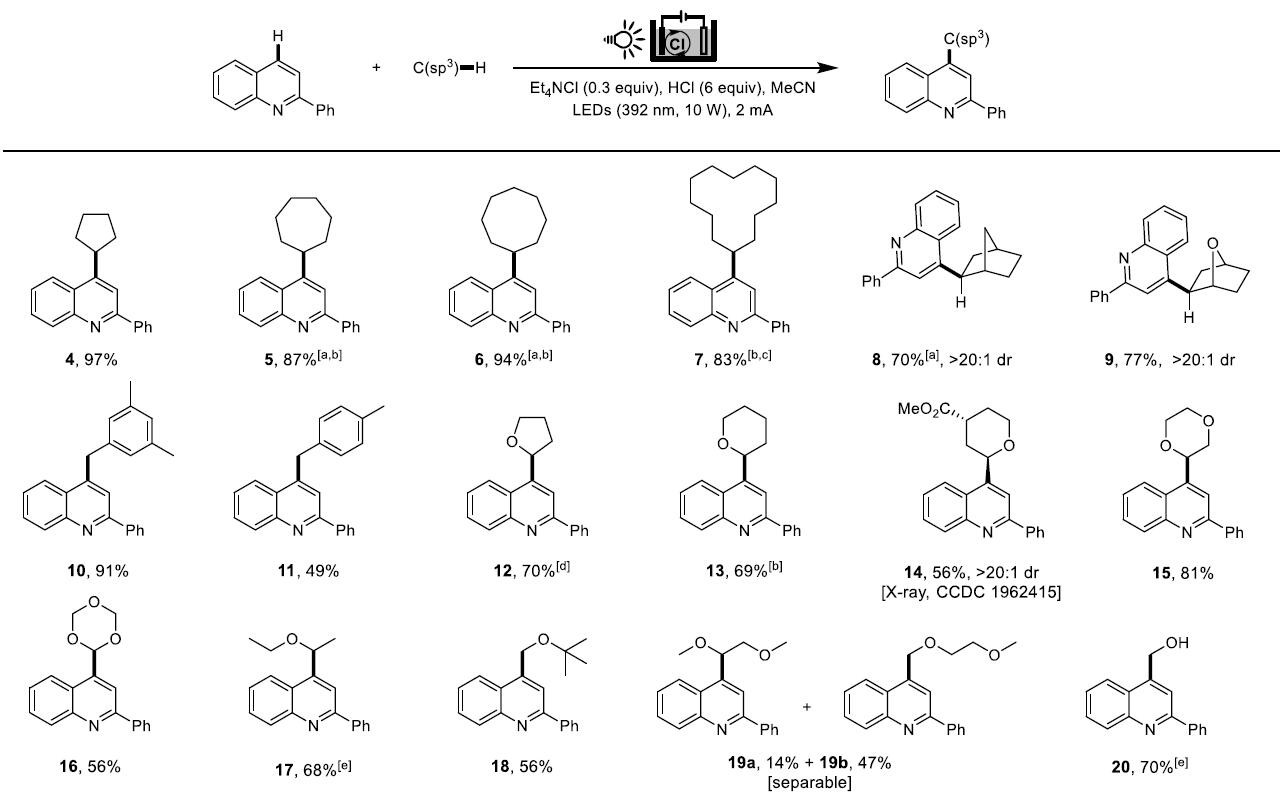
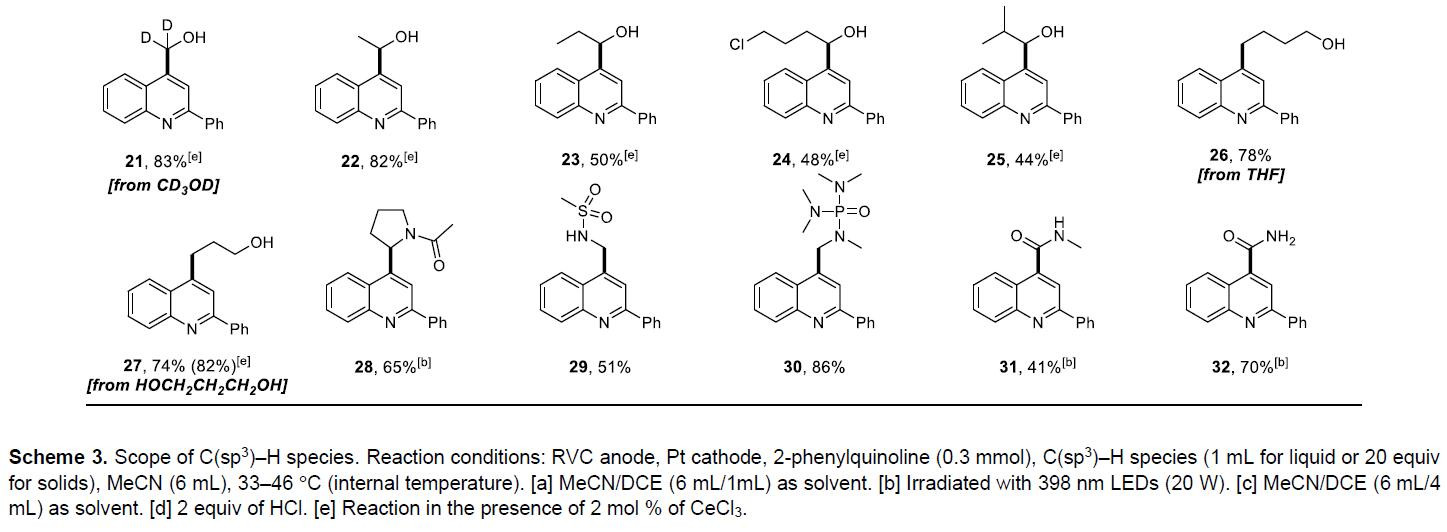
在获得上述最佳反应条件后,作者首先固定2-苯基喹啉,研究了C(sp3)-H底物的范围(Scheme 3)。反应结果表明,环状烷烃均是良好的底物,从而获得相应的产物4–7。值得注意的是,降冰片烷(8)和1,4-环氧环己烷(9)都以区域和立体选择性方式与2-苯基喹啉反应。同时,该反应可与多种C(sp3)-H共体反应,如甲苯衍生物(10和11)、醚(12–19)、伯醇(20–25)、酰胺(28)、磺酰胺(29)和磷酰胺(30),它们中大多数会产生易于氧化成碳正离子的自由基中间体。此外,在标准反应条件下,四氢呋喃(THF)、乙醚和伯醇的反应观察到了C-O键的断裂。同时,甲酰胺中的甲酰基C(sp2)-H键也可被活化,从而引入酰基(31和32)。
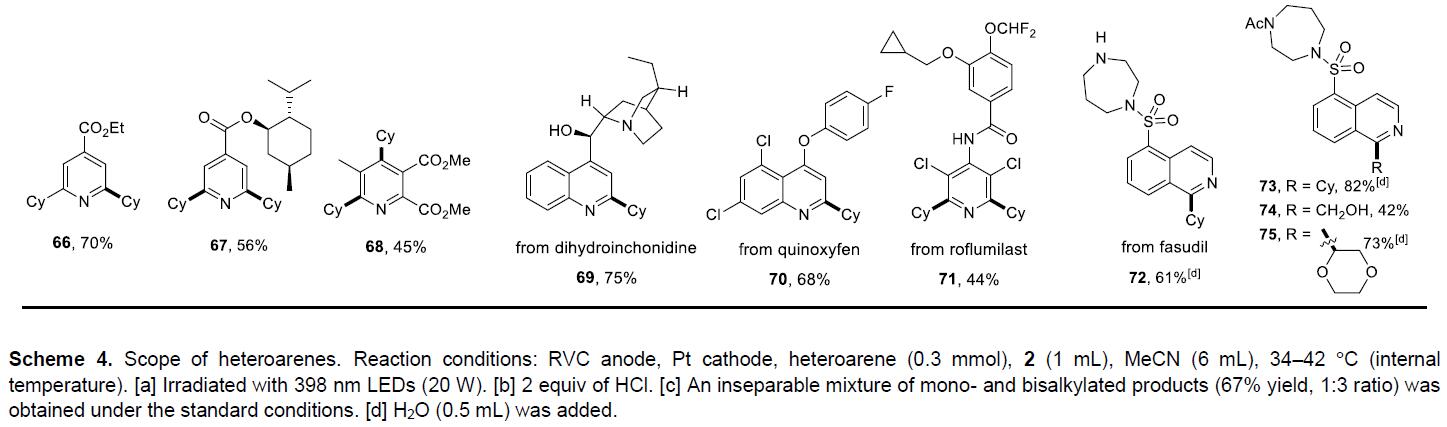
随后,作者固定环己烷,研究了杂芳烃的底物范围(Scheme 4)。反应结果表明,喹啉上含有OMe、Me、Cl、Br基团均与体系兼容,从而获得产物33–43。同样,异喹啉、菲啶、喹唑啉、喹喔啉、酞嗪、苯并噻唑、苯并噻吩,也可以环己烷反应获得相应的产物44–52,54。然而苯并恶唑(53)发生分解,无法获得所需的产物。嘌呤衍生物、咪唑并[1,2-b]哒嗪、哒嗪、嘧啶、吡嗪、吡啶的化合物均可与体系兼容,从而获得相应的产物55–68。此外,该方案还可对一些药物和生物性化合物进行后期修饰,如二氢辛可尼定(69)、奎诺芬(70)、罗氟司特(71)、法舒地尔(72)、酰化法舒地尔(73–75)等。
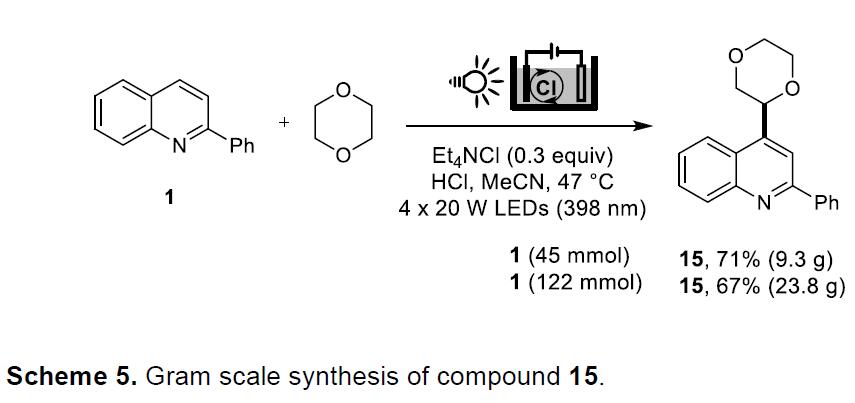
随后,作者开始尝试相关的克级实验(Scheme 5)。间歇式反应器的低表面积体积比阻碍了光电化学反应的规模化,但通过采用流动装置,可以进行克级规模的放大。
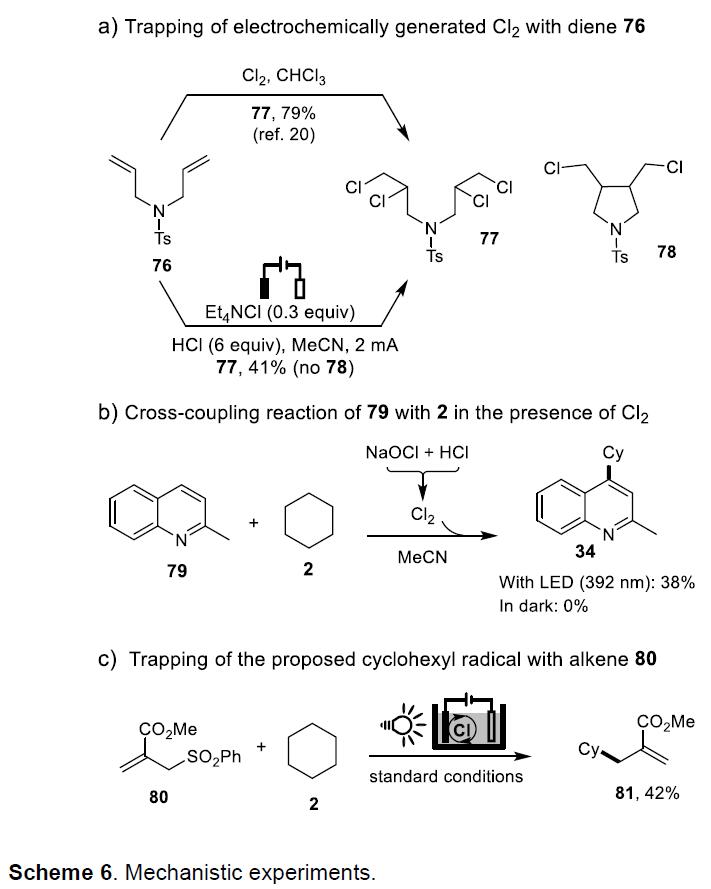
为了进一步了解反应的机理,作者进行了相关的对照实验(Scheme 6)。据文献报道,二烯76可与Cl2反应生成四氯化合物77,而不是自由基环化衍生的加合物78。与此相一致,在含有Et4NCl和HCl的MeCN溶液中电解获得41%收率化合物77,而未检测到78(Scheme 6a)。此外,通过NaOCl与HCl混合而产生Cl2,在Cl2存在下可实现79与2的交叉偶联获得预期的产物34,而当反应混合物避光时未观察到产物形成(Scheme 6b)。反应结果表明,电化学产生Cl2,并且对于促进随后的脱氢烷基化反应至关重要。同时,亲电烯烃80与环己烷的光电化学反应以42%的收率获得化合物81,为烷基作为中间体提供了支持(Scheme 6c)。
总结
厦门大学徐海超教授课题组报道了,通过将电化学与光化学相结合,实现了杂芳烃与脂肪族C-H键的高效脱氢交叉偶联。该反应无需使用金属催化剂或化学氧化剂,同时具有广泛的底物范围(各种杂芳烃以及活化和未活化的C(sp3)-H供体均与体系兼容)。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



















No comments yet.