本文作者:杉杉
导读
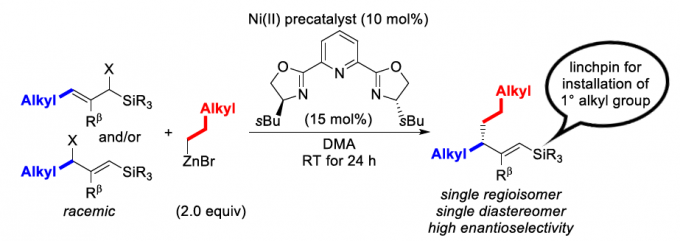
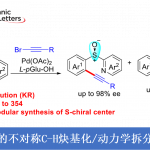
近日,德国柏林工业大学Martin Oestreich课题组在Angew. Chem. Int. Ed.上发表论文,报道了一种合成具有烷基取代无环烯丙基的对映和非对映选择性的策略。同时,对于不对称诱导和位点选择性均可在镍催化外消旋甲硅烷基化烯丙基卤化物和烷基锌试剂的C(sp3)-C(sp3)交叉偶联中被控制。此外,甲硅烷基使烯丙基移位形成乙烯基硅烷区域异构体,所得的C(sp2)-Si键作为后续引入各种C(sp3)取代基的关键。
Enantio- and Regioconvergent Nickel-Catalyzed C(sp3)-C(sp3) Cross-Coupling of Allylic Electrophiles Steered by a Silyl Group
Nektarios Kranidiotis-Hisatomi, Hong Yi, and Martin Oestreich*
Angew. Chem. Int. Ed. ASAP DOI:10.1002/anie.202102233
正文
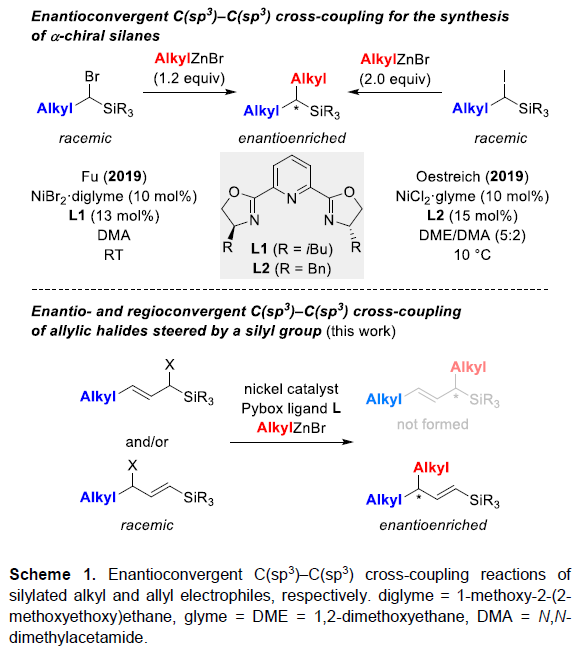
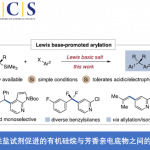
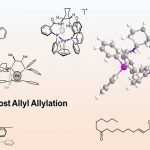
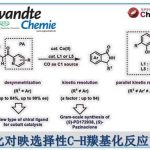
涉及自由基中间体的镍催化不对称合成可通过对映发散的方式从外消旋烷基亲电试剂中构建C(sp3)-C(sp3)键,如大量基于锌的亲核试剂和亲电偶联试剂。2019年,Fu等[1]报道由外消旋α-溴代烷基硅烷合成α-手性硅烷的方法(Scheme 1, top left)。同时,Oestreich课题组[2]也报道了使用α-碘代烷基硅烷底物可获得相似结果(Scheme 1, top right)。然而,对于外消旋甲硅烷基化烯丙基底物的相关C(sp3)-C(sp3)交叉偶联反应仅有少数的研究[3](Scheme 1, bottom)。
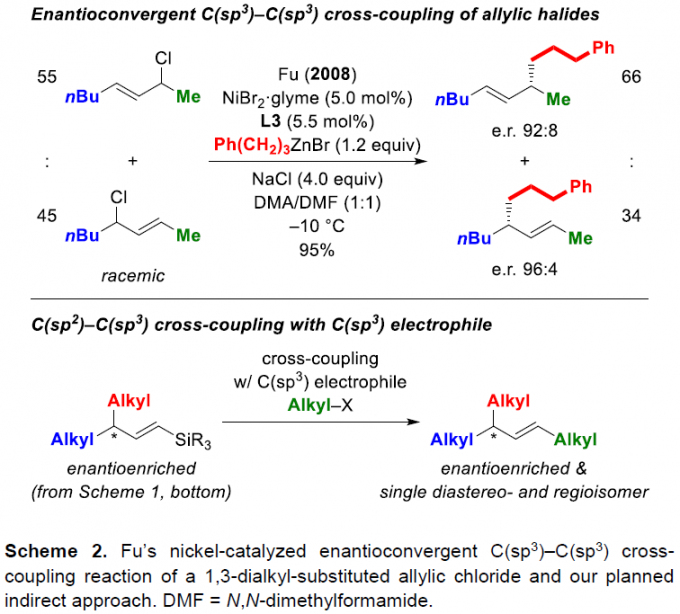
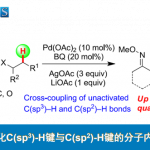
Son和Fu等[4]报道了在NiBr2·glyme和Pybox配体L3(R = CH2Bn)的催化体系下,实现了烯丙基氯化物的Negishi型偶联反应。对于2°和3°烷基以及在烯丙基底物的α和γ位具有一个吸电子基和甲基取代基时,区域选择性一直很高,但对于两个1°烷基区域选择性却中等(Scheme 2, top)。此外,由于叔丁基/甲基具有较高的区域控制能力,并且在过渡金属催化烯丙基反应中,甲硅烷基可控制选择性。因此,作者设想,甲硅烷基化的烯丙基卤化物的区域异构体混合物,偶联反应会选择性发生在具有立体碳中心的乙烯基硅烷上(Scheme 1, bottom)。然后,与C(sp2)碳原子相连的甲硅烷基可作为另一个1°烷基的“占位符”,从而以两步区域选择性合成具有优异非对映和对映选择性的烷基取代无环烯丙基(Scheme 2, bottom)。
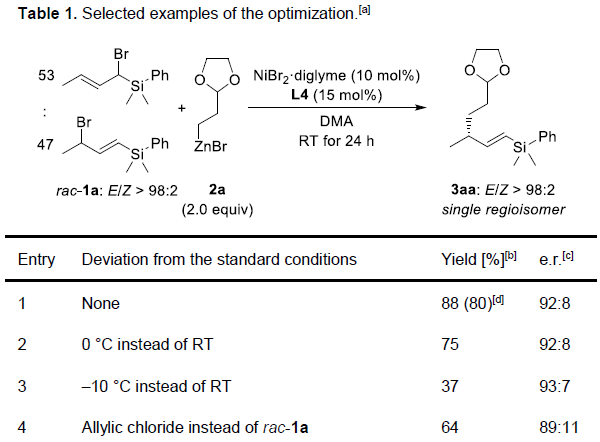
首先,作者以甲硅烷基化的烯丙基溴rac–1a(α:γ= 53:47)和伯烷基溴化锌2a作为模型底物,进行了相关偶联反应条件的筛选(Table 1)。反应结果表明,当NiBr2·diglyme作为前催化剂,Pybox配体L4(R = sBu)作为手性配体,可在DMA溶剂中室温反应,获得80%收率的目标产物3aa,E/Z > 98:2,e.r.为92:8。
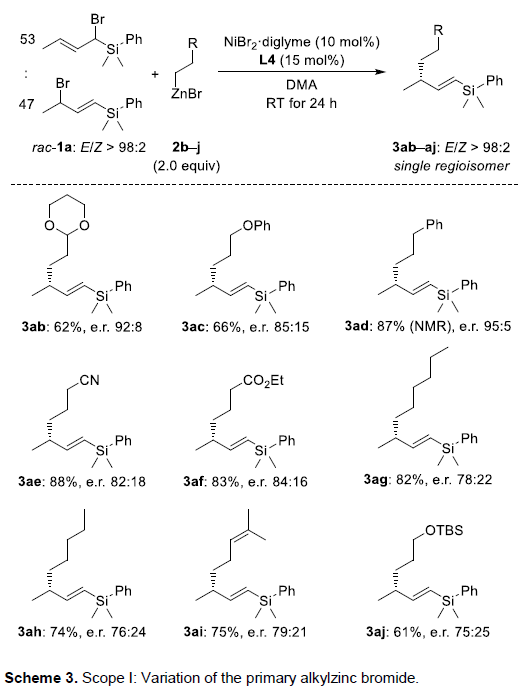
在获得上述最佳反应条件后,作者开始对烷基锌试剂2b-2j进行了扩展(Scheme 3)。反应结果表明,一系列不同取代的底物,如乙缩醛、醚、甲硅烷基醚、苯基、腈、酯、烯基以及未官能化的烷基,均可顺利反应,获得相应的产物3ab–3aj。
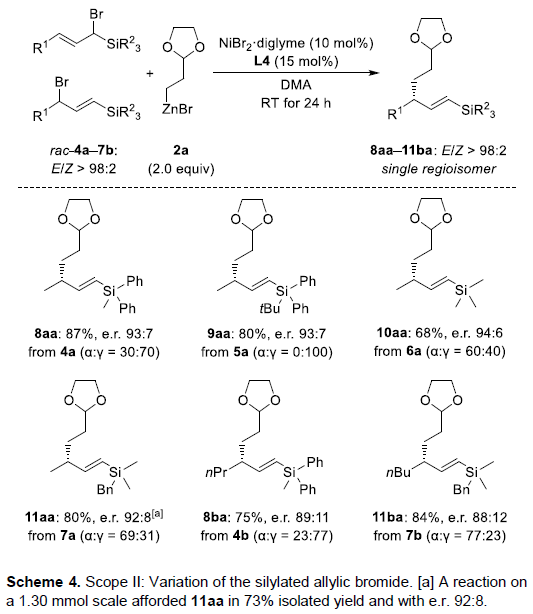
随后,作者对烷基硅底物4a–7b进行了相关的扩展(Scheme 4)。当Me2PhSi基团被空间位阻更大的基团取代(如MePh2Si和tBuPh2Si)以及简单的三有机甲硅烷基Me3Si时,均取得良好的结果,获得产物8aa–10aa。此外,当以MePh2Si和BnMe2Si作为甲硅烷基,作者研究了烯丙基单元的其他取代基,如正丙基和正丁基,均可顺利反应,获得产物11aa、8ba和11ba。然而,在β-位具有甲基的烯丙基溴化学稳定差,既不能通过硅胶快速色谱法纯化,也不能在蒸馏后分离。
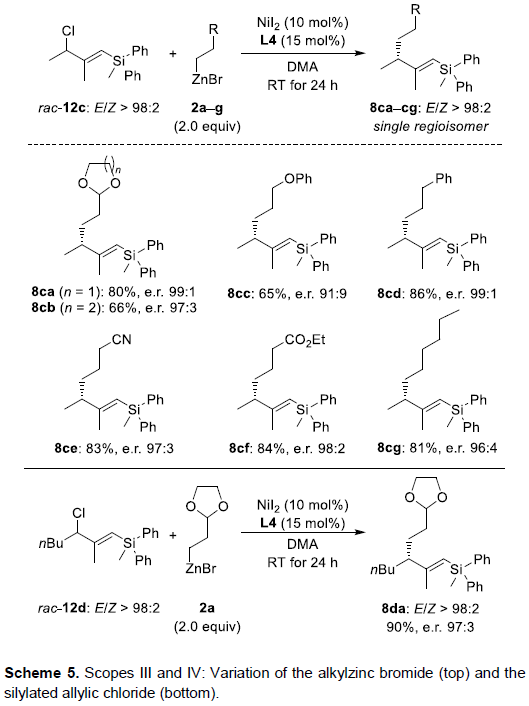
随后,作者将溴代底物改为氯代底物rac–12c,并与不同的烷基锌试剂2a–2g进行反应(Scheme 5)。通过对反应条件的进一步优化,当使用NiI2代替NiBr2·diglyme时,可将收率进一步提高。因此,rac–12c可与2a–2g顺利反应,获得良好收率的目标产物8ca–8cg(Scheme 5, top)。此外,具有更长的烷基链底物rac–12d也可与2a顺利反应,获得90%收率和97:3 e.r.的产物8da(Scheme 5, bottom)。
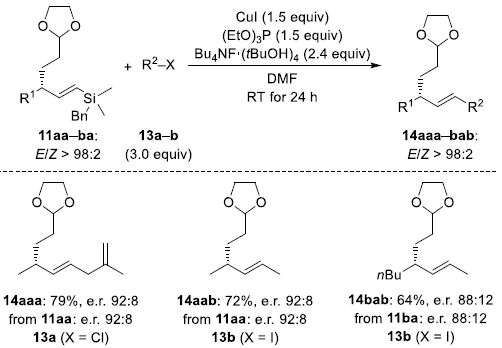
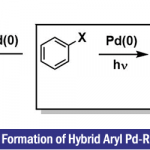
此外,作者使用BnMe2Si取代的烯丙基溴rac–7a和rac–7b与13a和13b进行了反应,从而以高收率生成C(sp2)-C(sp3)偶联产物14aaa–14bab,为单一区域异构体和非对映异构体,且对映体未受影响(Scheme 6)。
总结
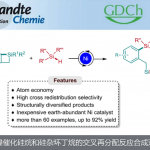
德国柏林工业大学Martin Oestreich课题组报道了一种外消旋α-/γ-甲硅烷基化烯丙基卤化物和烷基锌试剂的不对称发散性镍催化C(sp3)-C(sp3)交叉偶联反应。同时,区域选择性由甲硅烷基控制,该甲硅烷基使键的形成远离硅取代的碳原子。随后,所得的手性E-构型乙烯基硅烷可与亲电试剂偶联,如烯丙基和烷基卤化物。因此,可通过两步合成在烯丙基位具有立体中心的1,3-二烷基取代的无环烯丙基衍生物。





















No comments yet.