三唑并吡啶酮衍生物广泛应用于材料、药物以及农药中,因此该化合物的合成受到化学家们的广泛关注(Fig. 1a)。单取代的三唑并吡啶酮衍生物通常是通过相应的三唑并吡啶并酮与卤化物发生SN2取代反应得到的(Fig. 1b)。但关于合成二取代的三唑并吡啶酮的报道只有两例,且均没有关于合成三取代三唑并吡啶酮衍生物的报道。
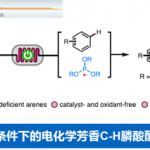
烷基羧酸因其化学性质稳定、方便使用以及结构多样等特性广泛用于Kolbe型电解反应以及经历脱羧生成的烷基自由基或碳基阳离子的偶联反应 (Fig. 1c),但Barton型脱羧反应的原子经济率很低。基于上述背景研究以及浙江工业大学张逢质课题组之前的工作,作者成功开发了无需金属和外源性氧化剂的电化学条件下,烷基羧酸与2-肼基吡啶原位生成的酰肼类化合物经历串联氧化环化和1,2-碳迁移过程可以良好至优秀的收率得到一系列大位阻取代的三唑并吡啶酮衍生物(Fig. 1c)。相关研究成果发表于
“Enantiospecific electrochemical rearrangement for the synthesis of hindered triazolopyridinone derivatives”
Zenghui Ye, Yanqi Wu, Na Chen, Hong Zhang, Kai Zhu, Mingruo Ding, Min Liu, Yong Li, Fengzhi Zhang. Nature Commun. 2020, ASAP. DOI: 10.1038/s41467-020-17389-w
(图片来源于 Nature Commun.)
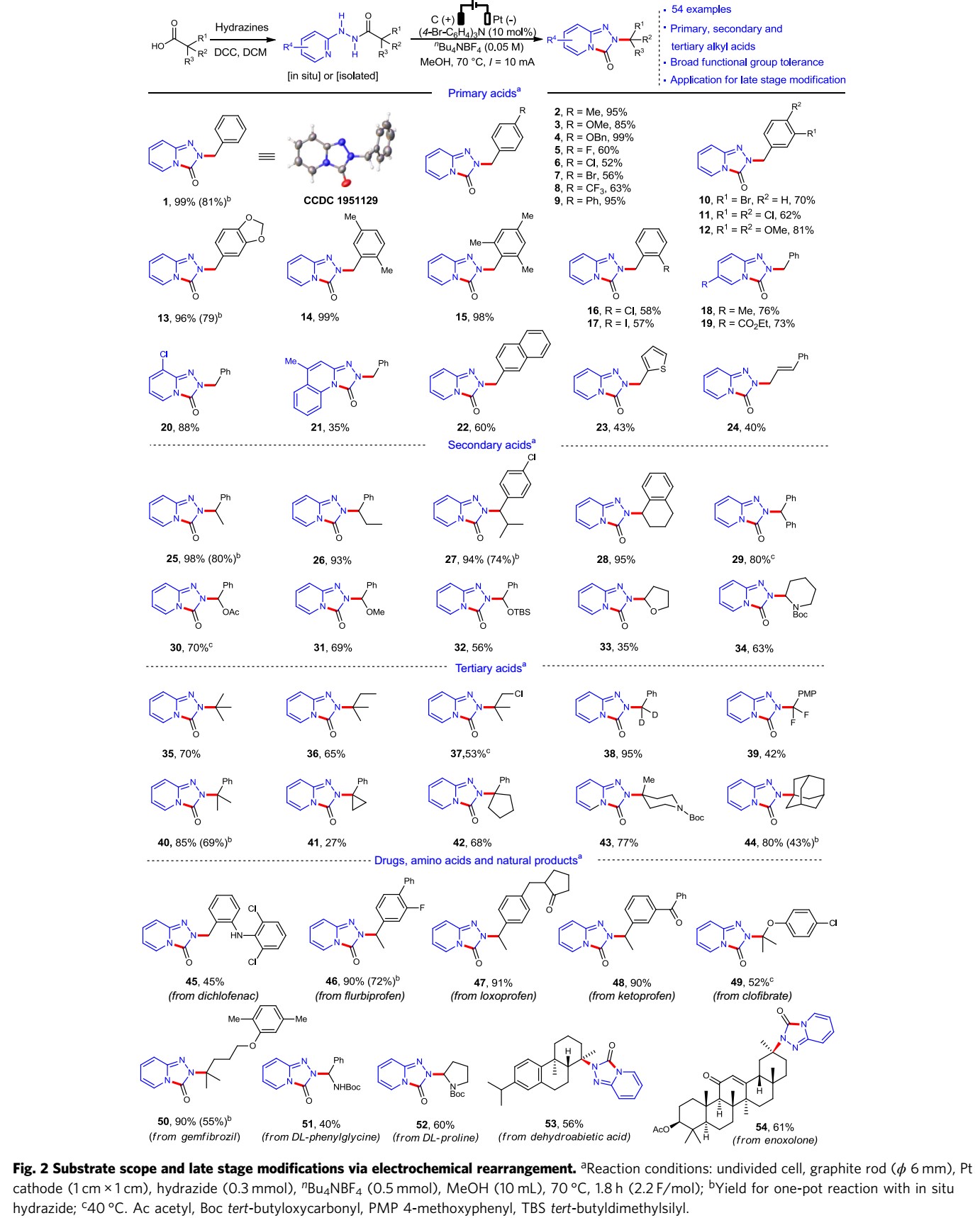
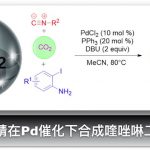
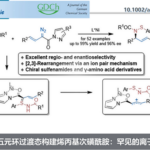
首先,作者以2-苯基乙酸和2-肼基吡啶反应生成的酰肼为模板底物,通过对反应条件的反复筛选,确定最优反应条件(Fig. 2).:石墨为阳极,铂为阴极,10 mol% (4-Br-C6H4)3N为氧化还原催化剂,四氟硼酸四丁基铵为电解质,MeOH为溶剂,在70°C条件下反应1.8 h,能以99%的收率获得所需产物1。紧接着,在最优反应条件下,作者对底物范围进行了考察(Fig. 2)。各种苄基取代、萘基、噻吩以及烯丙基取代的单取代羧酸均能较好的适应反应条件,能以中等至优良的收率得到相应产物。各种烷基以及芳环取代的二取代羧酸也能较好的适应反应条件,能以优良的收率得到相应产物,但α-C-杂环取代的二取代羧酸只能以较低的收率得到相应产物。各种简单的烷基取代、氘代、氟化以及环状取代的也能以较高的收率得到相应产物。同时,作者将这种策略应用于具有药理活性的化合物、氨基酸以及天然产物的合成中。
(图片来源于 Nature Commun.)
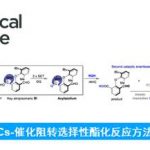
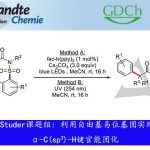
为了证明反应的应用潜力,作者又进行了一系列衍生反应(Fig. 3)。在最优反应条件下,氨基酸以及畅销的药物等手性羧酸能较好的适应反应条件,能以优秀的收率及对映选择性得到相应产物。同时,在最优反应条件下,酰肼61可以70%的收率转化为关键中间体62,再经水解和冷凝过程以97%的收率转化为硬脂酰基辅酶A去饱和酶抑制剂类似物63。紧接着,在标准反应条件下,酰肼64可转化为氯化物65,再与哌嗪化合物66发生偶联反应,合成曲唑酮类似物67。最后,以68为模板底物进行克级反应,该反应同样能以良好的收率和优秀的对映选择性得到相应手性产物(S)-60。
(图片来源于 Nature Commun.)
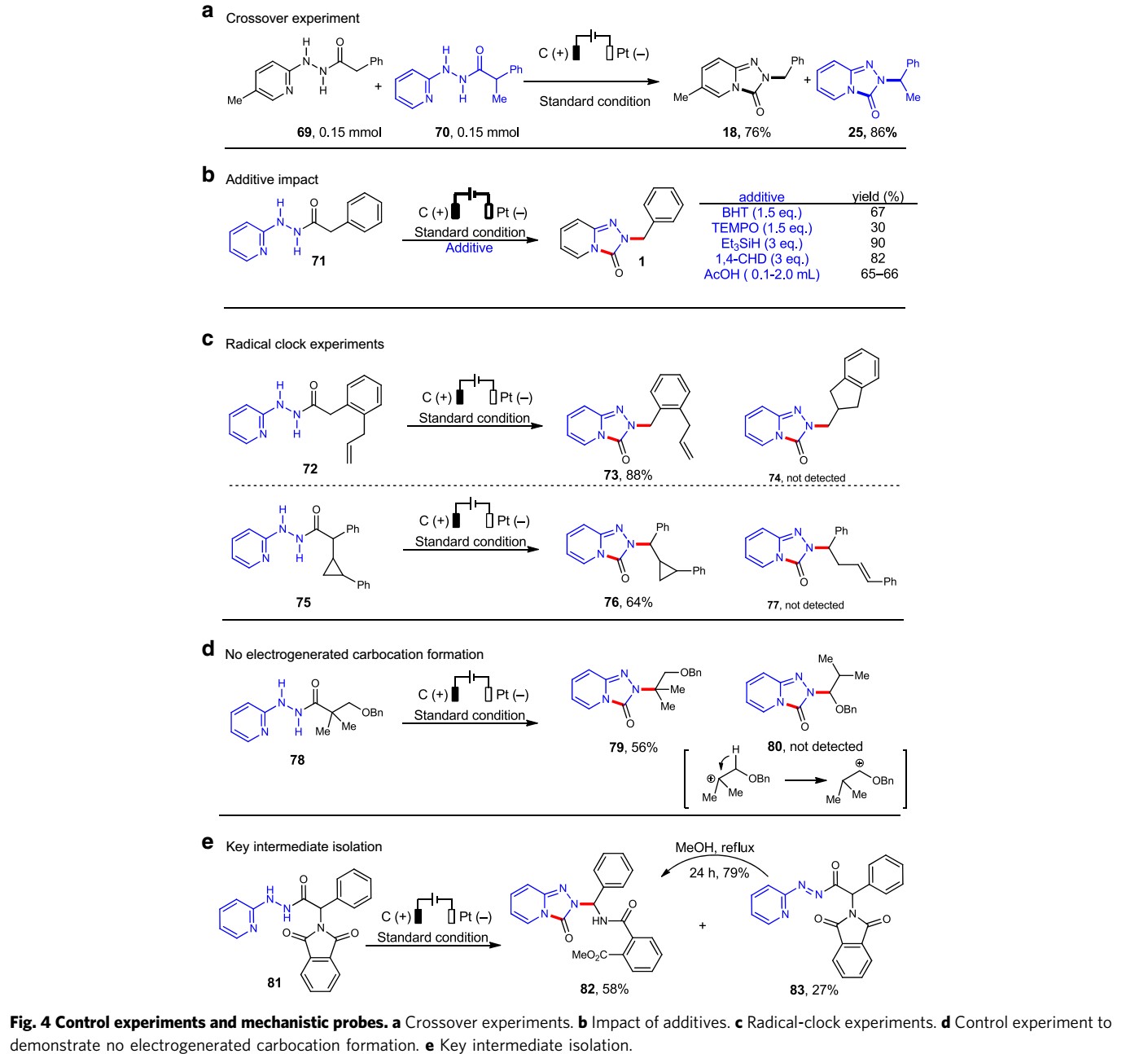
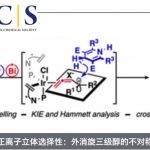
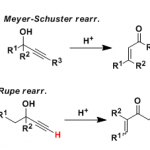
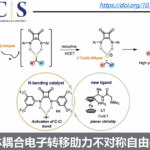
为了更好地研究反应的机理,作者又进行了一系列对照实验(Fig. 4)。首先,以69和70的混合物为模板底物,发现没有混合产物生成。这说明该重排反应必须为分子内反应。在标准条件下加入自由基清除剂(BHT和TEMPO)、H原子供体(三乙基硅烷或1,4-环己二烯)以及乙酸等添加剂,酰肼71仍可转化为相应产物。这说明这些添加剂不会影响反应的进行。作者以72和75为底物进行自由基时钟实验,发现仍能得到重排产物73和76。这说明该反应不涉及自由基过程。紧接着,作者以酰肼78为底物,发现只能检测到环化产物79但未检测出1,2-氢转移产物80。这说明碳正离子可能未参与该重排过程。最后,作者以酰肼81为底物,反应能以27%的收率得到重氮副产物83以及58%的收率得到重排产物82,同时,83在MeOH中回流24 h能以79%的收率得到重排产物82。这说明重排过程可通过重氮中间体发生。基于上述控制实验,作者提出可能的机理:在电化学氧化时,反应中会生成反式-重氮中间体,但该中间体易与顺式-重氮化物相互转化。紧接着,该中间体会发生亲核加成反应和1,2-烷基迁移过程生成相应的环化产物。
(图片来源于 Nature Commun.)
小结
浙江工业大学张逢质课题组成功开发了无需金属和外源性氧化剂的电化学条件下,烷基羧酸与2-肼基吡啶原位生成的酰肼类化合物经历串联氧化环化和1,2-碳迁移过程可以良好至优秀的收率得到一系列大位阻取代的三唑并吡啶酮衍生物。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!


















No comments yet.