近几年来,被称为「超分子聚合物(supramolecular polymers)」的材料作为智能软材料备受瞩目。
“通常的”聚合物(高分子)是由许多单体(momoner: 单体)通过共价键而连接起来形成的,与此相对,超分子聚合物是由单体通过氢键作用或者π—π相互作用等非共价键而结合起来的。
因为是非共价键作用,根据不同条件可能容易回到单体,但是通过一些不可逆的过程,是可以简单合成有秩序的聚合物材料的。因为这些单体所具有的自发形成非共价键的性质使得他们自己组装起来,只需要在适当条件下混合,便可形成聚合物了。
具有这样独特的性质的超分子聚合物,在合成上的问题之一是,长度还有分子量的控制精密合成比较困难。
前一阵、就这个问题,科学家们发现了一类新的精密合成超分子聚合物的方法,解决了这一困扰。是由理研创发物性科学研究中心创发软性物质机能研究组的宮島大吾研究员、相田卓三研究组长(东大院工・教授)和姜志亨研究生(東大院工)、阪大工学研究科的井上佳久教授等人合作研究下、于Science杂志上报道了这一研究。
“A rational strategy for the realization of chain-growth supramolecular polymerization”
Kang, J.; Miyajima, D.; Mori, T.; Inoue, Y.; Itoh, Y.; Aida, T Science 2015, 347, 646. DOI:10.1126/science.aaa4249
那么、究竟如何能够控制超分子聚合物的结构,下面就这一问题的解决办法来做以说明。另外这一次,也顺便对这篇science论文的代表作者之一宮島博士进行了特别专访,从中获得的一些评论,就放在一起给大家介绍一下吧。
- 超分子聚合的精密制御的问题点
共价键的聚合物合成,需要聚合引发剂,反应位点通常仅限聚合物链的末端,所用的单体量的多少就能够决定聚合物的长度及分子量(链增长聚合: chain-growth polymerization)。
而超分子聚合物是各个单体键相互作用开始形成骨架,也就是说单体本身是聚合引发剂,各处引发聚合会同时进行,使得聚合物的长度变异(图1)。因此,超分子的长度以及大小等精密制御合成变得困难。
最近、超分子聚合物的长度及分子量制御合成方法也有手法也有报道,主要是通过控制温度等精密制御来实现的[1]。
- 设计超分子聚合物的精密聚合
构造制御的关键之处和通常的聚合物的链增长聚合相同。
通过研究「聚合引发剂和单体」的关系来完成精密聚合,这样的想法。
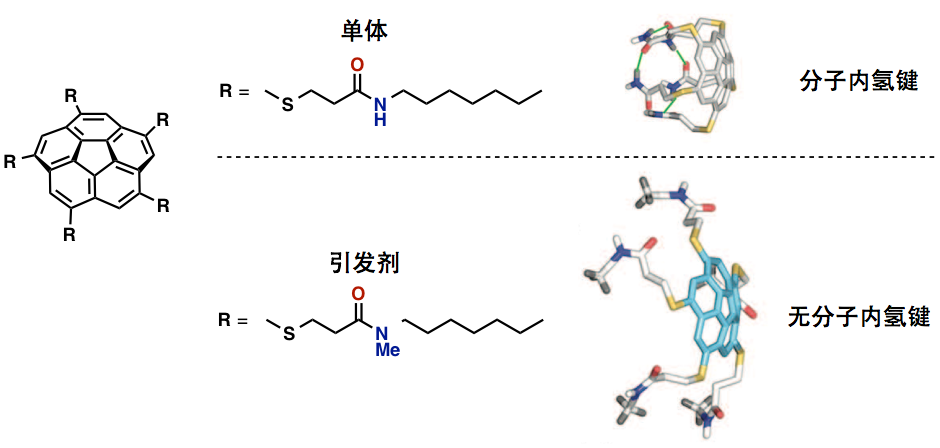
作者们用了含有五个酰胺基的硫烷基侧链的碗状烯烃类似物、这个单体的侧链上含有的酰胺基团能够形成分子内的环状氢键,能够生成单一的稳定的单体并能够抑制分子间的相互作用,从而防止了单体间的自聚。[2] 也就是说和通常的聚合物合成的单体是相同的状态,被称为“亚稳态单体”(图2上)。
「亚稳态单体」的聚合需要聚合引发剂,这次,作者设计了单体侧链N原子甲基化的分子作为聚合物引发剂。(图2下)。
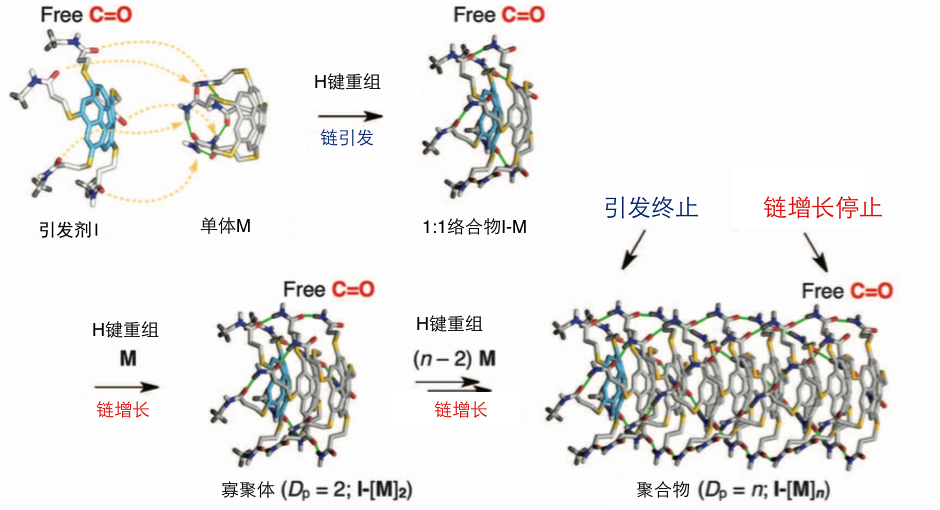
聚合物引发剂、由于甲基化而不会发生分子内氢键作用,也就是说,保持了聚合反应所用的羰基部分,由于甲基化阻止了分子内氢键作用使得分子呈延展状的结构,即具有聚合活性的羰基作为能够发生反应的(作为氢受体)状态而存在。然后与亚稳态单体混合,引发剂的羰基与亚稳态单体之间通过分子间氢键作用生成二聚体,紧接着,再次暴露出来的新的羰基与新的亚稳态单体反应,通过这样进行聚合反应(图3)。当然聚合物链末端的引发剂因为甲基化活性降低,生成的聚合物链之间也就不会发生偶联反应。
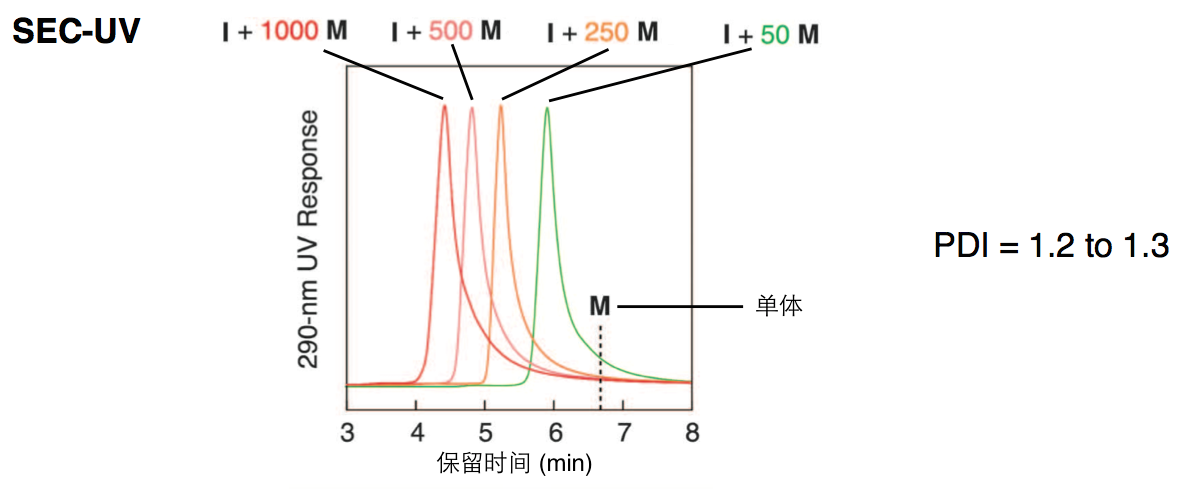
单体之间的反应得到了很好地控制,只在聚合链末端产生聚合反应活性物种,对聚合链的长度也能够很好地控制,在对引发剂50当量至1000当量的单体聚合反应中,对所得聚合物的PDI(分子量分布)测定,基本都保持在较低的程度1.2到1.3左右,说明对分子量的控制也成功实现(图4)。
- 光学活性超分子聚合物
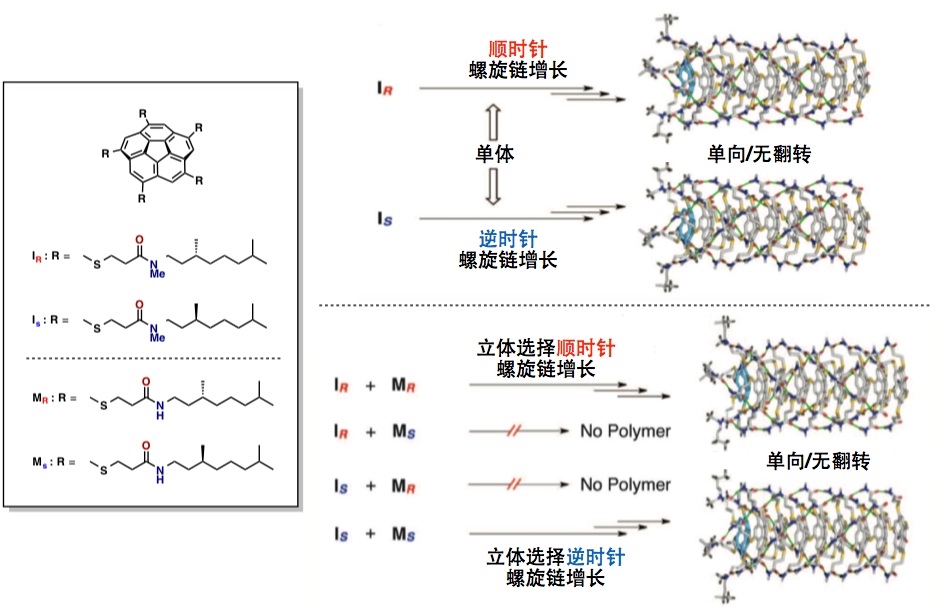
生成的超分子聚合物有单体以螺旋状的方式叠加起来,若使用在侧链引入手性结构的聚合引发剂,这个螺旋构造的方向会向着一个方向叠加(图5上)。
还有、聚合引发剂与单体都就与手性结构式,因为若不按照手性一致的方式组合,聚合反应就不会发生(图5下),通过这一个原理,对外消旋的单体与手性引发剂作用,则会实现手性拆分。
通过共价键连接的聚合物通常是很难实现高的立体选择性的,这次的超分子聚合物中是以较高的选择性来进行,关于这一点,在下面的笔者评论部分给大家介绍一部分。
「这样高的选择性的出现,在发展比较成熟的高分子化学研究中倒不是件容易的事。而超分子化学是通过多位点的弱相互作用使得分子间能够稳固的连接起来。单体的分子内氢键打开,为了聚合反应的进行,需要多个分子内氢键同时转变为分子间氢键。一个位点出错了倒是有可能,但是这么多个位点同时出差错则难于发生,所以在结果上会实现很高的选择性。还有一个一个都是比较弱的相互作用,结合错误也能简单矫正,这也是超分子科学的特征之一。这一特征与生物材料的高选择性・可复制性在本质上是相同的。」
这样以来,也让人们感慨超分子的独到之处。
以上、就是由亚稳态单体和引发剂作用的超分子聚合物的精密合成法的介绍。不光是控制了聚合物的长度,也实现了单体手性拆分的的选择性合成以及光学活性的聚合物合成。
亚稳态单体与引发剂分子的试剂虽然不容易,但在今后的研究中,还是会继续努力并期待着能够合成出更多其他的超分子聚合物。
- 来自研究作者的意见
最后附上有作者们那里收获到的评论观点以及他们的照片给大家做个简单介绍。
「精密制御超分子聚合」——是我们一直以来的梦想
这个研究中最难得应该就是如何证明是「分子量均一的超分子聚合物」。在这以前,超分子聚合物的大小的评价表征、都是通过透射电子显微镜(TEM)还有原子力显微镜(AFM)直接计算的。但是,通过这种方法得到的信息只是非常局限的一部分聚合物的信息,我们当时只能通过分子(空间)排阻色谱(SEC)来解析,这是评估高分子的标准方法,相比起能消除随意性,它的优点更在于能适用于多种聚合物的评价。
另一方面,这个测定的问题在于,用于分析的色谱柱内难免会发生超分子聚合物链的切断、分解等现象。因为超分子聚合物是单体之间的非共价键结合,它的稳定性与溶剂的类型有很大关系,遗憾的是SEC所用的溶剂会使大多超分子聚合物分解成单体。我们只能对色谱柱的种类,溶剂组成、流速、实验温度等进行彻底的优化,并且重复性较好的聚合物才能通过SEC解析,仅仅优化分离条件就得花至少两周,而且这个SEC测定再加上动态光散射(DLS)测定,圆二色性(CD)等等组合起来的证据,才让我们有足够的自信把论文投出去了,可是审稿编辑中的一位要求我们做进一步分析。
拿到这个意见后只能接受现实,并且静下来想想,SEC測定・DLS測定・CD測定、这些都是间接的评价方法,果然我们还是是需要显微镜给出的超分子链长短表征的直接证据,就这样重新来了一遍。在投稿的论文中把原子力显微镜的解析结果加上,还有NMR表征的扩散系数的结果也加上,虽然在追加实验补充数据花了一些时间,但是让我们的研究(论文)的质量又上升了一个高度,现在的话,反倒还要多谢当时给我们提这意见的那位审稿编辑。
这个研究总体说来还是进展挺快的,这篇论文的第一作者姜志亨同学功劳非常大,如果没有他,这个研究的开始可能都不可能。姜(同学)是非常优秀的大学院生,利用计算机科学对分子间相互作用的解析;另外观测到的圆二色性的理论解析则得到了大阪大学的森 直老师、井上佳久老师、还有东京大学伊藤善光助教很大的帮助,借此机会感谢他们的贡献。
超分子聚合的精密制御合成实现了会怎么样呢?这是我们多年以来一直思考的问题,有许许多多好的想法,也出了一些比较有意思的成果。把超分子化学的优点还有高分子化学至今以来所积累的知识相结合,希望能够在新的化学领域有所突破。
最后了,再提一下我们研究所物质材料研究机构(NIMS)的杉安和憲主任研究员・竹内正之组长等人去年在超分子聚合物长度制御合成的研究(发表在Nature Chemistry Nat. Chem.6, 188–195, 2014)。他们是巧妙利用了速度论的生成物和热力学生成物的稳定性来研究,也是一篇非常有意思的论文。和我们的论文做个比较的话,他们更接近超分子化学的视点来解决这一问题,而我们则更侧重高分子化学的角度,还是有所区别的。
理化学研究所 宮島大吾
[1] Ogi, S.; Sugiyasu, K.; Manna, S.; Samitsu, S.; Takeuchi, M. Nat. Chem. 2014, 6, 188. DOI:10.1038/NCHEM.1849 [2] Kang, J.; Miyajima, D.; Itoh, Y.; Mori, T.; Tanaka, H.; Yamauchi, M.; Inoue, Y.; Harada, S.; Aida, T.J. Am. Chem. Soc.2014, 136, 10640. DOI:10.1021/ja505941b
- 参考文献
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!