2017年、阿尔伯塔大学・Dennis G. Hall课题组、着眼于利用细胞毒性小的硼酸与二醇反应形成硼酸酯、再与腙的形成进行组合,形成不可逆的复合体的手法,成功应用在了活细胞的共轭正交反应上。
“Synergic “Click” Boronate/Thiosemicarbazone System for Fast and Irreversible Bioorthogonal Conjugation in Live Cells”
Akgun, B.; Li, C.; Hao, Y.; Lambkin, G.; Derda, E.; Hall, D. G.* J. Am. Chem. Soc. 2017, 139, 14285. DOI: 10.1021/jacs.7b08693
需要解决的问题点
使用毒性低的试剂在细胞内进行生物正交反应,是用于理解生物体分子在细胞内功能的一种很有效的手段。特别是在低浓度・水系溶剂中显示出高反应性・选择性、没有副产物生成,并且收率高的Click chemistry,是目前该领域关注度最高的。
Hall课题组也是瞄准这类反应,报道了基于硼酸酯形成的新型生物正交反应的开发[1]。在该反应中,尽管nopoldiol衍生物与2-甲基-5-羧甲基苯基硼酸形成的硼酸酯的稳定性高,然而由于在水中会发生逆反应,成为了这个反应的一个需要改善的问题(下图)。
具体手法
作为改善的思路,作者重点关注生物正交反应中使用的亚胺·腙·肟形成、作者认为可以通过使用它作为第二种协同相互作用来合成更稳定的复合物,并优化试剂骨架。
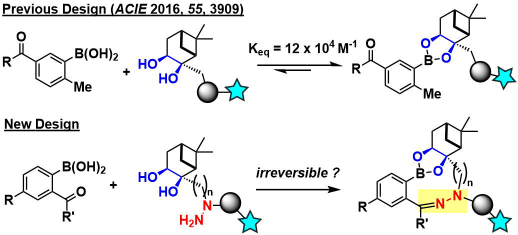
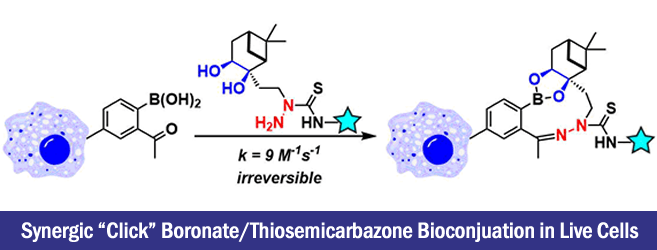
将二醇结构固定在nopodiol上、然后作者进行了用于各种C = X键的相互作用位点结构的组合研究。有报道表明氨基硫脲比邻位带有甲基酮的硼酸,苯肼的稳定性,安全性更高[4],因此作者以此为启发,得到了在nopodiol的两个碳linker上连接有如标题图所示结构的最佳化合物。该反应在50 μM浓度下3.5小时以内就能得到定量的复合体。
主张的有效性验证
①在生物体内环境下复合体的稳定性确认
硼酸+二醇氨基硫脲配置成复合体后,再加入过量的其他硼酸,放置数天后,并没有观察到硼酸的交换。稀释条件,对pH3以及9的buffer稳定,没有观察到复合体的解体。
②反应的生物正交性验证
多元醇结构存在于各种生物分子中,最常见的有糖类化合物。在葡萄糖(8 mM)、果糖(300μM)、或儿茶酚(0.1 μM)存在下,进行硼酸+二醇氨基硫脲试剂的络合物形成、反应结果没有变化。 由此可见,生物多元醇不会影响反应。
另外,通过蛋白质的翻译后修饰导入酮或者醛结构的研究近年来也有报道[3][4]。利用可以模仿该结构的乙醛醛作为底物,用二醇缩氨基硫脲试剂尝试进行作用,结果没有发现缩氨基硫脲的形成。
③向活细胞应用的可能性
作者对每种试剂进行了细胞毒性试验,在与反应时间(18小时)相当的试验时间内没有观察到显著的毒性。
然后、再HEK293T细胞表面利用SNAP-tag法对硼酸进行固定,进行荧光素缀合的二醇氨基硫脲试剂反应。然后通过荧光显微镜观察后发现细胞表面被荧光标记。代之以使用缺乏二醇的氨基硫脲(thiosemicarbazide)试剂、由于没有观察到表面荧光、事实证明,这两种协同反应对标记都是不可或缺的。
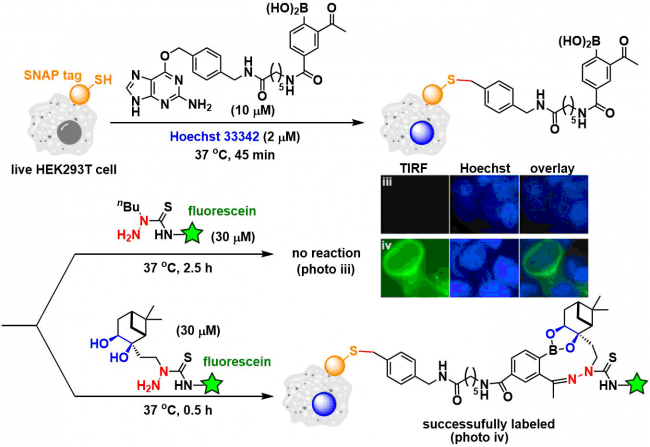
Comment
- PBS buffer、37℃这样的非常温和的条件下进行,不需要金属参与是其比较大的优势。
- 虽然它是算生物正交反应,但需要引入非天然氨基酸来修饰蛋白质。目前,从天然氨基酸转换为硼酸将是非常困难的的。如果要拓展应用性,还需要寻找更简单的结构。
次に読むべき論文は?
- 在细胞内进行化学反应的实例[5][6]。这次的论文虽然停在了细胞表面的修饰,如果能有一些在细胞内如何能实现,能应用的idea的话可能会更有意思。
参考文献
- Akgun, B.; Hall, D. G. Angew. Chem., Int. Ed. 2016, 55, 3909. doi:10.1002/anie.201510321
- Bandyopadhyay, A.; Cambray, S.; Gao, J. J. Am. Chem. Soc. 2017, 139 , 871. DOI: 10.1021/jacs.6b11115
- Matthews, M. L.; He, L.; Horning, B. D.; Olson, E. J.; Correia, B. E.; Yates, J. R.; Dawson, P. E.; Cravatt, B. F. Nat. Chem. 2017, 9, 234. doi:10.1038/nchem.2645
- Prescher, J. A.; Bertozzi, C. R. Nat. Chem. Biol. 2005, 1, 13. doi:10.1038/nchembio0605-13
- Agarwal, P.; Beahm, B. J.; Shieh, P.; Bertozzi, C. R. Angew. Chem. Int. Ed. 2015, 54, 11504. doi:10.1002/anie.201504249
- Li, S.; Wang, L.; Yu, F.; Zhu, Z.; Shobaki, D.; Chen, H.; Wang, M.; Wang, J.; Qin, G.; Erasquin, U. J.; Ren, L.; Wang, Y.; Cai, C. Chem. Sci. 2017, 8, 2107. doi:10.1039/C6SC02297A
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



















No comments yet.