概要
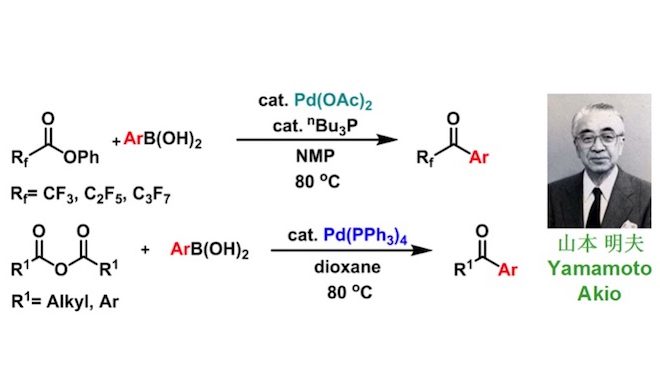
1995年,日本早稻田大学(Waseda University)的山本明夫(Yamamoto Akio)研究室报道了钯催化剂促进的酸酐C-O键活化过程。2001年,该课题组将这一过程应用于全氟羧酸酯与有机硼化合物之间发生交叉偶联反应,成功获得对称及非对称芳酮类化合物,2002年,该课题组又将反应底物扩展至羧酸酐。 这两类反应统称为Yamamoto酮合成(Yamamoto ketone synthesis)。同时,该课题组对其它有机硼化合物进行了研究,表明四苯硼酸钠同样适用于该反应。
目前,该反应主要应用于各种全氟烷基芳酮、对称及非对称芳酮类化合物的合成。
基本文献
- K. Nagayama, F. Kawataka, M. Sakamoto, I. Shimizu, A. Yamamoto, Chem. Lett. 1995, 367. doi: 10.1246/cl.1995.367.
- K. Nagayama, F. Kawataka, M. Sakamoto, I. Shimizu, and A. Yamamoto, Bull. Chem. Soc. Jpn., 1999, 72, 573. doi: 10.1246/bcsj.72.573.
- A. Yamamoto, Adv. Organomet. Chem., 1992, 34, 111. doi: 10.1016/S0065-3055(08)60016-7.
- K. Nagayama, F. Kawataka, M. Sakamoto, I. Shimizu, A. Yamamoto, Chem. Lett., 1995, 367. doi: 10.1246/cl.1995.367.
- R. Kakino, I. Shimizu, A. Yamamoto, Bull. Chem. Soc. Jpn. 2001, 74, 371. doi: 10.1246/bcsj.74.371.
- R. Kakino, I. Shimizu, A. Yamamoto, Bull. Chem. Soc. Jpn., 2002, 75, 137. doi: 10.1246/bcsj.75.137.
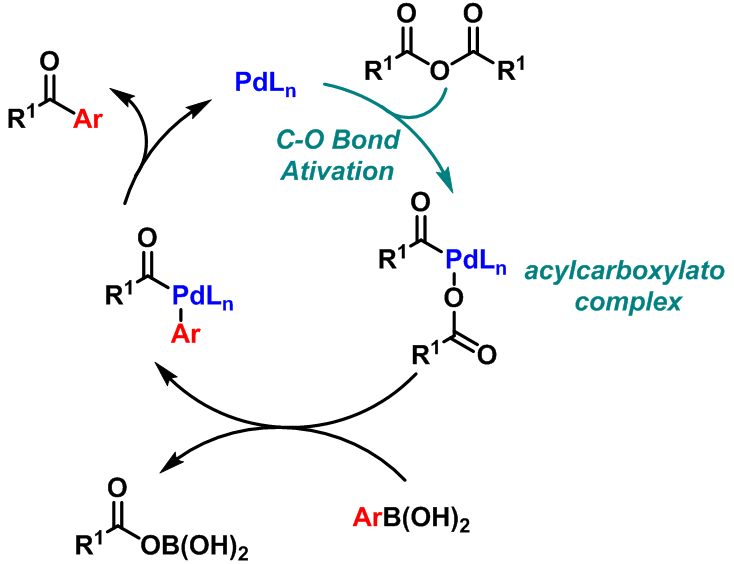
反应机理
- T. Yamamoto, K. Sano, K. Osakada, S . Komiya, A. Yamamoto, Y. Kushi, T. Tada, Organornetallics 1990, 9, 2396. doi: 10.1021/om00158a041.
- K. Osakada, M.-K. Doh, F. Ozawa, A. Yamamoto, Organometallics 1990, 9, 2197. doi: 10.1021/om00158a010.
- T. Yamamoto, K. Igarashi, J . Ishizu, A. Yamamoto, J. Chem. Soc., Chem. Commun. 1979, 554. doi: 10.1039/C39790000554 .
反应实例
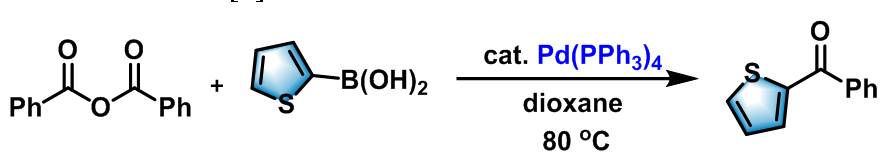
非对称酮的合成[1]
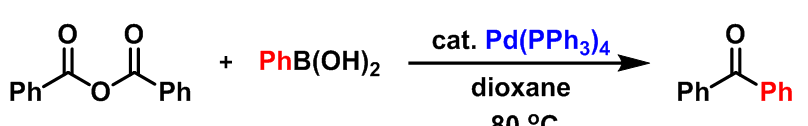
对称酮的合成[1]
三氟甲基酮的合成[2]
实验步骤
全氟烷基芳酮的合成:将Pd(OAc)2的NMP溶液(催化剂浓度为0.01 M,0.05 eq.)、三正丁基膦(0.15 eq.)三氟乙酸苯酯(1 eq.)及芳基硼酸(1.22 eq.)装入Schlenk管中。 氩气气氛下,将上述反应混合物在80°C下加热,直至反应结束。反应结束后,将反应液冷却,加水稀释后,再加入乙醚进行萃取。将合并的乙醚相采用无水MgSO4进行干燥,并在减压条件下除去溶剂。将粗产物采用硅胶柱色谱(正己烷/Et2O = 9:1 v/v)进行分离纯化后,获得相应全氟烷基芳酮类化合物。
芳酮的合成:将Pd(PPh3)4的二噁烷溶液(催化剂浓度为0.0042 M,0.02 eq.)、羧酸酐(1 eq.)及芳基硼酸(1.20 eq.)装入Schlenk管中。 氩气气氛下,将上述反应混合物在80°C下加热,直至反应结束。反应结束后,将反应液冷却,加水稀释后,再加入乙醚进行萃取。将合并的乙醚相采用无水MgSO4进行干燥,并在减压条件下除去溶剂。将粗产物采用硅胶柱色谱(正己烷/Et2O = 9:1 v/v)进行分离纯化后,获得相应芳酮类化合物。
实验技巧
参考文献
- R. Kakino, I. Shimizu, A. Yamamoto, Bull. Chem. Soc. Jpn., 2002, 75, 137. doi:10.1246/bcsj.75.137.
- R. Kakino, I. Shimizu, A. Yamamoto, Bull. Chem. Soc. Jpn. 2001, 74, 371. doi: 10.1246/bcsj.74.371.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



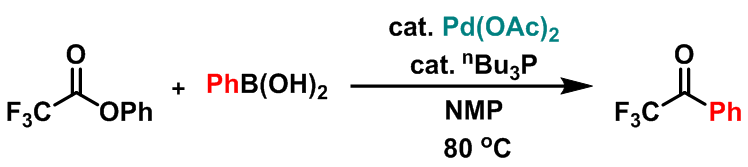














No comments yet.