作者:杉杉
导读:
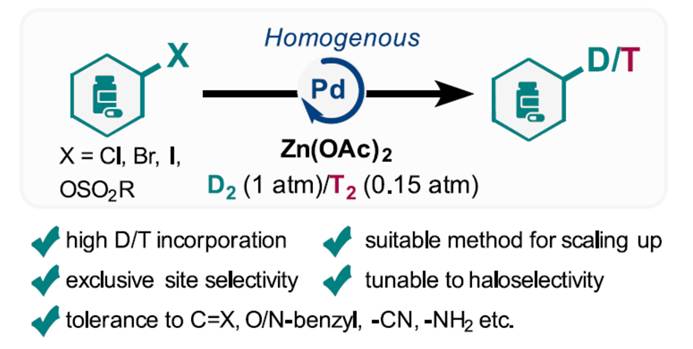
近日,美国默克公司的Jingwei Li与Qiao Lin团队在J. Am. Chem. Soc.中发表论文,报道一种使用Zn (OAc)2作为添加剂的新型钯催化体系,该体系能够使用D2/T2气体实现新型的均相脱卤氘代与氚代反应。在温和的反应条件下,一系列药物相关的芳基卤和拟卤化物均可进行选择性氘代反应。该反应显示出与各种官能团的优异相容性,包括多键、O/N-苄基与氰基,这些官能团具有一定的反应活性,因此在Pd/C催化体系中常常参与反应。此外,该方法已成功应用于四种卤代药学相关分子的氚代反应,导致每个卤素原子具有可预测的高比活度 (specific activity,SA)。值得注意的是,该反应还可用于含氘中间体的克级制备,这是合成氘标记药物分子的关键步骤。此外,作者提出了一种关键中间体结构Pd(Ar)OAc,用于在脱卤氘代与氚代过程中活化氢气。同时,Zn(OAc)2在抑制卤化物对钯的中毒中起着至关重要的作用。
Homogenous Palladium-Catalyzed Dehalogenative Deuteration and ritiation of Aryl Halides with D2/T2 Gas
J. Li, Q. Lin, O. Dungan, Y. Fu, S. Ren, S. Ruccolo, S. Moor, E. M. Phillips, J. Am. Chem. Soc. 2024, ASAP. doi: 10.1021/jacs.4c08176.
正文:
氢同位素标记的化合物在各个领域均具有广泛的用途,特别是可以应用在制药行业的药物发现与开发中(Scheme 1A)。首先,氘标记化合物已被广泛用于反应机理研究。其次,氘代药物分子在医学化学中作为潜在的新型候选药物具有巨大的前景,如FDA批准Deutetrabenzaine与Deucravacitinib。与含抗氧化剂的药物分子相比,选择性地将氘掺入药物分子的特定代谢“软点”可能有利于其药代动力学与毒性特征。此外,氘标记的内标与氚标记的放射性示踪剂,仍然是临床前与临床研究中检测与定量药物以及药物代谢物的最有效方法。因此,开发一种高效、经济、选择性的合成方法来制备氢同位素标记的化合物至关重要。
合成氢同位素标记化合物有两种主要方法:(1)氢同位素交换(HIE)与(2)还原氘代或氚代反应。HIE特别有吸引力,因为它允许在后期将同位素快速直接掺入活性药物成分(API)中[1]。然而,HIE存在官能团耐受性差、缺乏选择性与可预测性、同位素掺入不完全以及需要导向基团等弊端,从而限制了相关的应用(Scheme 1B)。相比之下,还原氘代或氚代作为一种补充的方法,由于未标记前体中不饱和键或卤素原子的预定位置,提供了独特的位点选择性与可预测的比活度。虽然引入这些前官能团可能需要从头合成,但芳基卤的后期官能化(LSF)已经得到了很好的发展,使这些前体更容易获得[2]。因此,相应芳基卤的脱卤氚代已成为制备氚标记化合物最常用的方法之一。
芳基卤的脱卤氘代或氚代通常使用非均相钯催化剂(Pd/C)以及氘与氚气体(Scheme 1C)。然而,尽管这种方法具有广泛的实用性,但存在两个局限性。首先,在某些可还原官能团(如烯基、炔基、N/O-苄基、氰基与硝基)存在的情况下,非均相催化体系可能无法选择性地进行芳基卤的脱卤,这大大限制了底物的范围。其次,观察到氚代产物中比活度按ArI > ArBr > ArCl的顺序呈降低的趋势。同时,当需要高比活度氚标记示踪剂时,通常需要制备多碘前体。因此,开发一种有效与化学选择性的芳基卤的脱卤氘代与氚代,特别是使用D2/T2气体作为同位素源以及芳基溴与氯为底物,是非常可取的。
作者设想,一个均匀的钯体系将有可能解决这些问题。关键的挑战是钯不能同时活化氢气与Ar−X键。Ritter课题组报道了一种均相钯催化芳基噻鎓蒽盐(TT+)盐与D2/T2气体的开创性氘代与氚代反应[3]。这种开创性的方法通过形成阳离子钯中间体,显著提高了钯对D2/T2的反应性(Scheme 1D)。虽然这种方法非常有利,但它受到噻鎓蒽基团体积大与原子经济性低的限制。此外,这些条件下对芳基卤也缺乏反应性。这里,美国默克公司的Jingwei Li与Qiao Lin团队报道一种均相钯催化芳基卤与D2/T2气体的脱卤氘代与氚代反应(Scheme 1E)。该方法与各种官能团表现出显著的相容性,包括多键、O/N-苄基与氰基。在传统的HIE或Pd/C脱卤条件下,这些官能团通常是不耐受的。机理研究表明,氢活化不是通过钯阳离子发生的,而是通过Pd(Ar)OAc发生的,它模拟了协同金属化-去质子化(CMD)途径,而没有配体解离。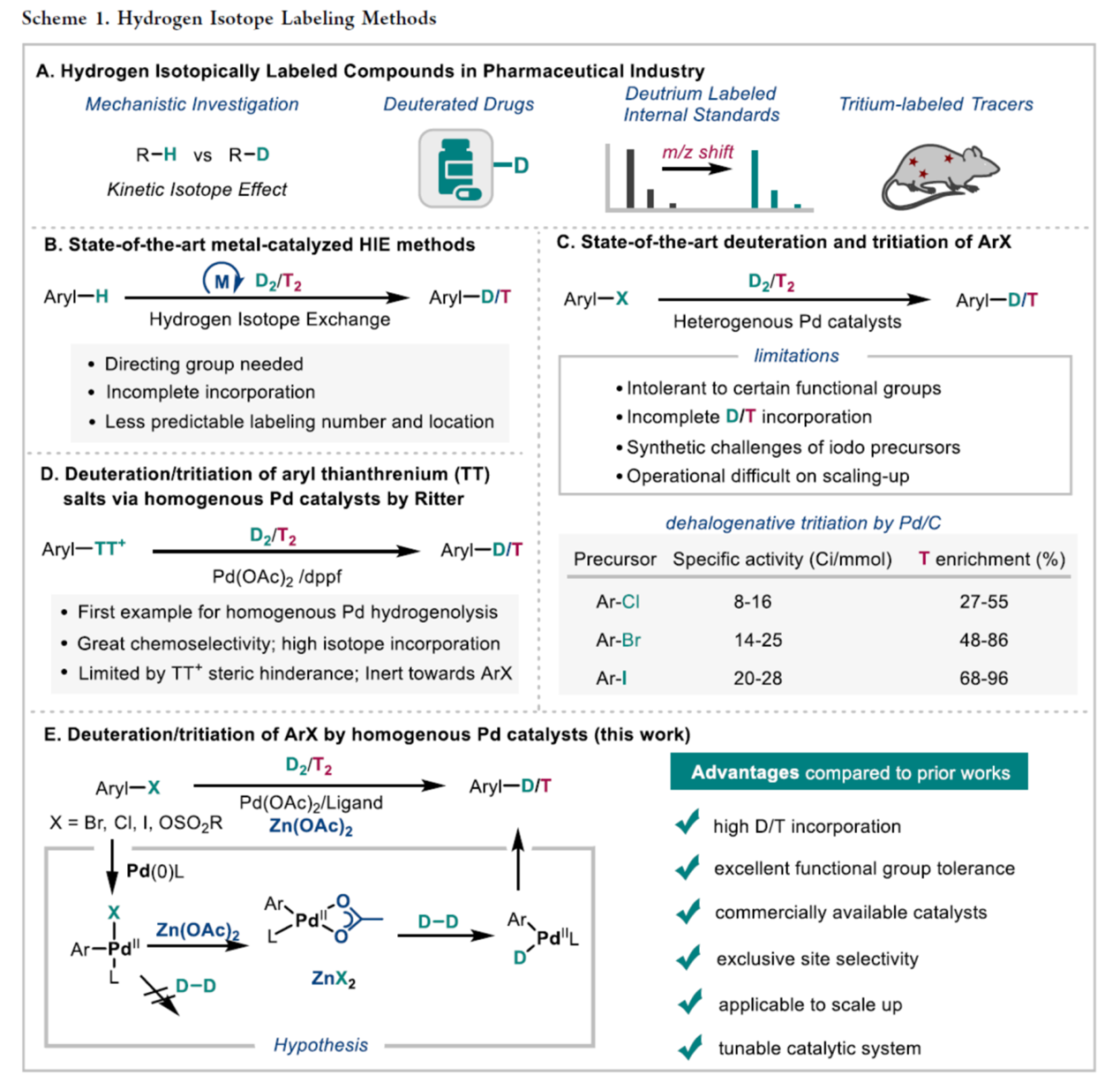
首先,作者采用N-(4-溴苄基)-N-环己基苯甲酰胺(1a)作为模型底物,进行相关反应条件的优化筛选 (Figure 1)。进而确定最佳的反应条件为:采用D2(1 atm)作为氘源,PdCl2(amphos)2作为催化剂,Zn(OAc)2作为添加剂,在DMAc反应溶剂中,反应温度为室温,最终获得100%收率的产物1b(>99% D)。同时,若采用N-(4-氯苄基)-N-环己基苯甲酰胺(2a)作为模型底物,需以Pd(OAc)2作为催化剂,L1作为配体,Zn(OAc)2作为添加剂,同样可获得100%收率的产物1b(>99% D)。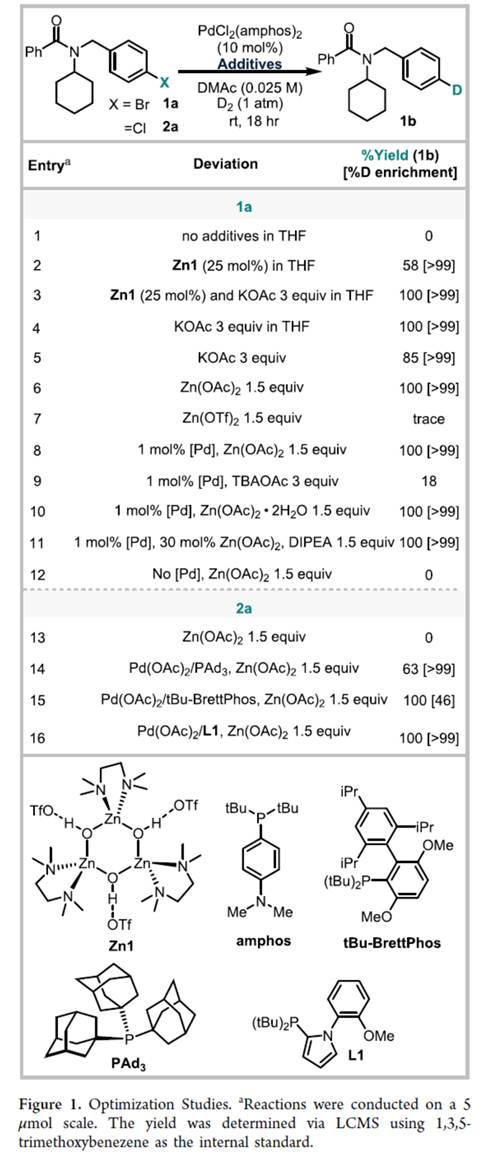
在上述的最佳反应条件下,作者底物的应用范围进行深入研究 (Scheme 2)。首先,带有吡啶基、吲哚、噻吩与嘧啶等杂芳环取代的溴化物以及芳基取代的溴化物(3–13),均可顺利进行反应,可以高收率得到相应的产物。值得注意的是,对还原条件敏感的官能团,如烯基、O-苄基、N-苄基与氰基,均可耐受。其次,对于同时含有溴与氯的底物,通过调整催化剂负载量与反应时间,实现了选择性的脱溴反应,如14b与15b。芳基氯衍生物(16与17),也能够顺利进行反应,具有高收率。此外,该反应也同样适用于芳基碘或拟卤化物(18与19),。含有α,β-二酮单元(20)与α-吡啶基卤化物(22)的底物在标准条件下的转化率较低,这可能是由于它们的螯合特性。然而,将配体从L1切换到L2分别显著提高了20与22的产率,前者从小于10%提高到94%,后者从40%提高到70%。该方法的当前局限性是对含有炔基环烷基(21)的底物进行脱氯,这意外地导致了过度还原与开环的副产物的生成。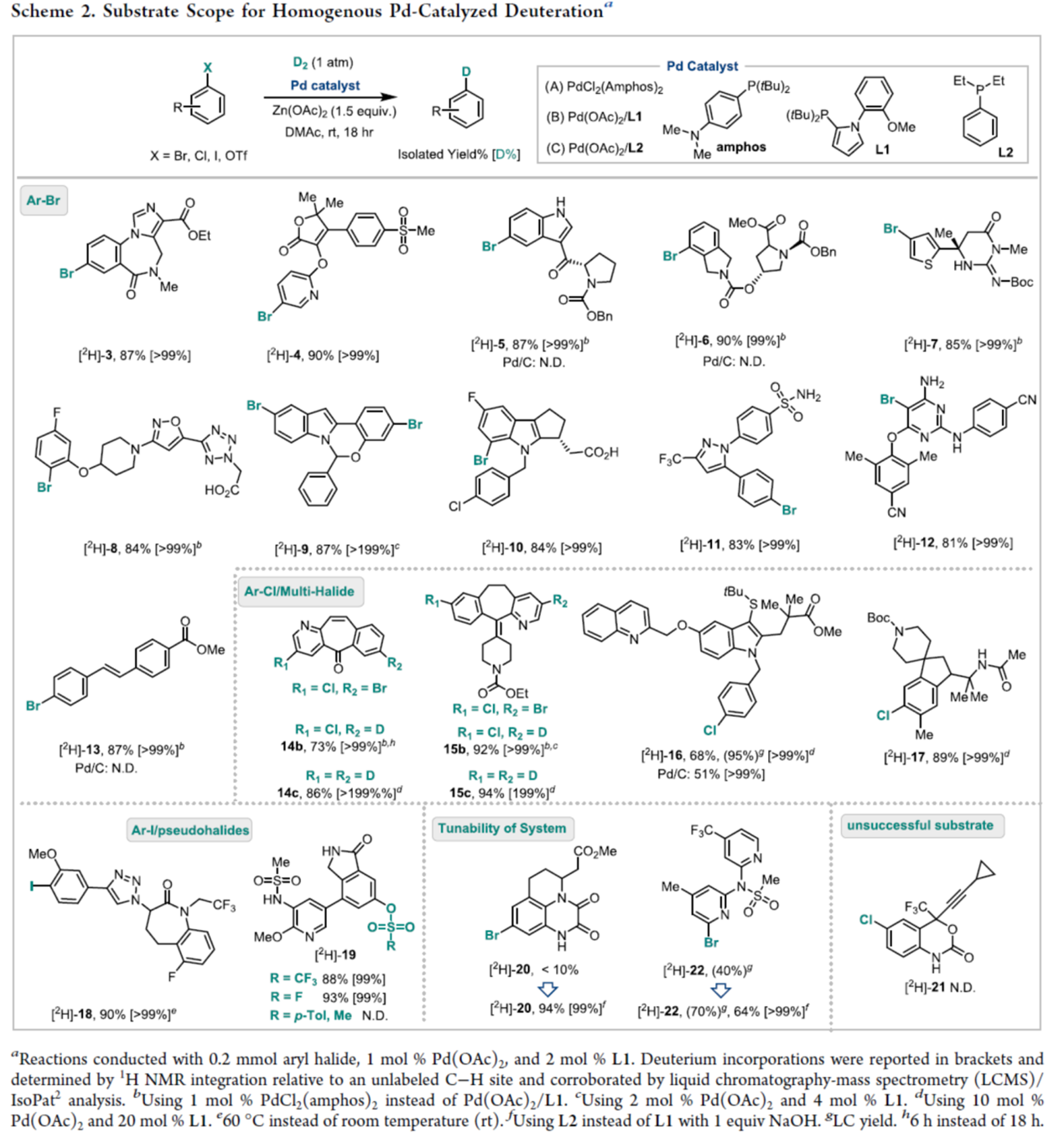
随后,作者对均相钯催化药物分子的脱卤氚代反应的范围进行了扩展(Scheme 3)。研究结果表明,Br-TAK875、Br-MK-4618、Br-MK-4305与溴氯雷他定衍生物,均可顺利进行反应,获得相应的氚代产物23–26。值得注意的是,与已知的Pd/C催化体系相比,该策略具有出色的SA。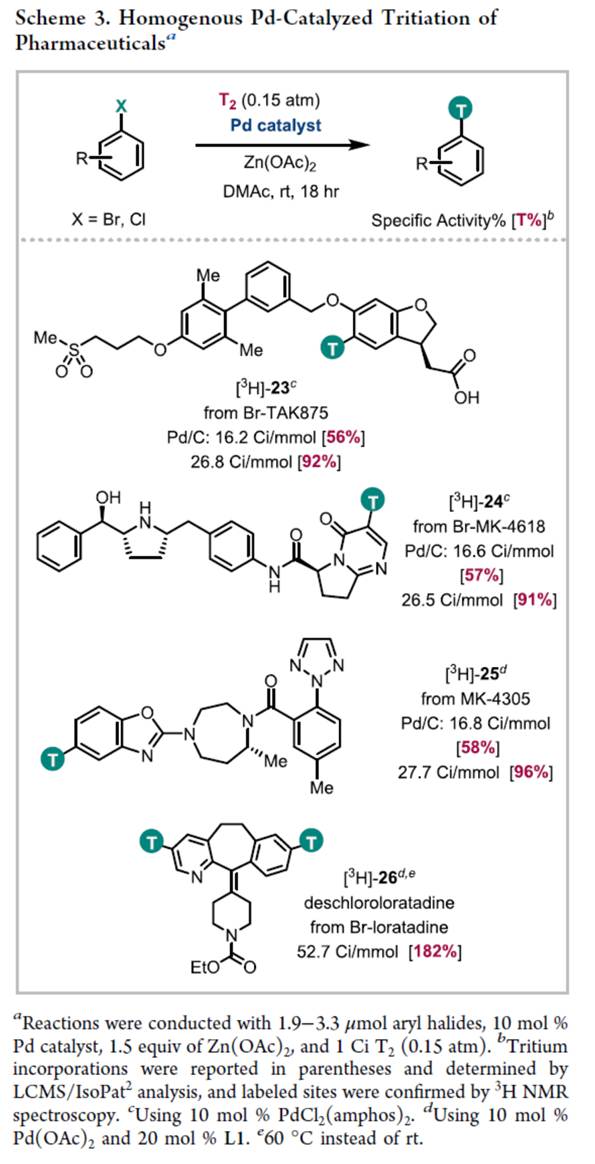
同时,作者还对反应的实用性进行了研究(Scheme 4)。3-溴-4-氯苯甲酸的克级脱溴氘代反应,可以85%的收率得到氘代化合物27,其是制备神经激肽-3受体拮抗剂29的关键氘代中间体。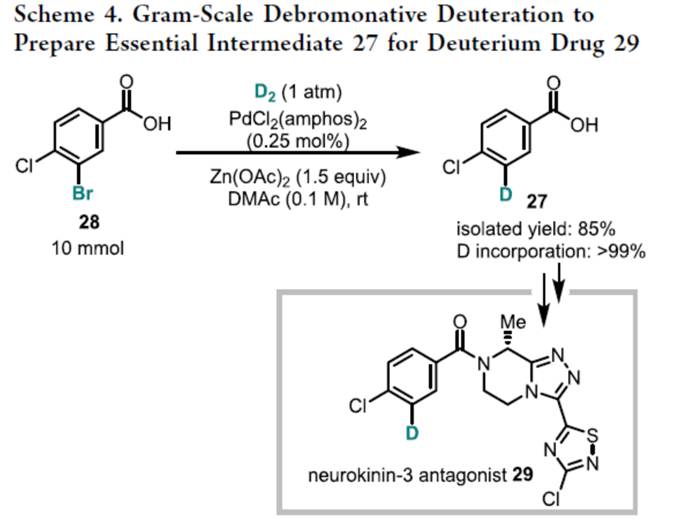
接下来,作者对上述脱卤氘代与氚代过程的反应机理进行进一步研究 (Figure 2)。首先,根据Ritter的研究[3],阳离子[P(Ad)3Pd−Ar]+ (Pd3)可能是促进氢活化的中间体。当混合PdArCl (Pd1)与Zn(OAc)2时,NMR分析显示没有形成阳离子Pd3。相反,在30秒内观察到一种新的中间体PdArOAc(Pd2),产率为50%(Figures 2A)。其次,作者以1-溴-4-氟苯为底物,Pd4为催化剂,采用NMR监测催化反应过程发现,在DMAc-d9中存在Zn(OAc)2的情况下,Pd4快速定量转化为Pd2(Figure 2B)。在D2气氛下,Pd2的信号强度保持不变,而1-溴-4-氟苯的信号逐渐减弱,氘代产物开始积累。这种行为强烈表明Pd2是催化剂的静止状态(resting state)。此外,Pd2很容易与D2反应,导致15分钟内消耗90%(Figures 2C)。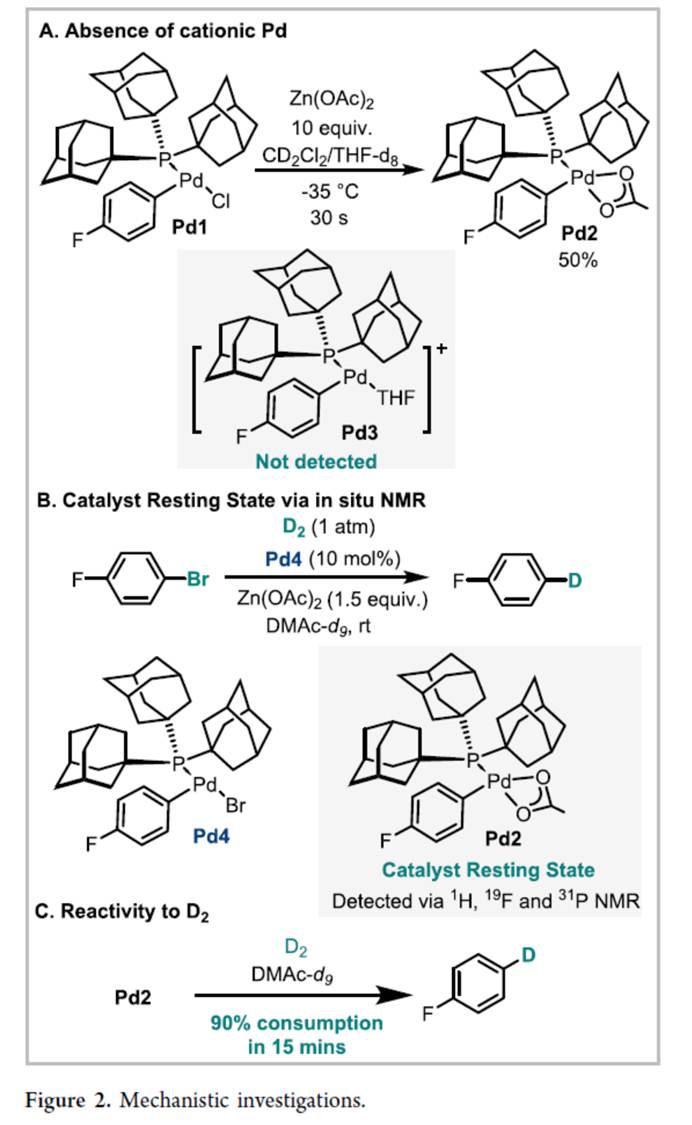 同时,作者还进行了催化剂抑制研究 (Figure 3)。研究结果表明,脱卤产生的卤素阴离子会毒害催化剂。然而,Zn(OAc)2的存在被证明有利于周转,不仅可以作为醋酸盐来源,还可以作为有效的卤化物清除剂。Zn(OAc)2提供了比碱金属醋酸盐(Na、K与Cs)更好的催化剂利用率,而碱土金属醋酸盐即使使用10 mol%的钯也会导致不完全转化。这些发现强调了锌的独特的耐受性及其作为氧化还原中性卤化物清除剂的潜力。
同时,作者还进行了催化剂抑制研究 (Figure 3)。研究结果表明,脱卤产生的卤素阴离子会毒害催化剂。然而,Zn(OAc)2的存在被证明有利于周转,不仅可以作为醋酸盐来源,还可以作为有效的卤化物清除剂。Zn(OAc)2提供了比碱金属醋酸盐(Na、K与Cs)更好的催化剂利用率,而碱土金属醋酸盐即使使用10 mol%的钯也会导致不完全转化。这些发现强调了锌的独特的耐受性及其作为氧化还原中性卤化物清除剂的潜力。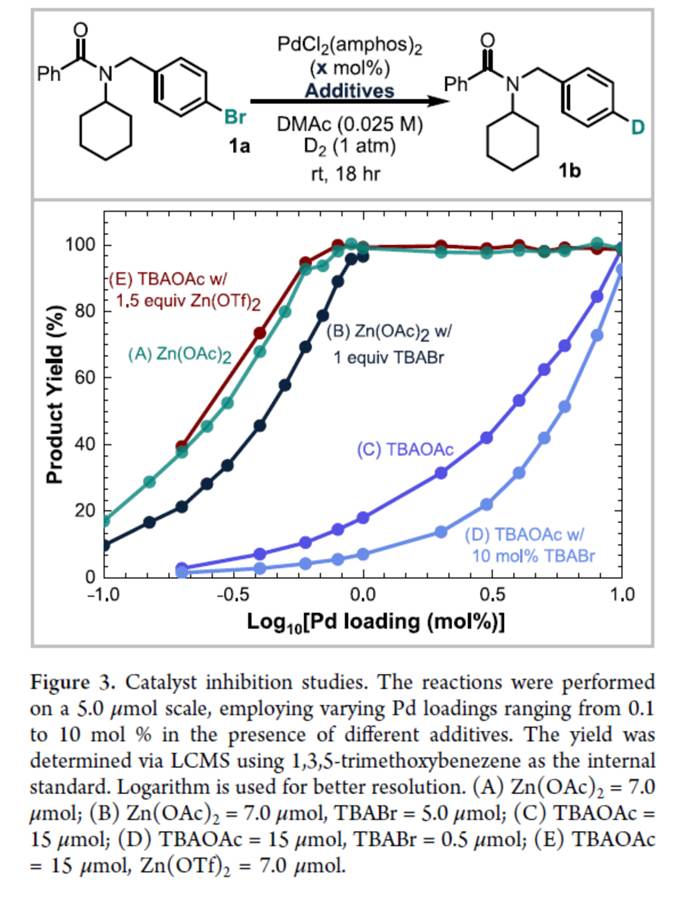
紧接着,作者对氢活化的过程进行了计算研究 (Figure 4)。H2活化的过渡态TS1具有一个6元环,类似于芳香族C−H活化中的协同金属化-脱质子化(CMD)途径。H2与乙酸盐中的氧的线性排列以及O−H的相对较短距离表明,H2在Pd与配位乙酸盐配体(TS1)的帮助下被活化。乙酸盐的存在稳定了过渡态TS1与产物IM2,这有助于随后的还原消除。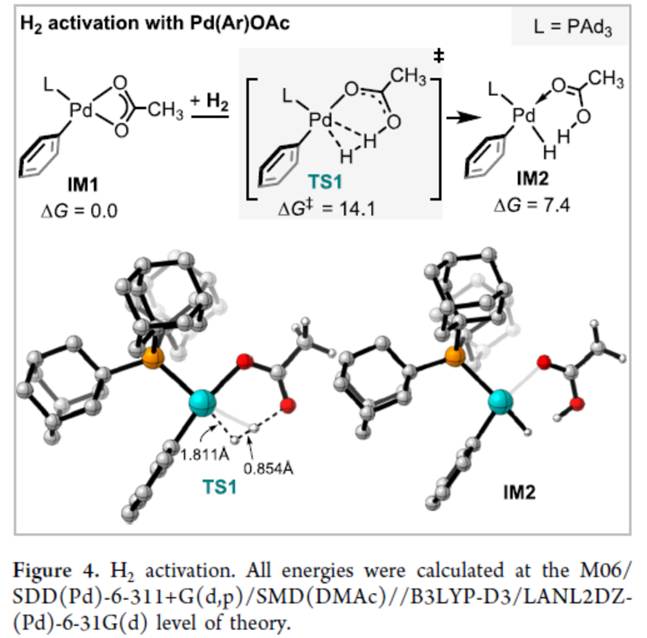
最后,作者提出如下合理的反应机理 (Figure 5)。首先,芳基卤与Pd(0)经氧化加成,形成Pd(II)ArX。其次,Zn(OAc)2发生快速配体交换,生成PdArOAc,即催化剂的静止状态。DFT计算表明,PdArOAc能够在乙酸盐的帮助下活化D2键。然后,得到的Pd(II)−D中间体通过还原消除提供所需的脱卤芳烃产物。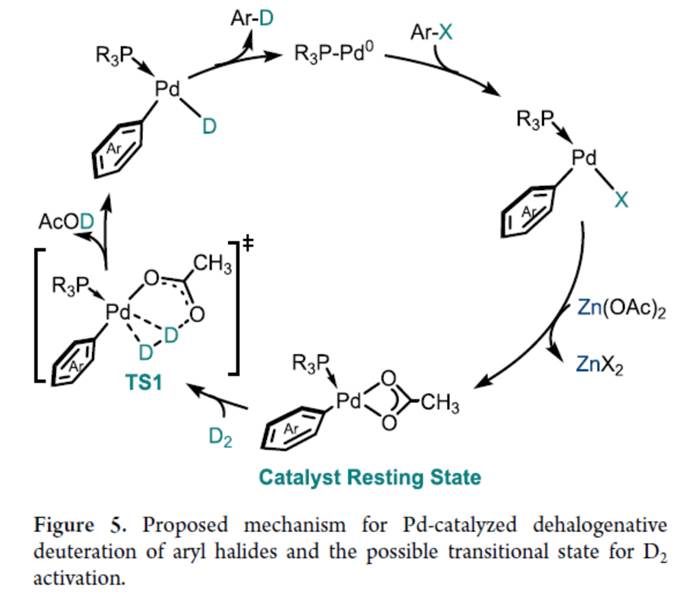
总结:
美国默克公司的Jingwei Li与Qiao Lin团队报道一种新型的均相钯催化芳基卤的脱卤氘代与氚代反应,乙酸锌作为关键的添加剂。该反应证明了具有不同电子与空间性质的各种芳基卤与拟卤的普遍性。值得注意的是,与现有的多相催化体系相比,这些反应始终提供了高产率与定量水平的D掺入,并对各种官能团表现出显著的耐受性。药物化合物的氚代,实现了每个卤素原子的高SA,解决了芳基溴/氯底物参与Pd/C化学中长期存在的局限性。克级规模反应显示了该反应在合成大量含氘API分子方面的显著潜力。初步的机理研究表明,PdArOAc中间体是催化剂的静止状态。Zn(OAc)2不仅用作乙酸盐源,而且用作高效的卤化物清除剂,以防止催化剂中毒。
参考文献:
- [1] C. Zarate, H. Yang, M. J. Bezdek, D. Hesk, P. J. Chirik, J. Am. Chem. Soc. 2019, 141, 5034. doi:10.1021/jacs.9b00939.
- [2] G. K. S. Prakash, T. Mathew, D. Hoole, P. M. Esteves, Q. Wang, G. Rasul, G. A. Olah, J. Am. Chem. Soc.2004, 126, 15770. doi:10.1021/ja0465247.
- [3] D. Zhao, R. Petzold, J. Y. Yan, D. Muri, T. Ritter, Nature 2021, 600, 444. doi:10.1038/s41586-021-04007-y.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841

















No comments yet.