作者:石油醚
导读:
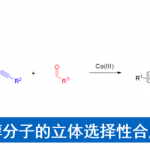
近日,南方科技大学徐明华教授课题组实现了在无金属条件下,三氟甲磺酸促进的烯胺/亚胺与重氮丙酮酸酯多步串联反应,用于构建结构多样的多取代吡咯分子。该反应具有条件温和,操作简单,化学选择性好,底物作用范围广等优点。可用于构建三,四和五取代吡咯以及N-H未保护吡咯。该反应为功能性吡咯分子提供了一种经济高效的合成途径,在相关药物发现与合成中有潜在的应用前景。
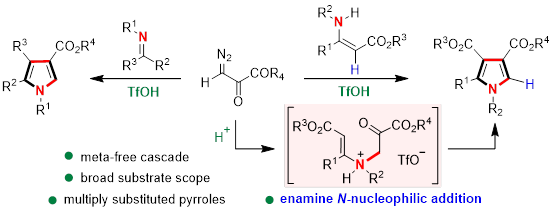
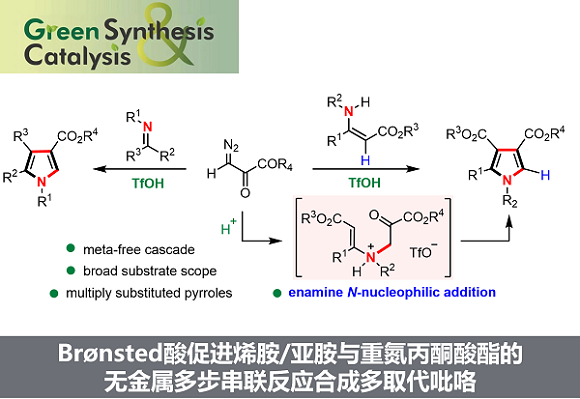
“Brønsted acid promoted synthesis of polysubstituted pyrroles from enamines/imines and diazopyruvates: a metal-free cascade approach
Farrukh Sajjad, Ming-Hua Xu*.
Green Synth. Catal. 2023, ASAP. doi: 10.1016/j.gresc.2023.12.002”
正文:
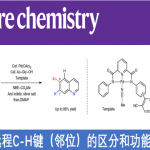
吡咯是组成众多天然产物、药物以及生物活性分子重要结构单元,因此,发展高效构建容忍各种取代基吡咯的合成方法具有重要研究意义。近些年来,过渡金属催化卡宾转移反应已发展成为快速构建多取代吡咯分子的新兴策略之一。其中,结合烯胺/亚胺互变异构化学,这两类底物与重氮化合物的多步串联反应已被科学家广泛用于构建多取代吡咯分子,但目前此类反应需要针对不同底物以及不同反应位点(氮或碳亲核位点选择性)精心挑选金属催化剂,如铜,铱,银 (图一)。另一方面,Brønsted酸已被证明可以质子化重氮化合物,进而促进其进一步化学转化。与使用过渡金属催化剂,Brønsted酸不仅可以降低合成成本,还可以避免产物中金属残留问题。基于以上研究背景,南方科技大学徐明华教授课题组在无金属条件下成功实现了三氟甲磺酸促进的烯胺/亚胺与重氮丙酮酸酯多步串联反应,用于构建结构多样的多取代吡咯分子。该成果于近期发表于国产顶级期刊《Green Synthesis and Catalysis》(DOI: 10.1016/j.gresc.2023.12.002)。
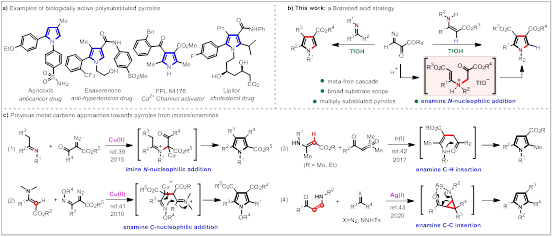
图一. 基于重氮化合物合成多取代吡咯
该反应具有条件温和,操作简单,化学选择性好,底物作用范围广等优点。例如,从烯胺底物出发,反应可高选择性地由N-亲核位点进攻质子化后的重氮丙酮酸酯,随后C-亲核加成,再脱水芳构化形成各种不同取代基的四取代吡咯。底物作用范围如图二所示,吡咯的氮上取代基R1可以是芳基和烷基;吡咯2号位上的取代基R2也可以很好地容忍芳基和烷基;3号位上取代基R3虽然受限于烯胺底物的稳定性必须是吸电子基团,但也可以容忍酯,酮,腈等官能团;4号位上取代基R4来源于重氮底物,其酯基部分可以有各种变化,甚至可以引入天然产物片段。值得一提的是,这些结构多样的吡咯分子绝大多数都可以高产率地合成得到,说明了该反应可以为构建多取代吡咯骨架提供高效合成途径。
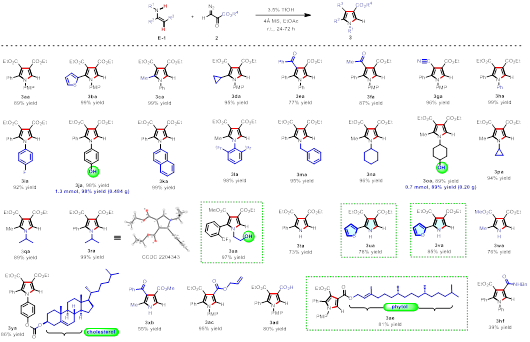
图二. 烯胺与重氮丙酮酸酯反应底物普适性考察
从亚胺底物出发,在相同的条件下亚胺N-亲核进攻质子化后的重氮丙酮酸酯,随后亚胺异构成烯胺并实现C-亲核加成,再脱水芳构化,实现三取代或四取代吡咯的快速合成,反应也具有良好的普适性(图三)。利用此方法,在3号位上取代基R3中可引入芳基或烷基,进一步丰富了多取代吡咯分子结构的多样性。
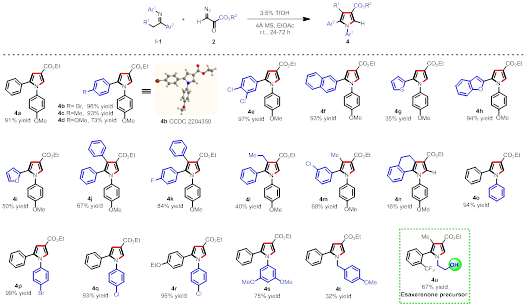
图三. 亚胺与重氮丙酮酸酯反应底物普适性考察
进一步拓展底物作用范围发现,该方法还可以实现双重吡咯化反应,合成结构新颖的双吡咯分子(图四),这些分子在配体化学以及材料化学中有着良好的应用前景。
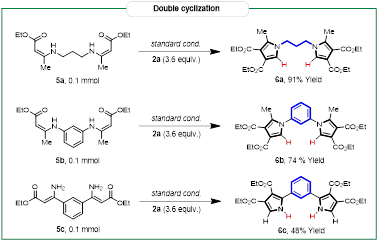
图四. 双吡咯分子的合成
此外,合成得到的多取代吡咯产物还可进一步衍生化合成结构更加多样的其它吡咯分子。特别值得注意的是,吡咯5号位可实现氯代或溴代,进而通过偶联化学引入不同取代基,合成五取代吡咯分子(图五)。
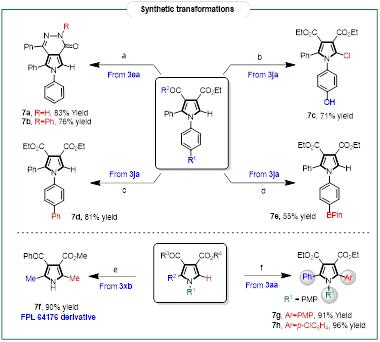
图五. 产物衍生化应用研究
综上所述,南方科技大学徐明华课题组开发了一种高效的Brønsted酸促进的烯胺/亚胺与重氮丙酮酸酯的无金属多步串联反应。该反应具有条件温和,操作简单,化学选择性好,产率高,底物作用范围广等优点,可用于构建三,四和五取代吡咯以及N-H未保护吡咯。该反应为功能性吡咯分子提供了一种经济高效的合成途径,在相关药物发现与合成中有潜在的应用前景
导师简介:
徐明华教授,中科院百人计划、国家杰出青年基金获得者。博士毕业于中国科学院上海有机化学研究所,曾任中国科学院上海药物研究所研究员、课题组长、博士生导师,新药研究国家重点实验室研究员。2018年受邀加入南方科技大学,现任化学系和深圳格拉布斯研究院双聘教授,获深圳市国家级领军人才、广东省“珠江人才计划”领军人才称号。
主要从事有机不对称合成及手性药物方面的研究,致力于发展高效不对称催化方法用于手性药物绿色合成和小分子药物发现。在国内外核心学术期刊上发表论文130多篇,多个工作受到国际国内同行的关注和好评,30多次被选为研究亮点报道;申请国内外专利24项,授权16项(美国专利2项)。
曾获中国化学会青年化学奖(2005),首届药明康德生命化学研究奖(2007),中国科学院朱李月华优秀教师奖(2012),中科院优秀研究生指导教师(2013),上海市优秀学术带头人(2014),中国科学院特聘骨干研究员(2015),前沿有机化学亚洲核心计划讲座奖ACP Lectureship Award(日本3次、韩国、新加坡、泰国、台湾),以及法国斯特拉斯堡大学邀请教授、日本九州大学“Global 30”计划“Part-time Lecturer”、台湾国科会化学促进中心访问教授、日本北海道大学Hokkaido Summer Institute邀请教授,中国化学会高级会员、英国皇家化学会会士等荣誉。2014年获上海市自然科学一等奖,2016年获国家自然科学二等奖。
课题组长期招聘有机合成工作人员和博士后,从事有机不对称合成及创新药物的研究,详见课题组网页:http://faculty.sustech.edu.cn/xumh/
相关链接:
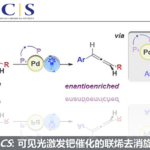
南方科技大学徐明华课题组Angew: 铑催化不对称分子内环丙烷化反应方法学
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
















No comments yet.