本文作者:杉杉
导读
近日,四川大学的刘波课题组在Angew. Chem. Int. Ed.中发表论文,首次完成天然产物shizukaol J与trichloranoid C以及trishizukaol A的对映选择性全合成。其中,对于shizukaol J全合成路线设计中的关键步骤主要涉及:通过Nelson催化不对称烯酮-醛环加成以及后续的烯丙基烷基化/酸促进的环化过程,构建相应的内酯结构单元;通过双重羟醛缩合策略构建5/6双环结构单元;通过PTC促进的非对映选择性亲核取代步骤,构建shizukaol J分子中相应的四级立体生成中心。而trichloranoid C 与trishizukaol A全合成路线中的关键步骤则涉及呋喃基二烯 (furanyl diene)的形成与Diels-Alder反应的串联以及呋喃氧化与全去保护(global deprotection)的一锅反应过程。
Asymmetric Total Synthesis of Shizukaol J, Trichloranoid C and Trishizukaol A
X. Wang, Z. Wang, X. Ma, Z. Huang, K. Sun, X. Gao, S. Fu, B. Liu, Angew. Chem. Int. Ed. 2022, ASAP doi:10.1002/anie.202200258.
正文
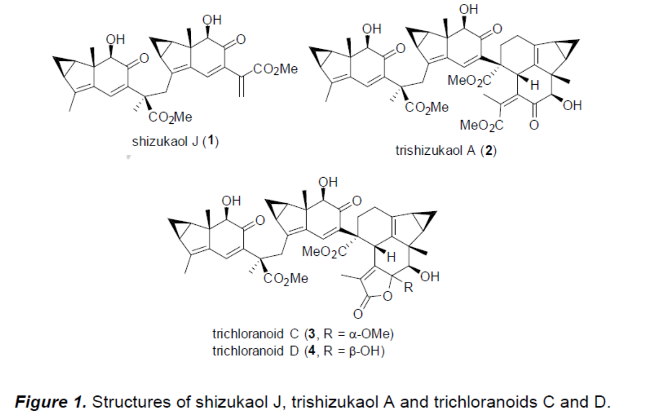
Oligomeric lindenane sesquiterpenoids是由Chloranthus genus中分离出的一类重要天然产物,具有良好的生物活性。目前,对于lindenane sesquiterpenoid类天然产物的全合成,已经有相关的文献报道[1]-[2]。然而,对于部分天然 lindenane oligomer类天然产物,例如shizukaol J (1),trishizukaol A (2)以及trichloranoids C与D (3–4) (Figure 1) 的全合成路线设计,则尚未有相关的文献报道。这里,四川大学的刘波课题组成功完成首例天然产物shizukaol J、trichloranoid C以及trishizukaol A的对映选择性全合成路线设计。
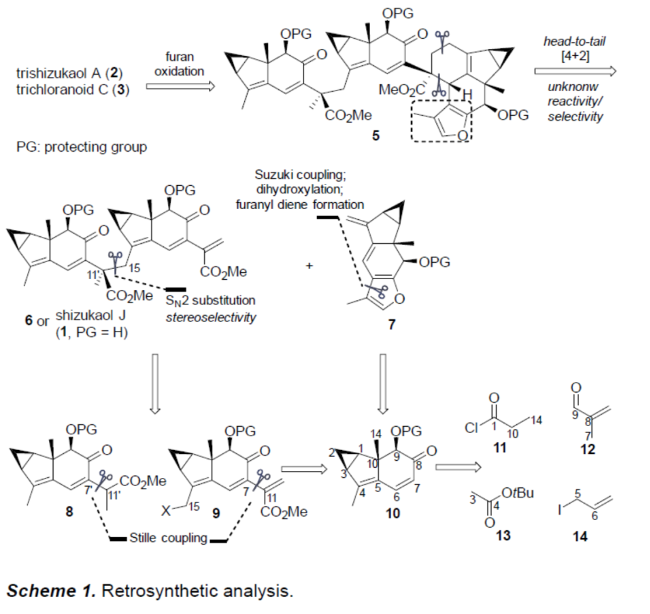
首先该小组通过逆合成分析(Scheme 1)表明,上述天然产物shizukaol J与trichloranoid C以及trishizukaol A的对映选择性全合成路线设计中的关键砌块以及起始原料主要涉及砌块5、亲二烯体砌块6或1、二烯砌块7、亲核前体8、烯丙基卤砌块9以及砌块 10与起始原料11–14。
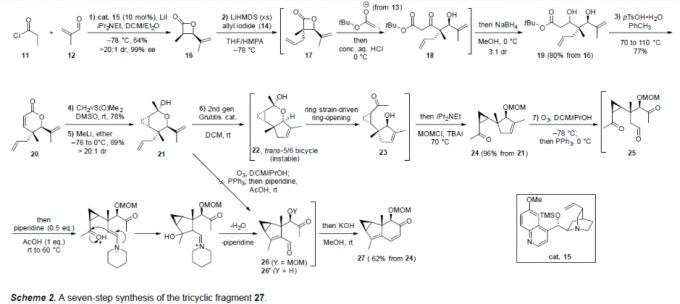
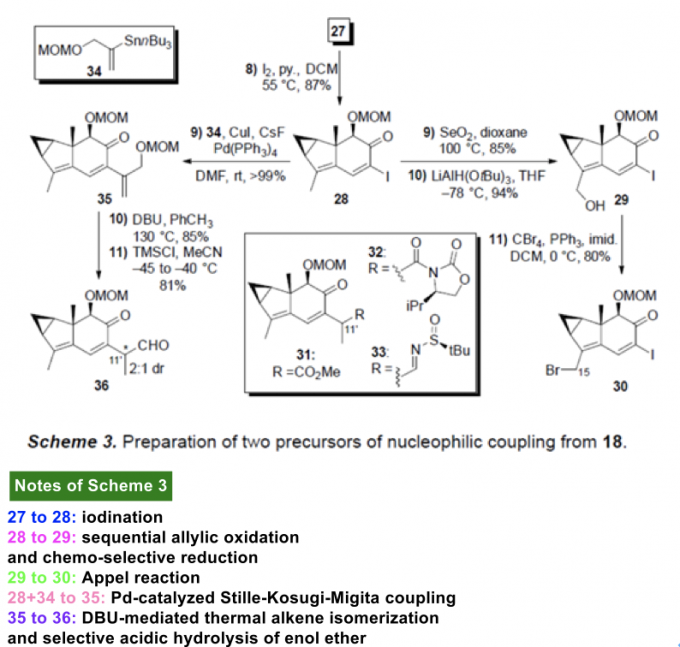
接下来,该小组首先进行三环结构单元27 (Scheme 2)以及后续全合成路线设计中的关键砌块30与36以及28的构建 (Scheme 3)。
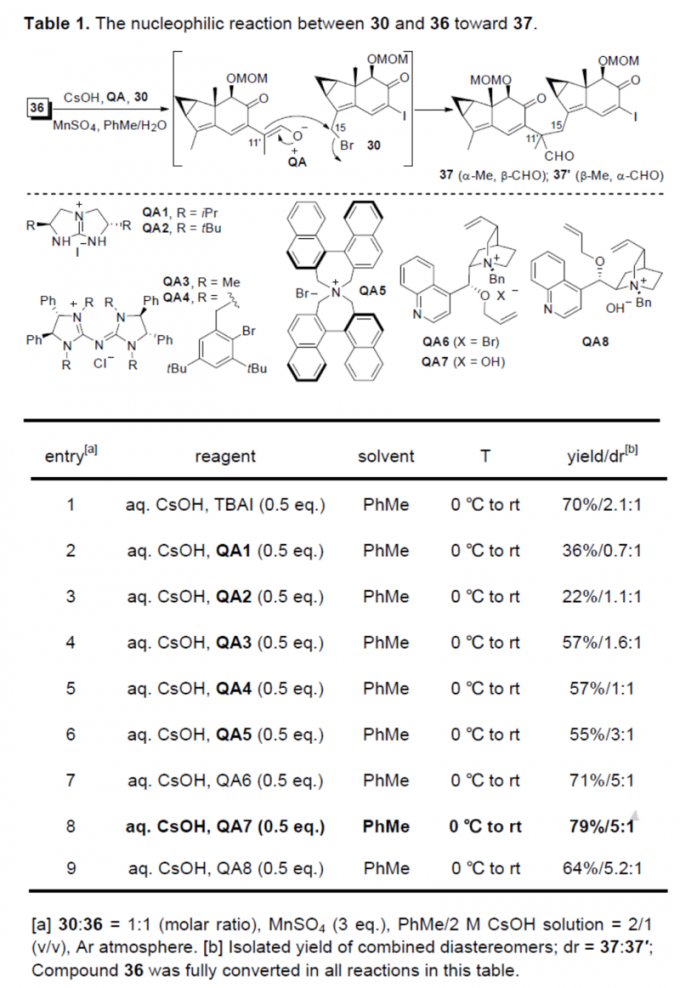
接下来,该小组进一步对于通过砌块30与36之间的亲核取代过程,获得砌块37的反应条件进行进一步优化(Table 1)。研究表明,在采用手性QA (quaternary ammonium)7作为PTC时,能够获得良好的反应收率与立体选择性。
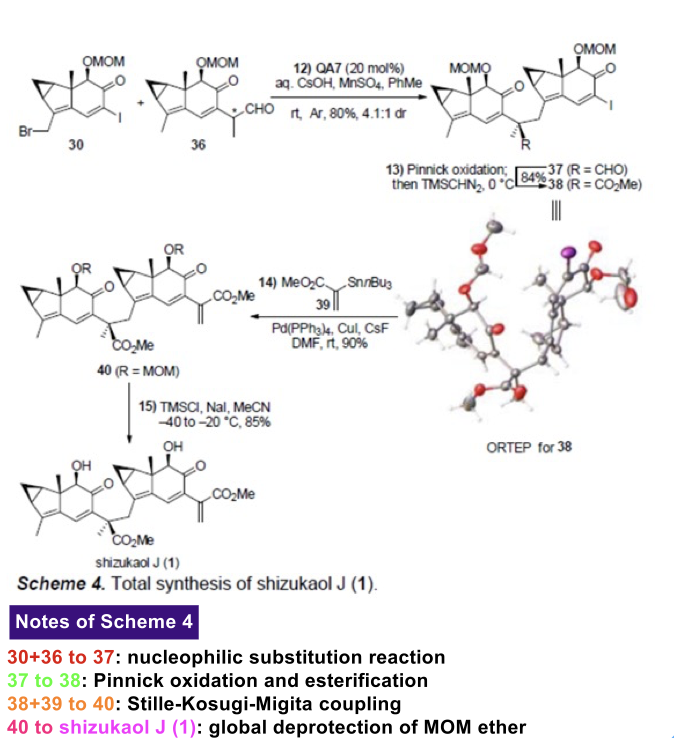
之后,该小组进一步通过砌块37最终完成shizukaol J (1)的对映选择性全合成 (Scheme 4)。
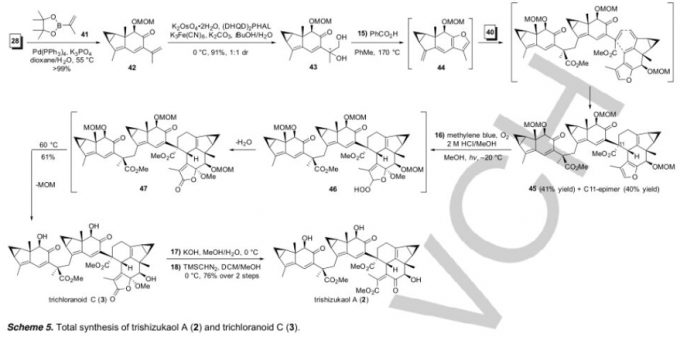
同时,该小组发现,通过砌块28能够进一步完成相应天然产物trichloranoid C以及 trishizukaol A 的对映选择性全合成 (Scheme 5)。
参考文献
- [1] (a) G. Yue, L. Yang, C. Yuan, B. Du, B. Liu, Tetrahedron 2012, 68, 9624. doi: 10.1016/j.tet.2012.09.053.
- (b) J. Wu, Y. Lu, B. Tang, X. Peng, Nat. Commun. 2018, 9, 4040. doi: 10.1038/s41467-018-06245-7.
- (c) B. Du, Z. Huang, X. Wang, T. Chen, G. Shen, S. Fu, B. Liu, Nat. Commun. 2019, 10, 1892. doi: 10.1038/s41467-019-09858-8.
- (d) S. Qian, G. Zhao, Chem. Commun. 2012, 48, 3530. doi: 10.1039/C2CC17882F.
- (e) G. Yue, L. Yang, C. Yuan, B. Du, B. Liu, Tetrahedron 2012, 68, 9624. doi: 10.1016/j.tet.2012.09.053.
- [2] C. Yuan, B. Du, H. Deng, Y. Man, B. Liu, Angew. Chem. Int. Ed. 2017, 56, 637. doi: 10.1002/anie.201610484.
- [3] C. Zhu, X. Q. Shen, S. G. Nelson, J. Am. Chem. Soc. 2004, 126, 5352. doi: 10.1021/ja0492900.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载





















No comments yet.