本文作者:杉杉
导读
近日,南京大学朱少林教授课题组在Nature Communications发表论文,报道了一种NiH催化N-酰基烯胺(N-acyl enamines)的对映和区域选择性还原氢芳化策略,可在温和且操作简单的反应条件下,合成各种结构多样且对映体富集的苄胺衍生物(benzylamines)。
NiH-catalyzed asymmetric hydroarylation of N-acylenamines to chiral benzylamines
Yuli He, Huayue Song, Jian Chen & Shaolin Zhu*
Nat.Commun. 2021, 12, 638. DOI:10.1038/s41467-020-20888-5
正文
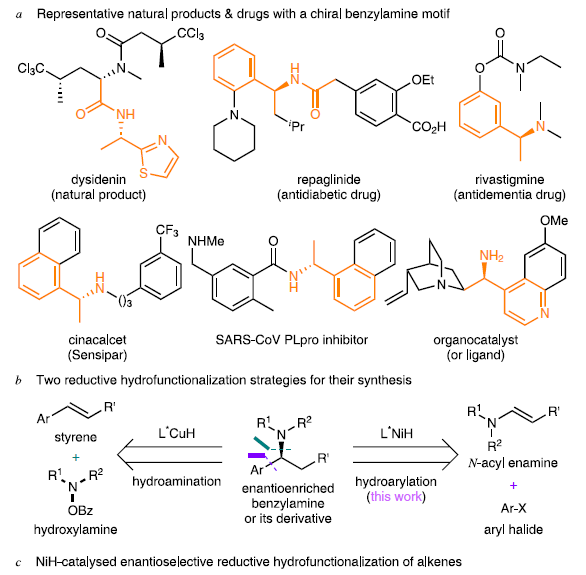
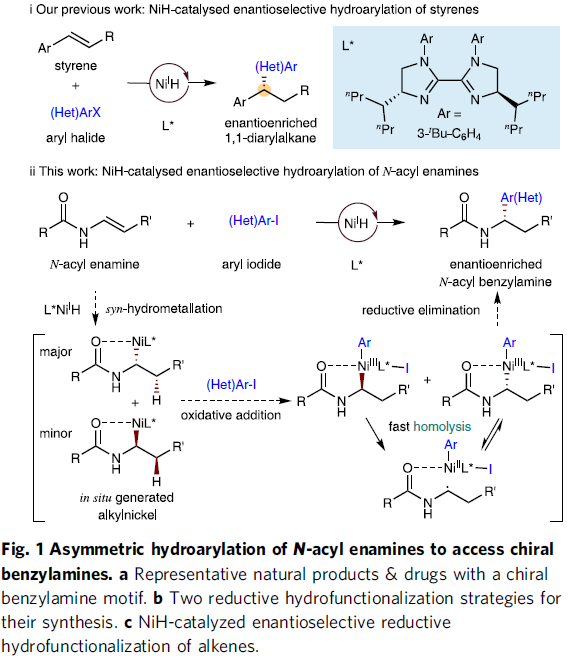
苄胺以及相关酰胺衍生物,是天然产物、药物、农用化学品和其他化学品中常见的骨架(Fig. 1a)。长期以来,研究者一直在探索关于此结构的对映选择性合成策略。其中,通过金属氢化物催化烯烃的还原性加氢官能化反应是一种具有吸引力的合成苄胺的方法。前期,以苯乙烯和亲电胺化试剂为初始底物,Buchwald[1]和Miura、Hirano[2]分别实现了CuH催化对映选择性还原加氢胺化反应(Fig. 1b, left)。受此启发,作者设想,如果可实现烯胺的不对称加氢芳基化,则可直接获得对映体富集的苄胺衍生物(Fig. 1b, right)。
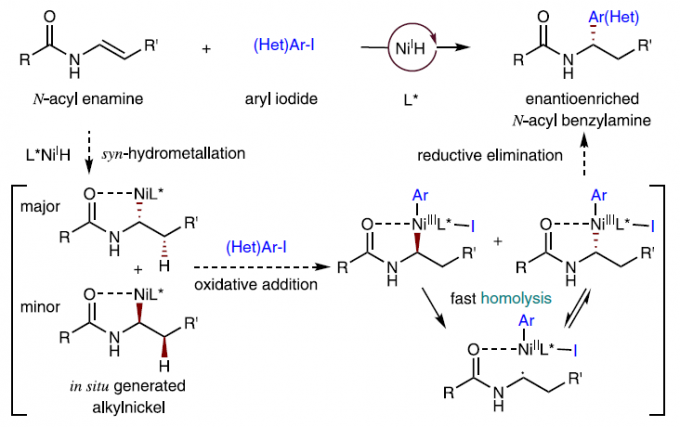
近年来,NiH催化已成为不对称构建C-C键的有效手段。在该过程中:(1)起始烯烃和芳基卤化物/烷基卤化物均可商购或合成;(2)无需预先制备有机金属试剂;(3)非手性烯烃的碳或外消旋烷基亲电体的碳形成的sp3-杂化立体中心可能被对映选择性地控制。最近,本课题组[3]使用新型手性镍-双(咪唑啉)催化剂,实现了苯乙烯的对映选择性加氢芳基化反应(Fig. 1c, i)。为了进一步证明这种还原性NiH催化的适用性,作者还对富电子烯烃(如N-酰基烯胺)的不对称加氢芳基化的可行性进行了研究,后者通常不如苯乙烯(Fig. 1c, ii)。首先,L*NiH物种加氢金属化至N-酰基烯胺,生成两个烷基镍对映体。随后,它们可与芳基碘化物进行氧化加成,得到两种高价的Ar-Ni(III)-烷基对映体,在选择性还原消除之前,它们会经历快速的均相分解和立体选择性自由基重组。在合适的手性配体的存在下,自由基重组过程可以被对映选择性地控制并获得单个Ar-Ni(III)-烷基对映体。最后,通过还原消除即可获得对映富集的芳基化产物。此外,在编写本论文期间,Nevado等[4,5]也报道了类似的工作。
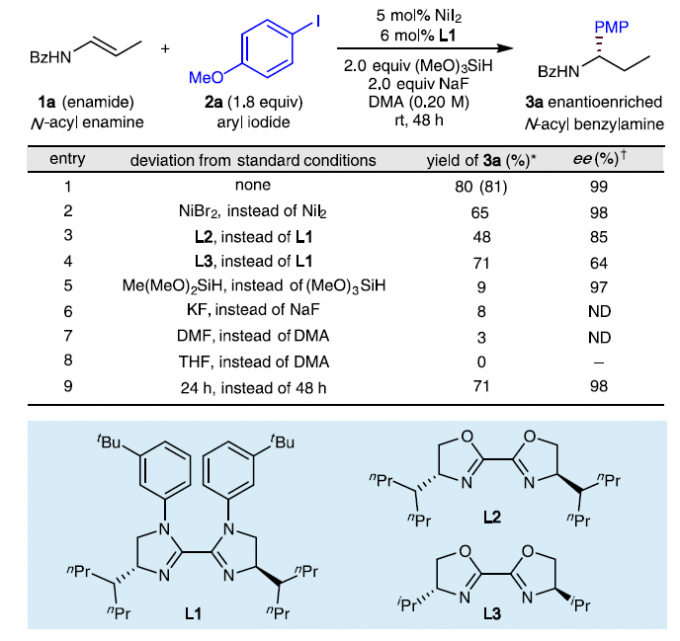
首先,作者以烯基酰胺1a和4-碘苯甲醚2a作为模型底物,进行了相关反应条件的筛选(Fig. 2)。反应结果表明,当使用5 mol%的NiI2为催化剂,6 mol%的手性双咪唑啉(L1)为配体,同时加入两当量的(MeO)3SiH和NaF,可于DMA(0.2 M)溶剂中室温反应48 h,以80%的收率和99%的 ee值获得目标产物3a。
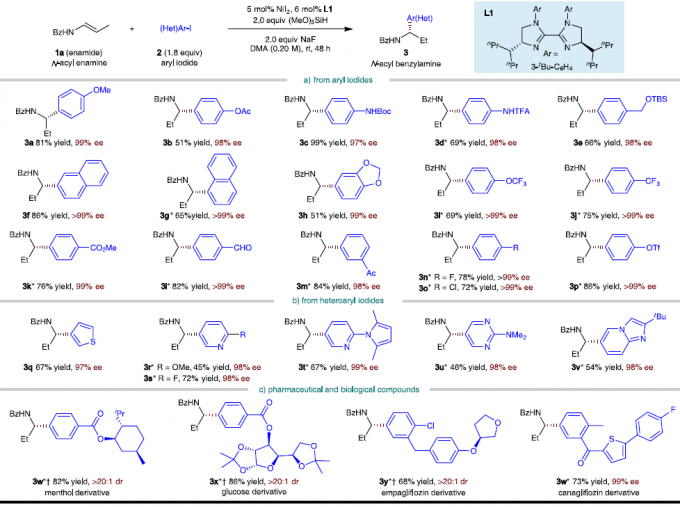
在获得上述最佳反应条件后,作者首先固定烯基酰胺1a,对芳基碘化物2的范围进行了扩展(Fig. 3)。邻、间或对位(2a–2p)的芳基取代基均可反应,但对于邻位取代基的芳基碘化物反应性较低(2g)。具有给电子(2a–2e)和吸电子(2h–2p,2w–2z)的芳基碘化物,均可顺利反应,当以Ni(ClO4)2∙6H2O为催化剂时,后者仅需1.5当量的芳基碘化物。同时,各种官能团均可耐受,如醚、酯、氨基甲酸酯、酰胺、三氟甲基、醛、酮、卤素等,为进一步反应提供了多种可能。此外,含有噻吩(2q,2z)、吡啶(2r,2s和2t)、吡咯(2t)、嘧啶(2u)和咪唑并吡啶(2v)等杂环化合物,也同样与体系兼容。值得注意的是,一些生物活性和药物分子,如 薄荷醇(L-menthol,2w),葡萄糖衍生物(2x),恩格列净(empagliflozin,2y)和卡格列净(canagliflozin,2z),也可同样取得了预期的结果,进一步说明了反应的实用性。
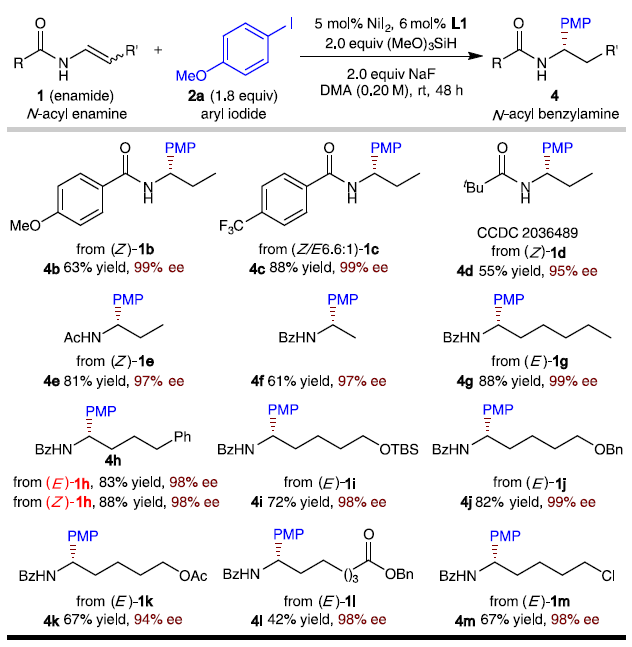
随后,作者固定4-碘苯甲醚2a,对烯基酰胺1的范围进行了扩展(Fig. 4)。苯甲酰基的芳环上缺电子取代基比富电子取代基具有更高的收率(1c对1b)。位阻较少的N-乙酰基烯胺(1e)比N-新戊酰烯胺(1d)更具反应性。在β-位具有一系列不同官能化烷基取代基的酰胺底物也能顺利进行不对称氢芳基化反应(1h–1m)。同时,该反应可兼容各种官能团,如醚(1i,1j),酯(1k,1l)和烷基氯(1m)。此外,烯基酰胺底物的E-和Z-异构体均产生相同的对映体产物,具有相同水平的对映体选择性(4h)。
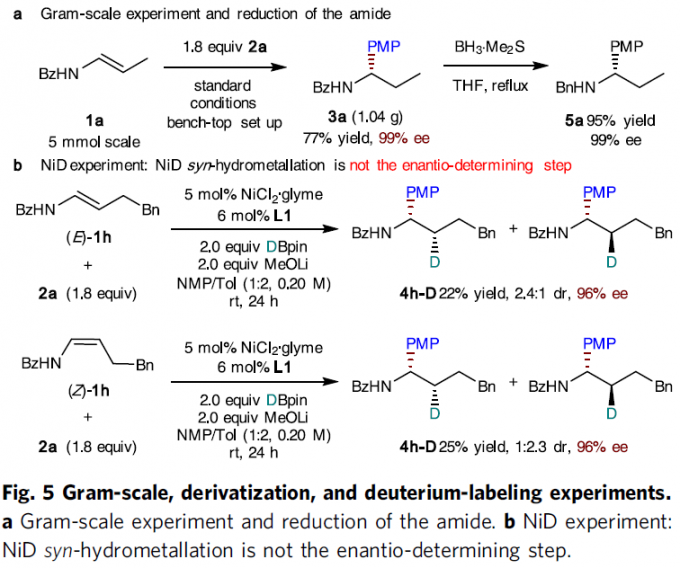
紧接着,通过3a的克级实验(5 mmol规模)以及3a的后期的衍生化(5a),进一步证明了反应的实用性(Fig. 5a)。为了进一步阐明加氢金属化过程(Fig. 5b),作者使用氘代DBpin,并将2a分别与 (E)-1h和 (Z)-1h反应,获得相反的非对映异构体混合物。若将NiD加氢金属化作为N-酰基烯胺的对映体确定步骤,则应形成非对映体纯的4h-D。然而,反应均获得两种非对映异构体的混合物,从而表明NiD的插入不是对映体确定步骤。同时,作者还发现,在反应过程中(E)-烯烃底物可异构化为(Z)-异构体。相反,(Z)-烯烃底物向(E)-异构体的异构化速度则非常缓慢。另一方面,在存在(E)-和(Z)-烯烃底物的时,氘代产物的对映选择性水平相同与Ni(III)迅速均化为Ni(II)的机理一致,随后的对映选择性自由基重组充当了对映体决定步骤(Fig. 1c, ii)。
总结
南京大学朱少林教授课题组报道了一种NiH催化N-酰基烯胺的对映和区域选择性还原氢芳化策略,可在温和的反应条件合成对映体富集的苄胺衍生物。同时,该反应具有操作简单、底物范围广泛、官能团耐受性良好等特点。此外,机理研究表明NiH的加氢金属化不是对映体确定步骤。
参考文献
[1] Zhu, S., Niljianskul, N. & Buchwald, S. L. Enantio- and regioselective CuH catalyzed hydroamination of alkenes. J. Am. Chem. Soc. 135, 15746-15749 (2013). [2] Hirano, Y., Miki, K., Satoh, T. & Miura, M. Copper-catalyzed intermolecular regioselective hydroamination of styrenes with polymethyl hydrosiloxane and hydroxylamines. Angew.Chem. Int. Ed. 52, 10830-10834 (2013). [3] He, Y., Liu, C., Yu, L. & Zhu, S. Enantio- and regioselective NiH-catalyzed reductive hydroarylation of vinylarenes with aryl iodides. Angew. Chem. Int. Ed. 59, 21530-21534 (2020). [4] Cuesta-Galisteo, S., Schörgenhumer, J., Wei, X., Merino, E. &Nevado, C. Nickel-catalyzed asymmetric synthesis of α-arylbenzamides. Angew.Chem. Int. Ed. https://doi.org/10.1002/anie.202011342 (2020). [5] He, Y., Song, H. & Zhu, S. NiH-Catalyzed asymmetric hydroarylation of N-acyl enamines: practical access to chiral benzylamines. ChemRxiv. Preprint at: https://doi.org/10.26434/chemrxiv.13084946.v1 (2020).















No comments yet.