2017年、首尔大学的 Soon Hyeok Hong课题组、使用镍-可见氧化还原催化剂体系成功实现了C(sp3)-H键的直接硫代羰基化。
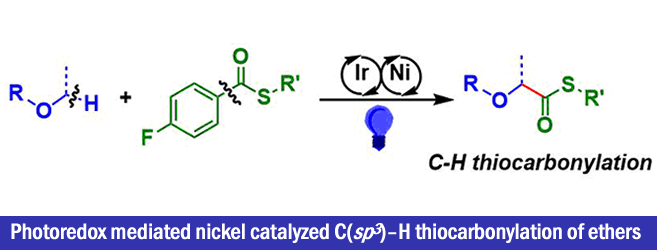
“Photoredox mediated nickel catalyzed C(sp3)–H thiocarbonylation of ethers”
Kang, B.; Hong, S. H. * Chem. Sci. 2017, 8, 6613. doi:10.1039/C7SC02516E
问题点设定
硫代酸酯合成方法,其中具有代表性的有以下几种。但是,这些常规方法需要有高氧化度的试剂,很严苛的反应条件,以及还存在容易发生硫醇氧化等问题。
- 巯醇与羧酸等价物的缩合反应
- 硫代酸与亲电子试剂反应(烷基化)
- 醛的氧化硫酯化
- 在CO气体存在下,烯烃和卤化物的硫代羰基化
因此,如果可以直接对C-H键实现硫代羰基化,那么这将是硫酯合成的最理想的方法。在体内,可以通过碳自由基中间体的重排反应形成硫酯。然而,在这么发达的有机合成领域,至今还没有一种对C-H键直接硫酯化的反应报道。
这次,作者使用一种简单的硫酯作为原料实现了C(sp3)-H硫代羰基化反应。
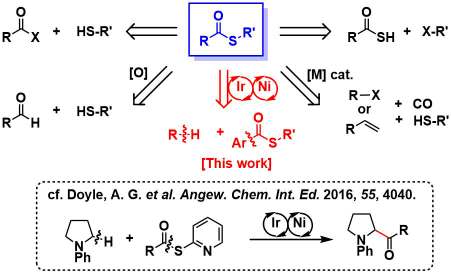
具体实施手法
要实现上述的变换,最大的难点是C(酰基)-S键比C(酰基)-C键要弱。目前就小编所知的,有机金属对硫酯的氧化加成的论文中,基本上都是只有切断C(酰基)-S键的例子。
2016年,Doyle课题组,使用镍-可见光氧化还原催化剂的协同催化体系,实现了2-吡啶基硫酯和N-芳基胺的反应[1]を。而该条件下也是发生的C(酰基)-S键的断裂(上图)。
本次介绍的论文中、作者认为可以通过筛选硫代酯侧的电子性・立体性、选择性的进行C(酰基)-C键的切断,而不是一直以来的C(酰基)-S键的切断、实现硫代羰基化反应。
主张的有效性验证
①反应条件
对于硫代酯源来说,经过筛选作者发现当离去基团为p-(三氟甲基)苯基时,目标产物的产率最高。非芳基或者非缺电子基团的产率非常低。
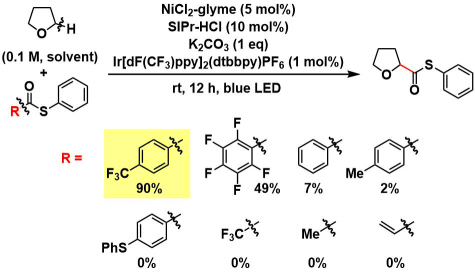
另外,除了硫代酯源,反应条件以Ni-SIPr催化剂、Ir[dF(CF3)ppy]2(dtbbpy)PF6光催化剂,溶剂量的醚的组合最佳。而对照实验也表明,这几个反应试剂缺一不可。如果NHC是现做现用的话,不用碱也能进行反应。
②底物拓展
・硫代酯的与硫连接的基团,如果是苯环的话,苯环上的取代基基本都能兼容。除了苯环以外,萘环跟苄基取代的底物也能进行反应。而脂肪族的取代基就无法进行反应了。
・醚侧、无论是环状或者链状的都可以进行反应,然而环状的产率要高。然而含有杂原子的,比如保护后的吡咯烷,噻吩等都无法进行反应。
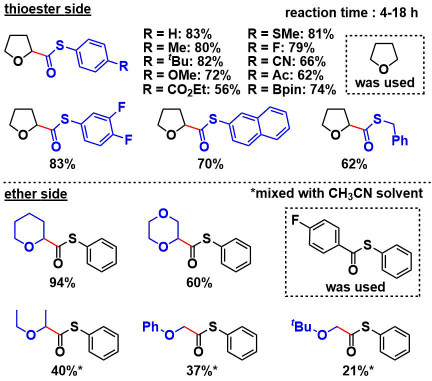
③反应机理
上述文章中已经提到,C(酰基)-S键比C(酰基)-C键要弱,而通过BDE计算发现有以下两点疑问。
・通过对上述硫代酯的BDE计算发现、确实是C(酰基)-S键要弱,因此选择性的切断C(酰基)-C键显得站不住脚。
・生成的各种硫代酯产物之间的BDE的差异很好,无法解释实验中带来的巨大的产率差异这一现象。
因此,作者试图调查了反应体系中镍催化剂的氧化态。发现,一般理论上用于引发氧化加成的Ni(0),并没有使得反应发生。而NHC-Ni(Ⅱ)活性种却能导致产率的提高,因此作者判断Ni(Ⅱ)作为催化活性种作用。
继而,作者假定除了氧化加成那步以外,硫代酯的活化路径都是以单电子还原的形式进行的。已知当通过电化学还原时,硫酯能分解为酰基和硫醇盐、因此作者认为这次也有可能通过可见光氧化还原催化剂进行相同的反应。
通过对硫酯试剂进行循环伏安法测量、发现其还原电位为は-1.65 V(vs SCE in MeCN)、该电位下理论上无法被Ir(Ⅱ)→Ir(Ⅲ)(-1.37 V vs SCE in MeCN)还原。然而作者等人通过对阳离子可见光氧化还原催化剂的路易斯酸性质分析和镍由来的硫醇盐捕捉等,认为该还原是可以进行的。
通过以上的考察分析以及机理解析实验的结果,作者提出了下图所示的反应机理假说。首先通过光激发的Ir(Ⅲ)将NHC-Ni(Ⅱ)(+1.01 V)氧化成Ni(Ⅲ)。生成的Ir(Ⅱ)与硫代酯发生单电子还原、重新再生成Ir(Ⅲ)が。被还原的硫代酯分解成酰基自由基与硫醇、硫醇被Ni(Ⅲ)捕捉。酰基自由基与镍催化剂反应发生脱CO反应生成芳基自由基,然后与醚的C-H键通过HAT过程进行C-H切断。然后生成的醚的碳自由基与Ni(Ⅲ)结合形成Ni(Ⅳ)活性体,最后发生还原消除得到产物。
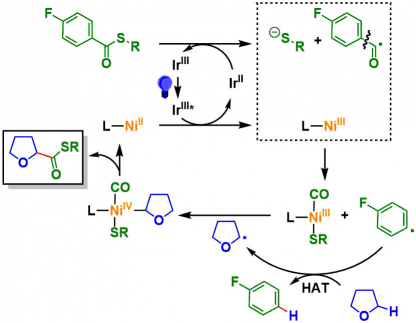
Comment
- 芳基自由基作为HAT的媒体,感觉也能与醚以外的反应物发生反应,到底是哪一块限制了其反应性?其对金属的配位?
- 硫酯侧的官能团改变电子状态从而影响单电子还原,因此底物扩展很困难?
- 很遗憾的本文中并未实现的、C(酰基)- C键优先于C(酰基)-S键发生断裂的方法,到底还有何下一步可望实现的idea?
参考文献
- Joe, C. L.; Doyle, A. G. Angew. Chem. Int. Ed. 2016, 55, 4040. DOI: 10.1002/anie.201511438
- Hong, X.; Liang, Y.; Houk, K. N. J. Am. Chem. Soc. 2014, 136, 2017. DOI: 10.1021/ja4118413
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!



















No comments yet.