概要
苄氧基羰基保护基(benzyloxycarbonyl, CbzまたはZ)、它经常用于通过形成氨基甲酸酯来保护胺基。在某些情况下,它还用于醇和苯酚上羟基的保护基。
于强碱条件下的酯水解条件・强酸性条件・亲核条件・弱的氢化物的还原条件耐受性好、可以通过接触还原条件进行脱保护。因此,可以与Fmoc保护基,Boc保护基联用。
基本文献
- Bergmann, M.; Zervas, L. Ber. 1932, 65, 1192. doi:10.1002/cber.19320650722
开发历史
本保护基在1932年由Max Bergmann首次合成应用于多肽的合成上。
反应机理
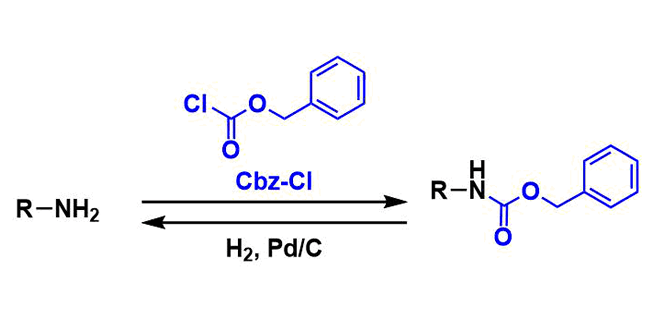
保护
氯甲酸苄酯(Cbz-Cl or Z-Cl)常用作反应试剂。反应中的碱通常为吡啶或三乙胺。对于氨基酸的保护等,使用无机碱的Schotten-Baumann条件也很常见。
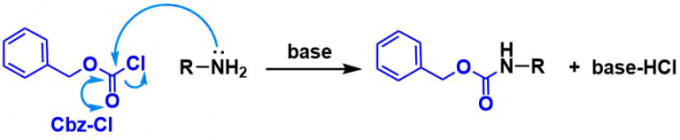
脱保护
Pd/C催化下的接触氢还原进行脱保护是常用的方法。副产物是挥发性的甲苯与CO2だ、因此后处理也很简便。对于比较难脱保护的底物,可以尝试下Pd(OH)2)。
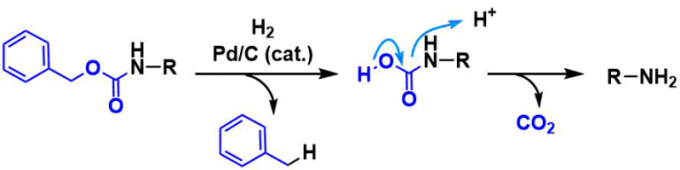
反应实例
与Boc2O共存下的Cbz脱保护,可以one step实现Cbz与Boc的置换[1]。
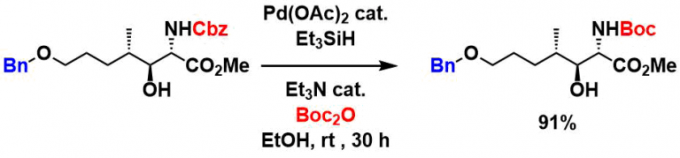
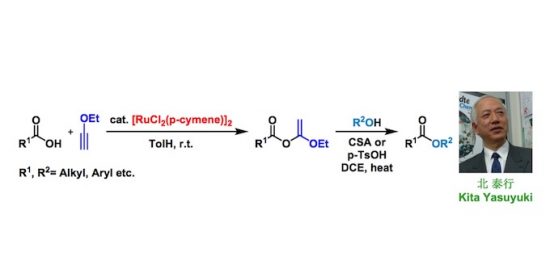
在添加方酸衍生物的条件下,可以在Cbz, Fmoc, Bn保护基存在下,选择性的还原双键[2]。
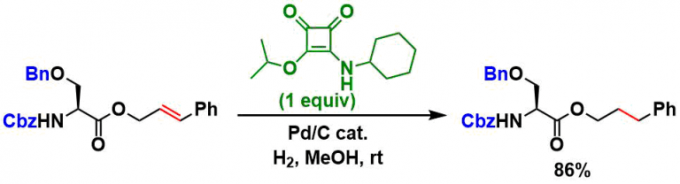
在氨源共存下,Bn基团的脱保护受到抑制,可以选择性地除去Cbz[3]。
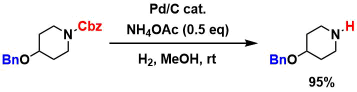
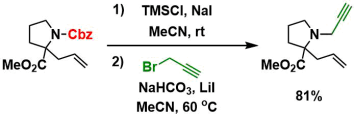
TMS-I条件下的脱保护[4]。
通过使用Ni催化剂,可以选择性地除去杂环氮上的Cbz基团[5]。
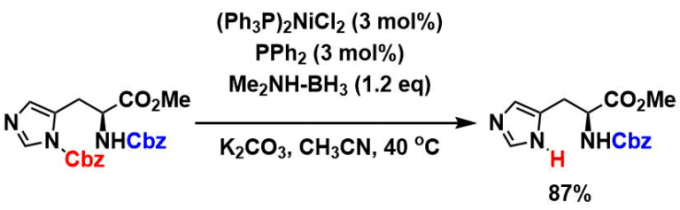
实验小技巧
- Pd(OAc)2とcharcholから系中でPd/Cを作る手法はより安全に水素添加が行えると報告されている[6]。
参考文献
- Sakaitani, M.; Hori, K.; Ohfune, Y. Tetrahedron Lett. 1988, 29, 2983. doi:10.1016/0040-4039(88)85064-0
- Shinada, T.; Hayashi, K.-i.; Yoshida, Y.; Ohfune, Y. Synlett 2000, 1506. DOI: 10.1055/s-2000-7655
- Sajiki, H. Tetrahedron Lett. 1995, 35, 3465. doi:10.1016/0040-4039(95)00527-J
- Tanimori, S.; Fukubayashi, K.; Kirihata, M. Tetrahedron Lett. 2001, 42, 4013. doi:10.1016/S0040-4039(01)00645-1
- Lipshutz, B. H.; Pfeiffer, S. S.; Reed, A. B. Org. Lett. 2011, 3, 4145. DOI: 10.1021/ol016693l
- Felpin, F.-X.; Fouquet, E. Chem. Eur. J. 2010, 16, 12440. doi:10.1002/chem.201001377
关联反应
关联书籍(日亚价格)
Greene’s Protective Groups in Organic Synthesis
- 著者Peter G. M. Wuts
- 参考価格¥ 12,342日元
- 出版社John Wiley & Sons Inc
外部链接
- Benzyl carbamates (Organic Chemistry Portal)
- Carboxybenzyl – Wikipedia
- Protecting Group (PG) (PDF)
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!





















No comments yet.