概要
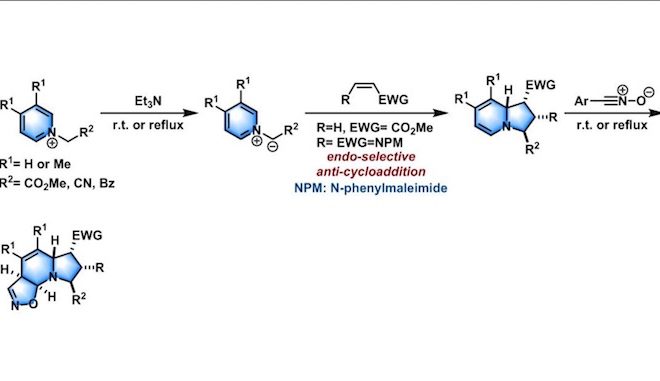
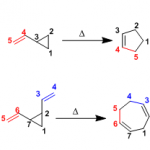
Tsuge反应(Tsuge reaction)是N-亚烷基吡啶鎓ylid或N-亚烷基异喹啉鎓ylid与烯基亲偶极体经过1,3-偶极环加成反应,产生不稳定的四氢中氮茚(tetrahydroindolizine)衍生物,随后,四氢中氮茚中的一个双键与腈氧化物进一步进行1,3-偶极环加成反应,形成稳定的I异噁唑稠合的四氢中氮茚类化合物的反应。该反应由日本九州大学(Kyushu university)的柘植乙彦(Tsuge Otohiko)研究组1985年首次报道,该反应具有高度的区域及立体选择性。
基本文献
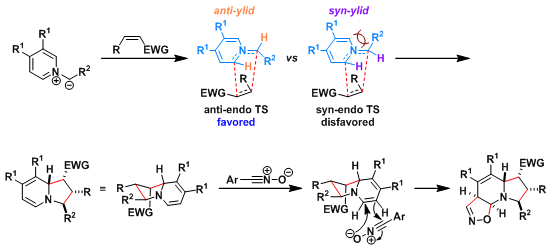
[1] O. Tsuge, S. Kanemassa, S. Takenaka, Bull. Chem. Soc. Jpn., 1985, 58, 3137. doi: 10.1246/bcsj.58.3137. [2] O. Tsuge, S. Kanemassa, S. Takenaka, Bull. Chem. Soc. Jpn., 1986, 59, 3631. doi: 10.1246/bcsj.59.3631.反应机理
反应实例
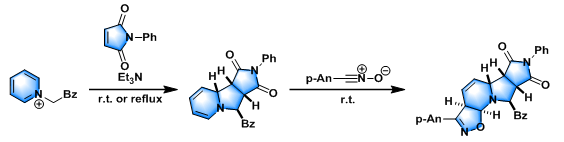
异噁唑稠合的四氢中氮茚类化合物的合成[1]
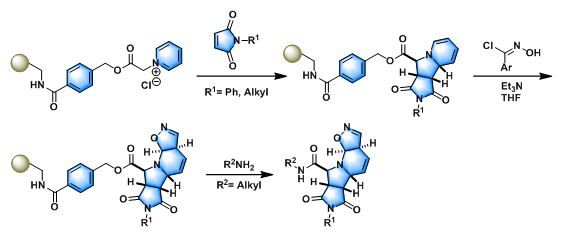
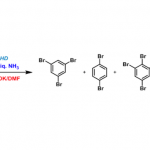
多组分固相Tsuge反应[2]
实验步骤
将三乙胺(2-4 eq.)加入到N-亚烷基吡啶鎓ylid前体(l eq.)与烯烃(l eq.)的无水二氯甲烷溶液(0.04-0.1 M)中。将上述反应混合物在室温或回流状态下进行搅拌10 min-6h (反应时间取决于不同的ylid及烯基亲偶极体底物)。再将上述混合物冷却至室温后,加入腈氧化物前体(l eq.),同时继续搅拌直至反应结束。反应结束后,将反应液倒入冰水中,并采用二氯甲烷进行萃取分液。将二氯甲烷相采用无水硫酸镁进行干燥后,减压除去溶剂。将粗产物采用硅胶柱色谱(正己烷/乙酸乙酯,5: 1 v/v到1:1v/v 作为洗脱剂)分离纯化,获得最终目标产物。
实验技巧
参考文献
[1] O. Tsuge, S. Kanemassa, S. Takenaka, Bull. Chem. Soc. Jpn., 1986, 59, 3631. doi: 10.1246/bcsj.59.3631. [2] P. Brooking, M. Crawshaw, N. W. Hird, C. Jones, W. S. MacLachlan, S. A. Readshaw, S. Wilding, Synthesis 1999, 1986. doi: 10.1055/s-1999-3615.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

















No comments yet.