作者:石油醚
引言
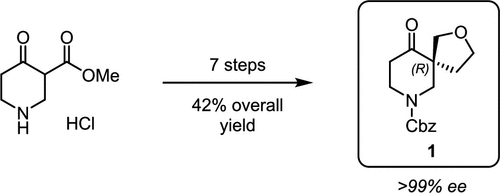
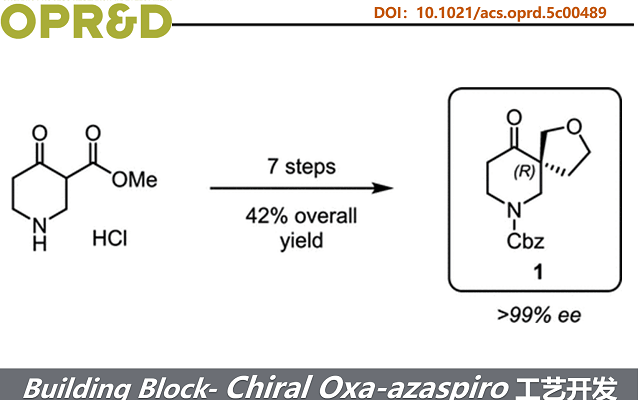
近日, Boehringer Ingelheim Pharmaceuticals公司开发一条不对称合成路线,高效制备benzyl (R)-10-oxo-2-oxa-7-azaspiro[4.5]decane-7-carboxylate (1)。该路线可直接放大,无需依赖制备型超临界流体色谱(SFC)拆分,显著优于传统消旋合成。
A Fit-for-Purpose Synthesis of a Chiral Oxa-azaspiro Building Block
Eugene Chong,* Alexander M. Haydl, Kirsty Anderson, and Sanjit Sanyal*
Org. Process Res. Dev. 2026. DOI : 10.1021/acs.oprd.5c00489
正文
螺环化合物不仅广泛存在于天然产物和药物中,还在药物研发中一直发挥着重要的作用。含氧、氮等杂原子的螺环骨架(如氧杂螺环、氮杂螺环)尤其受到合成化学界关注。其中,2-氧杂-7-氮杂螺[4.5]癸烷是一类具有药物合成价值的氮杂螺环骨架(Scheme1)。近日, Boehringer Ingelheim Pharmaceuticals公司开发一条不对称合成路线,高效制备benzyl (R)-10-oxo-2-oxa-7-azaspiro[4.5]decane-7-carboxylate (1)。该路线可直接放大,无需依赖制备型超临界流体色谱(SFC)拆分,显著优于传统消旋合成。
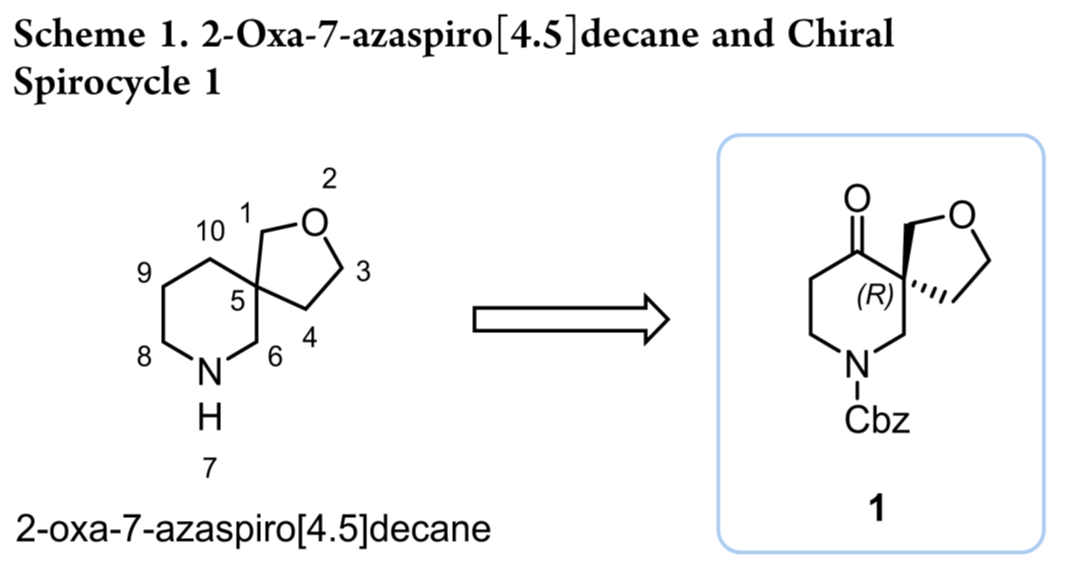
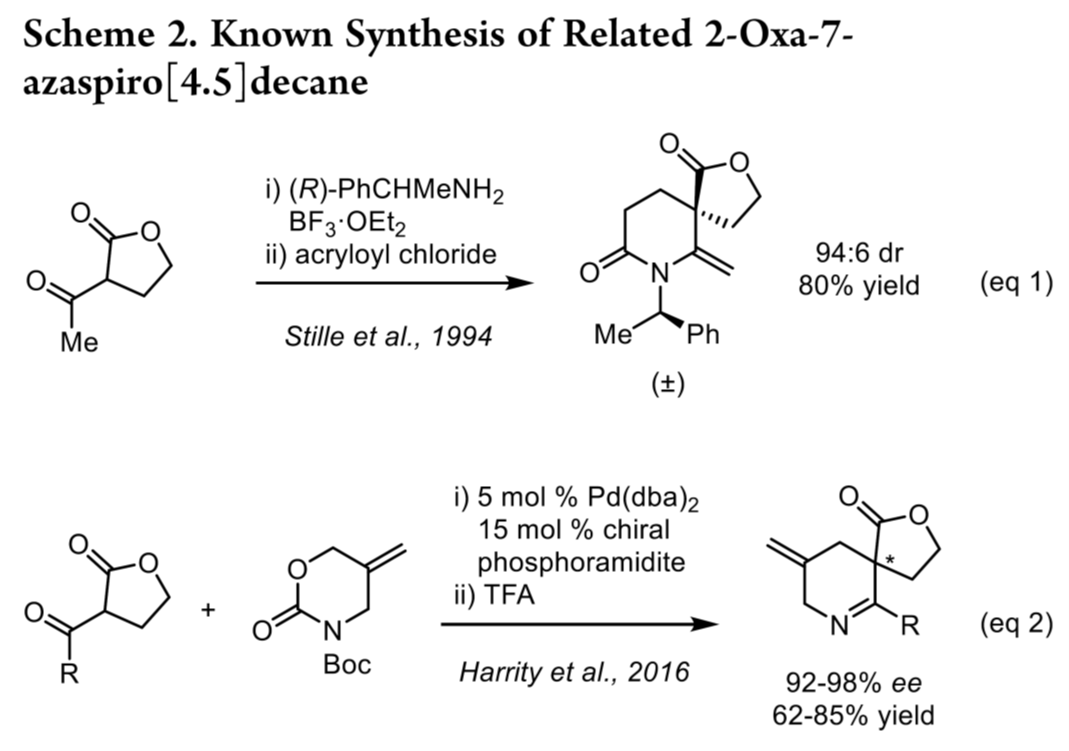
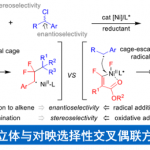
前人关于2-oxa-7-azaspiro[4.5]decane骨架的立体选择性合成报道极少,仅有手性辅助法(eq 1)和以2-氧代四氢呋喃-3-酮为原料的钯催化烯丙基化–缩合序列(eq 2)(Scheme 2)。然而,二者均需引入额外烯烃或内酯结构,导致适用性受限。Boehringer Ingelheim Pharmaceuticals的科学家另辟路径,不依赖四氢呋喃前体,对其进行逆合成分析(Scheme 3),即4-氧代哌啶底物4为原料,经钯催化不对称烯丙基烷基化(AAA)构建季碳中心3,3在通过缩酮保护及烯烃氧化/还原转化获得二醇2,2经Mitsunobu反应构建四氢呋喃结构,进而完成化合物1的百克级不对称合成。
首先,作者对钯催化不对称烯丙基烷基化(AAA)构建季碳中心进行了研究,如Table1。实验结果表明:6在(S,S)-DACH-Ph Trost配体与Pd催化的体系下反应6h,以92% ee和90%的产率(S)-Boc-7(Table 1,entry 2)。而将底物切换为N-Cbz取代的5,对映选择性仍达90–92% ee(entries 3–5)。进一步将Trost配体用量可降至1 mol%,烯丙基乙酸酯用量由1.5 equiv减至1.2 equiv(entry 4)同样可以反应。基于此条件,反应可将规模放大至279g,并以95%产率和92% ee转化得到产物3(entry 5),证实该条件具备百克级放大能力;但需在后续步骤中去除残余的对映体。
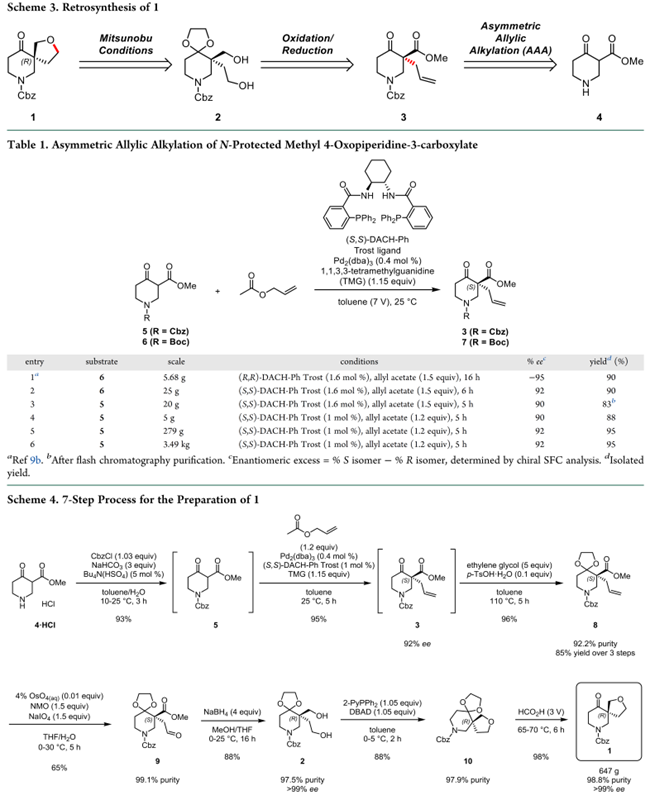
接下来,作者开发了一条以4•HCl为原料三步(Cbz保护、不对称烯丙基烷基化和缩醛保护)一锅法制备中间体8的工艺(千克规模)。即在甲苯/饱和NaHCO₃水溶液体系溶解4,并在TBAB存在下滴加CbzCl甲苯溶液,搅拌3 h;萃取、蒸馏后,以93% assay yield获得5的甲苯溶液。该溶液经氮气鼓泡除氧即可直接在0.4 mol% Pd₂(dba)₃ / 1 mol% (S,S)-DACH-Ph Trost配体的条件下发生AAA反应,以95% assay yield、92% ee高效生成3(Table 1,entry 6)。3在乙二醇/TsOH·H₂O体系下反应生成缩醛中间体8,前三步总收率达85%。此三步序列必须采用N-Cbz而非N-Boc保护:前者在酸性缩酮条件下稳定,后者则易发生Boc脱除及副反应。
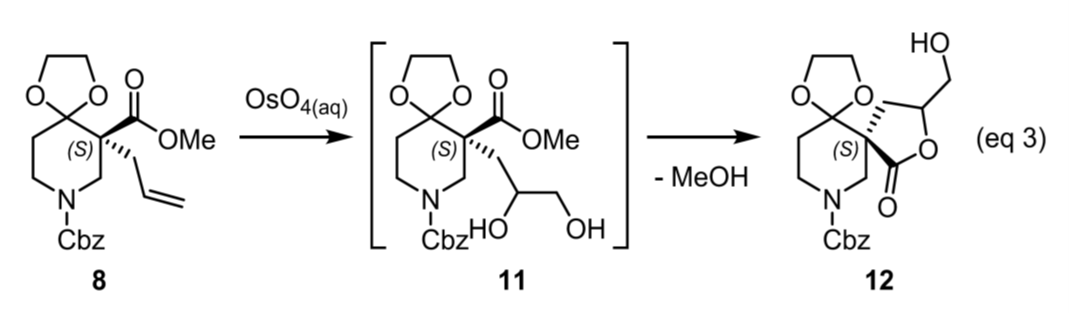
其次,作者对中间体8的氧化C−C键断裂工艺进行研究,进而通过闭环构建四氢呋喃环。结果表明:用Lemieux-Johnson氧化条件(催化OsO₄/NMO/NaIO₄),8可转化为9。进一步发现延迟加入NaIO₄会显著增加酯醇杂质12,通过优化加料顺序及后续操作可降低杂质12。即先加入NaIO₄促进二醇11裂解,再加入OsO₄与NMO。反应后经MTBE萃取、蒸馏得半固体粗品,再以1:6异丙醇/庚烷研磨结晶,同步去除残余对映体及杂质。该步骤可以2.16 kg规模,以65%收率、99.1% HPLC纯度获得9。该步虽收率中等,但完全规避手性SFC纯化。杂质12是原位生成的中间体11环化所致(eq 3)。
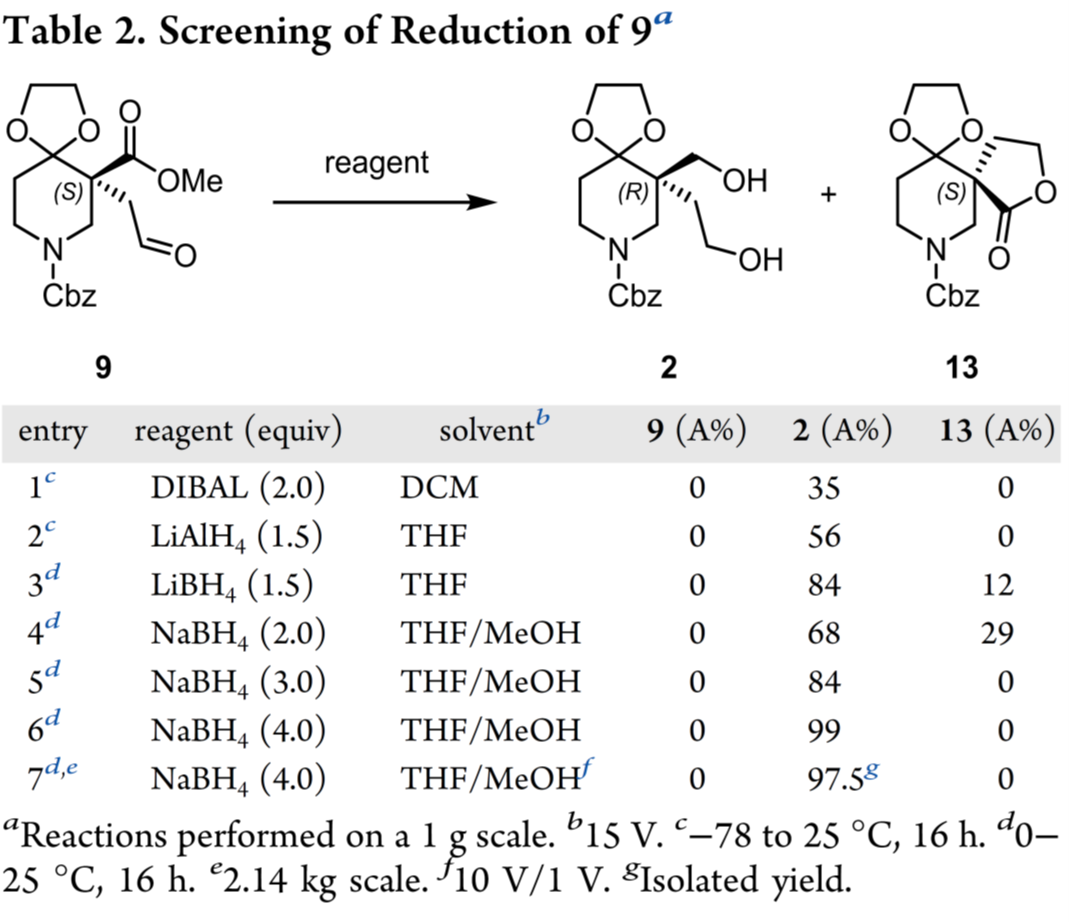
进一步对醛9的还原进行研究(Table 2)。实验结果表明:DIBAL或LiAlH₄收率低(entries 1–2);LiBH₄或NaBH₄转化改善,但仍残留内酯13(entries 3–4);将NaBH₄增至4 equiv,实现99 A%(HPLC面积归一化)的完全转化(enrty 6)。采用减少溶剂体积的体系下(THF 10 V / MeOH 1 V),该反应被放大至1.75 kg规模,得到二醇2( >99% ee)。2的ee测定结果证实:前步9的结晶已有效富集对映体纯度。
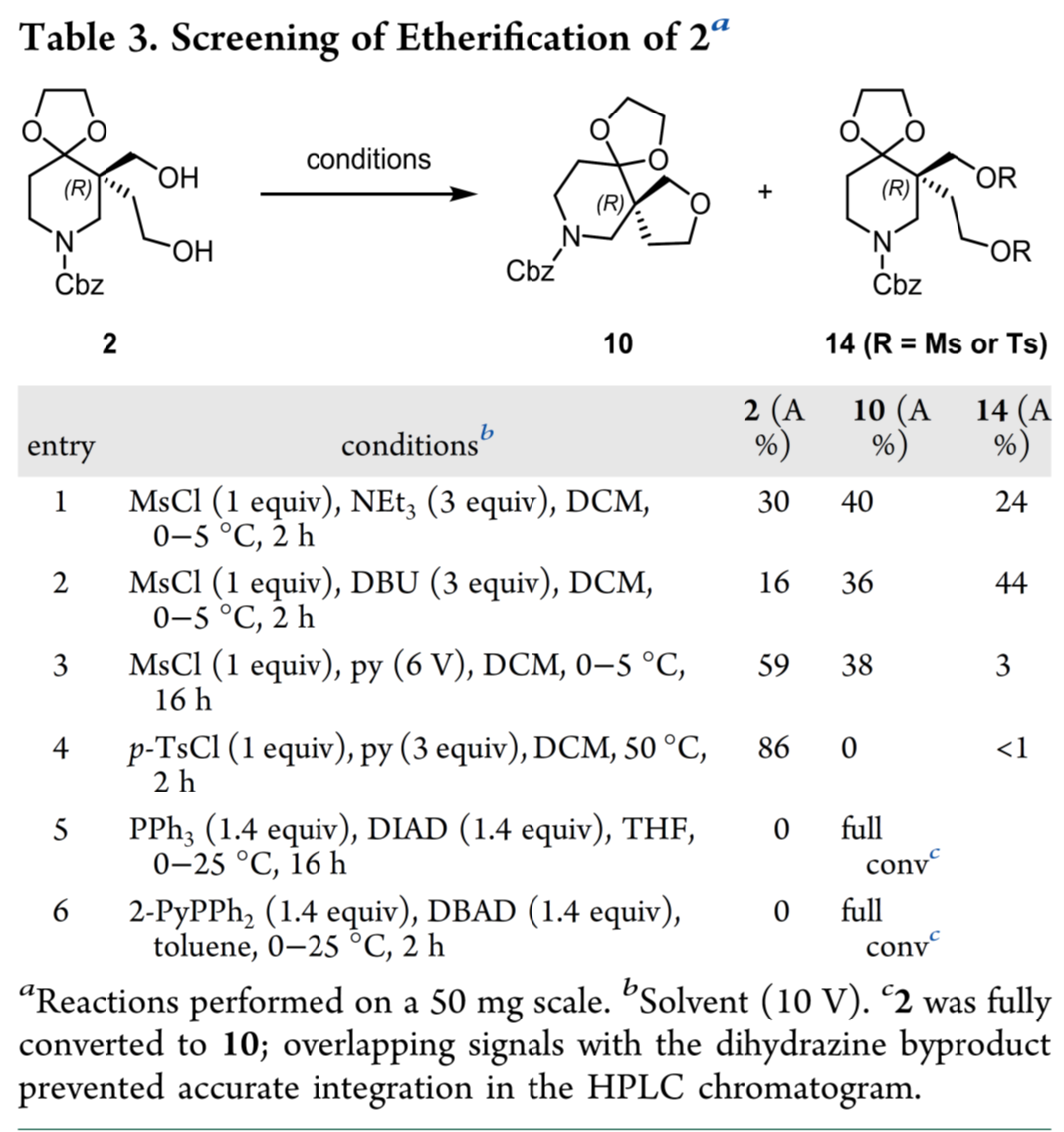
随后,作者对构建四氢呋喃结构进行了重点研究(Table 3)。初始尝试以MsCl或p-TsCl将其转化为磺酸酯,再经碱促进原位环化,但反应效果较差:生成双磺酸酯14且转化不完全(entries 1–4)。进一步筛选发现,Mitsunobu法效果最佳:PPh₃/DIAD组合成功环化(entry 5),但副产物的偶氮二甲酸二乙酯衍生物及三苯基膦氧化物难以去除。为此改用2-PyPPh₂/DBAD在甲苯中反应(entry 6):甲苯体系使副产物直接析出,可过滤除去;后续经EtOAc/甲基环己烷萃取及稀HCl水洗,有效去除磷氧化物及无机盐;残余DBAD副产物(~8–10%)可在下一步清除。放大至1 kg二醇2规模,并减低试剂用量(2-PyPPh₂与DBAD各1.05 equiv),以88%收率、97.9%纯度获得粗品10(Scheme 4)。
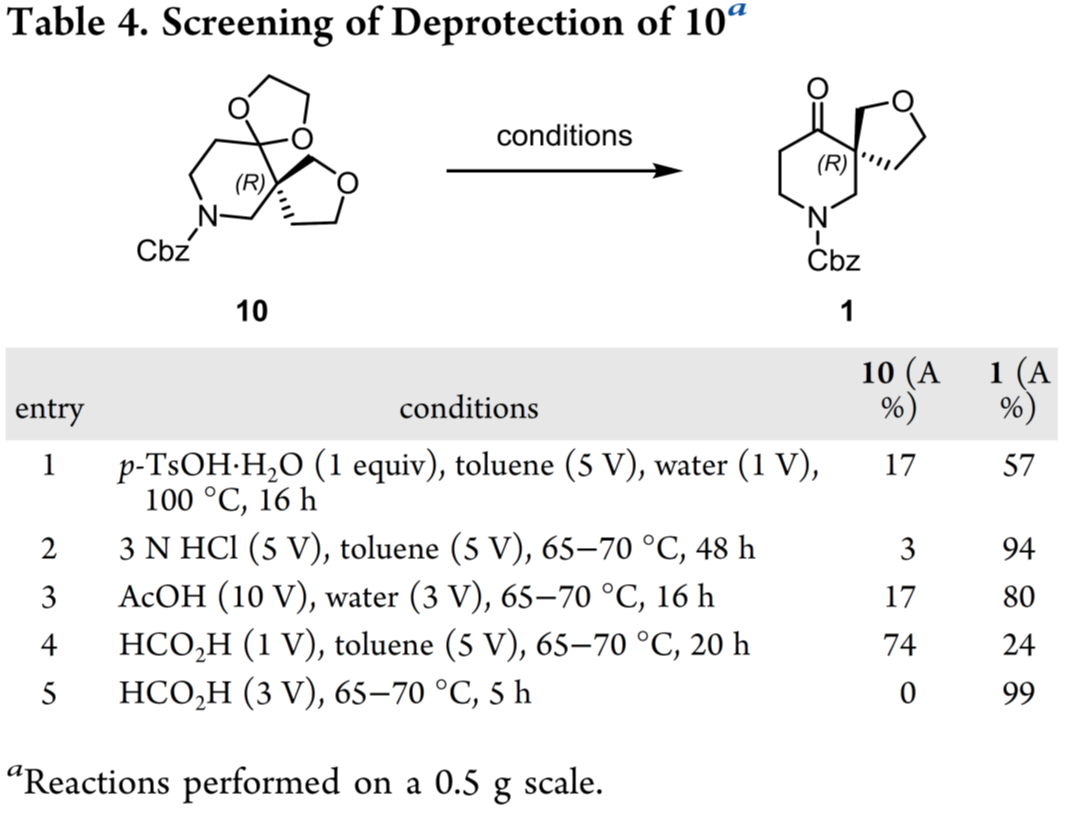
最后,对缩酮去保护制备1的工艺进行了研究(Table 4)。其中,1挥发性不足,无法蒸馏;又非结晶性固体,难以通过结晶纯化,进而需高效脱除10的保护基。即在100℃下,p-TsOH·H₂O在甲苯/水中反应,会导致转化不完全且1会发生降解(entry 1);改用65–70 °C的HCl或AcOH,转化改善但仍不彻底(entries 2–3);甲酸/甲苯体系转化率低(entry 4),而纯甲酸则实现完全、洁净脱保护(entry 5)。该条件用于10的最终脱保护。粗品经甲苯置换、饱和NaHCO₃溶液中和、活性炭脱色、氧化铝柱过滤及减压蒸馏,脱保护以98%收率获得1。最终得647 g浅黄色液体1, 98.8%纯度, 99.2% ee。
结论
Boehringer Ingelheim Pharmaceuticals公司开发一条不对称合成路线,以42%的总产率高效制备benzyl (R)-10-oxo-2-oxa-7-azaspiro[4.5]decane-7-carboxylate (1)。关键步骤采用不对称烯丙基烷基化,构建螺环季碳中心,初始ee ≥90%。尽管中间体多为脂肪族油状物,但固体中间体9可结晶,将ee提升至>99%,彻底避免制备型SFC分离。全程无需任何柱层析纯化——中间体及终产物1均经结晶或简单处理直接获得。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841
请登陆TCI试剂官网查看更多内容
https://www.tcichemicals.com/CN/zh/




















No comments yet.