作者:石油醚
引言
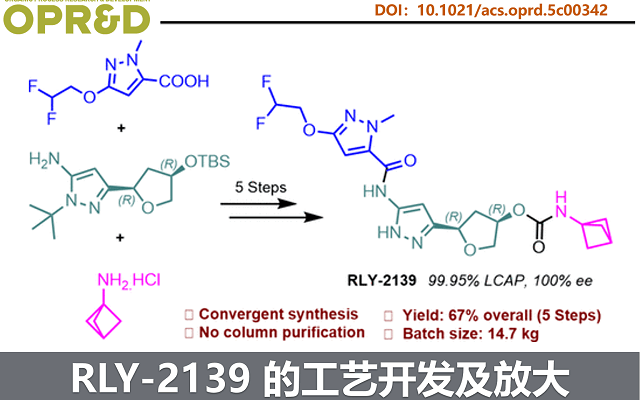
近日,Relay Therapeutics和康龙化等公司科学家合作成功开发出了一条适用于放大生产且低成本的 RLY-2139 合成路线,用于支持临床前及早期临床供应。该路线以中间体 1 和 2 偶联为起点,经脱保护和官能团转化得到终产物。关键工艺优化包括:以 CMPI 替代 T3P(提升操作安全性与可控性);以水相 TBAF 替代 HF·TEA(消除氢氟酸风险);以 DSC 替代苯基氯甲酸酯(避免酚类杂质,实现反应串联)。后期步骤重排显著改善杂质谱与工艺稳健性;柱层析被可放大的重结晶取代。该工艺已成功放大至多公斤级,累计交付 14.7 kg 高纯度 RLY-2139(从中间体 1 计,总收率 67%),LCAP ≥ 99.9%,对映体纯度 100%。
“Process Development and Scale-Up of RLY-2139: A Selective CDK2 Inhibitor Targeting ER+/HER2− Breast Cancer Seema Bag, Allen Qinglin Che, Andre Lescarbeau, Daniel Jones, Vishnu Karnati, Jing He, Alexander Merton Taylor, Charles Heap, Tim Briggs, Jianglin Colin Liang, Jay Larrow, Lingzhu Kong, Jin Zhang, Song Guo, Liyu Wang, Licheng Song,* and Surendra Singh*
Org. Process Res. Dev. 2026. DOI : 10.1021/acs.oprd.5c00342”
正文
RLY-2139 (Figure 1)是 Relay Therapeutics 开发的一种用于治疗ER+/HER2− 乳腺癌的高效选择性 CDK2 正构抑制剂。其通过选择性抑制 CDK2/细胞周期蛋白 E 复合物发挥作用,且该复合物是 CDK4/6 抑制剂耐药肿瘤中驱动细胞周期的关键因子。在HCC1569异种移植模型中,RLY-2139单药治疗在可耐受剂量下展现出强效抗肿瘤活性;其激酶选择性高、脱靶药理作用极低,且在预期人体剂量下几乎无细胞色素P450介导的药物相互作用风险。基于上述特性,RLY-2139已进入支持新药临床试验申请(IND)的临床前开发阶段,并将进一步评估其在乳腺癌联合治疗中的应用潜力。
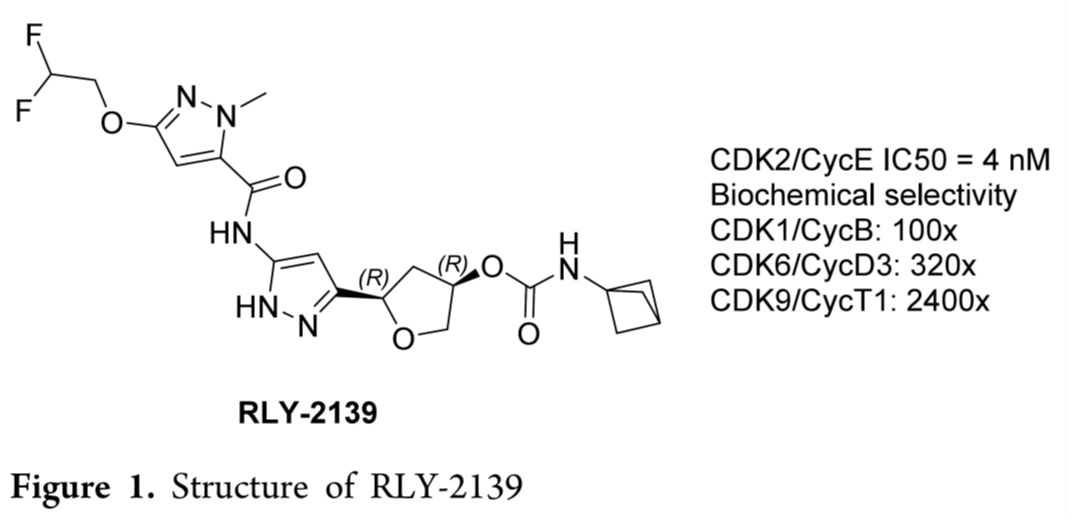
原药物化学路线(适用于早期研究,但难以放大并满足cGMP生产要求。本文报道了RLY-2139一条汇聚式四步合成工艺的开发与规模化:通过试剂优化、步骤重排、杂质全程控制及最终重结晶工艺建立,成功实现多公斤级高纯度、高收率结晶产品的稳定制备。
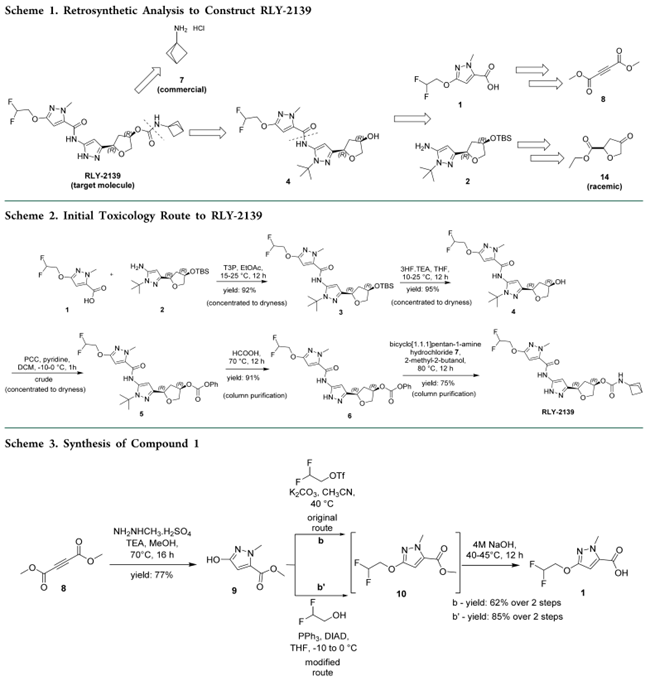
Scheme 1展示了早期发现阶段为支持PK和毒理学研究设计的逆合成路线。即RLY-2139采用模块化策略,由三个关键构建块(1、2、7)组装而成:化合物1由市售8经三步制得;化合物2由市售14经五步合成;构建块7(双环[1.1.1]戊烷胺盐酸盐)直接采购自供应商。
其中,化合物1的合成路线(Scheme 3):市售化合物8与甲基肼经Michael 加成和环化得到吡唑9,9与2,2-二氟乙醇经Mitsunobu反应得到10,10在碱性条件下发生皂化反应得到1 (65% overall yield)。化合物2的合成路线(Scheme 4):以马来酸二乙酯11为原料,经Michael加成和Dieckmann缩合反应合成13。13经脱羧获得14,14经金属催化氢化及TBS保护得15;后者在正丁基锂作用下与氰甲基化试剂反应,并与叔丁基肼环合生成2a;再经手性色谱拆分获得目标对映体2 (12% overall yield)。虽成功交付7 kg 2用于早期开发,但因效率与稳健性不足,不适用于后续放大。最终通过酶法手性拆分与不对称合成两条新路线,实现化合物2的多千克级GMP生产(Org. Process Res. Dev. 2026. DOI : 10.1021/acs.oprd.5c00354)。
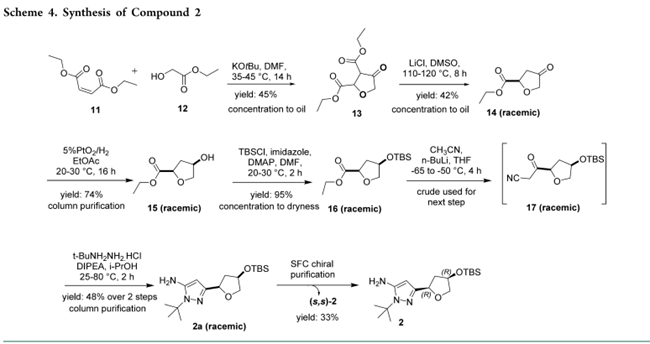
尽管初代化学路线(Scheme 2)成功交付950 g RLY-2139用于早期PK和毒理研究,但其存在多重根本性缺陷,无法满足放大及cGMP生产要求。关键问题在于:1)安全与监管风险:酰胺化使用T3P,需中国药监部门事前批准;TBS脱保护采用剧毒、强腐蚀性氢氟酸(HF),存在严重操作与工厂安全风险;2) 化学选择性差:碳酸酯活化使用苯甲酰氯,生成高活性中间体5,易水解返为醇4,并因试剂过量导致二酰化副产物;叔丁基脱除引发部分差向异构化;3) 工艺不可放大:“浓缩至干”用于前三步,缺乏可放大的纯化/分离工艺;后两步依赖低通量柱层析深度除杂,严重制约产能与稳健性。
为突破上述瓶颈、建立可放大且符合cGMP要求的工艺路线,重点实施两项改进:
- 试剂替代:以更安全、易得的试剂分别取代T3P和HF·TEA,提升操作安全性、监管合规性及工厂适用性;
- 碳酸酯活化优化:筛选温和活化剂替代氯甲酸苯酯,从源头抑制副产物生成,降低下游纯化难度。
- 序列优化:提前引入氨基甲酸酯基团,延迟脱保护至倒数第二步,提升杂质清除效率,规避高反应性中间体风险;
- 终局简化:重构最终脱保护路径,避免后期引入新结构单元(如7),显著降低杂质鉴定与控制难度,简化监管申报;
- 结晶替代层析:以稳健的重结晶工艺取代柱层析,同步实现晶型控制、纯度达标及工艺可放大。
该改进计划推动建立了可持续、全球适用的生产工艺,满足临床供应与商业化需求。基于此,作者对四步反应进行了优化(Scheme 5)。
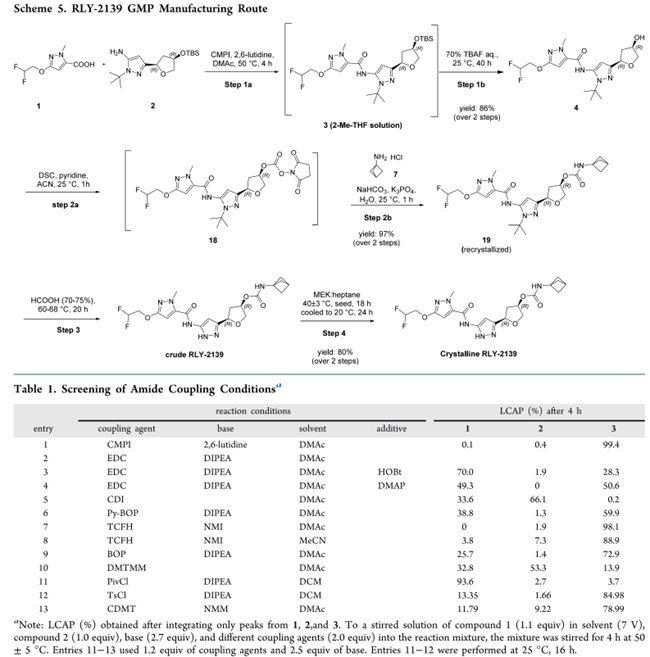
Step 1a: 酰胺缩合(1 + 2 → 3)
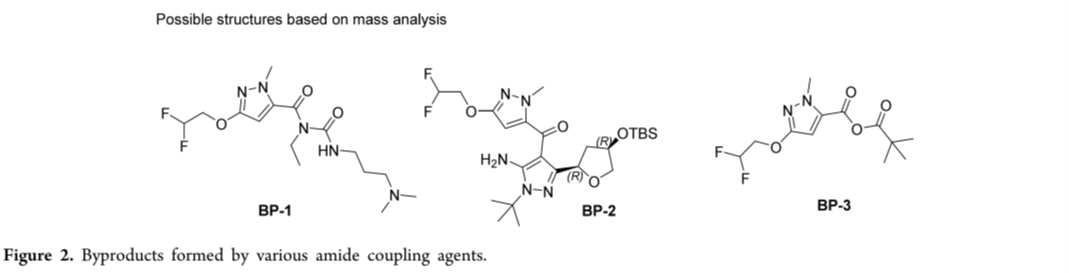
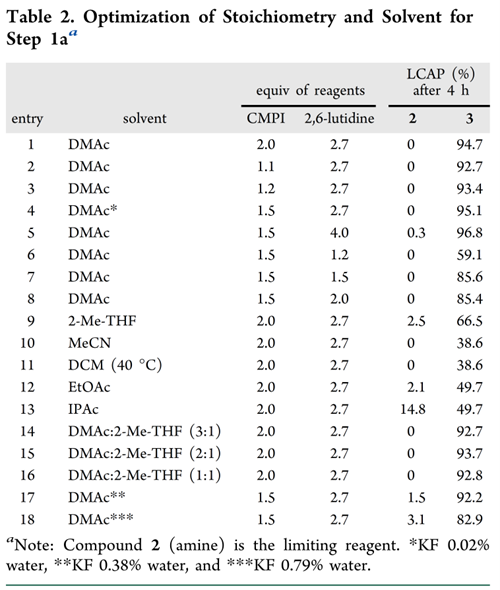
通过系统筛选(Table 1-2,Scheme 5),确定CMPI/2,6-路易斯碱/DMAc为最优偶联体系。其中,1)杂质溯源清晰:BP-1源于起始物料1与碳二亚胺试剂的副反应;TCFH虽得高纯产物,但引发酰基迁移生成BP-2;PivCl则导致过度酰化,主产BP-3(Figure 2);2)溶剂优选DMAc:MeCN、DCM、EtOAc转化不完全;DMAc/2-Me-THF混合体系无增益;3)工艺参数精控:CMPI 1.5 eq、2,6-路易斯碱 2.7 eq、50 °C、4 h,转化率>95%;CMPI<1.2 eq转化下降,过量碱诱发TBS脱保护;4)水分严控:KF ≤ 0.1 wt%(原料本底≤0.3 wt%,无需额外干燥);超限即显著降收;5)可放大性验证:公斤级运行稳定,化合物3不需分离,直接经水相处理+2-Me-THF共溶剂无缝衔接步骤1b。
Step 1b: TBS 脱保护(3 → 4)
原路线步骤2采用HF·TEA/THF脱除中间体3的TBS保护基(Scheme 2),虽有效但存在显著安全与操作风险,不适用于放大生产。基于此,在 70–75%水相用TBAF替代HF·TEA:
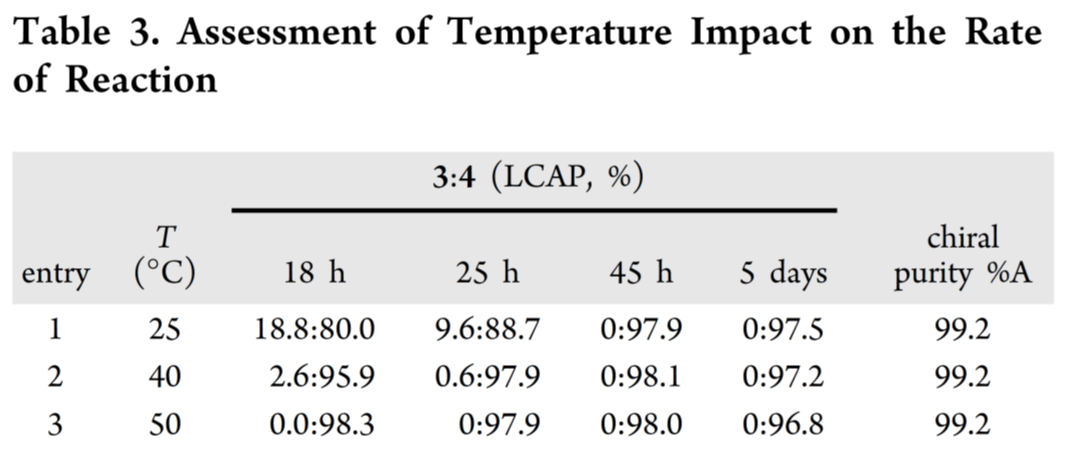
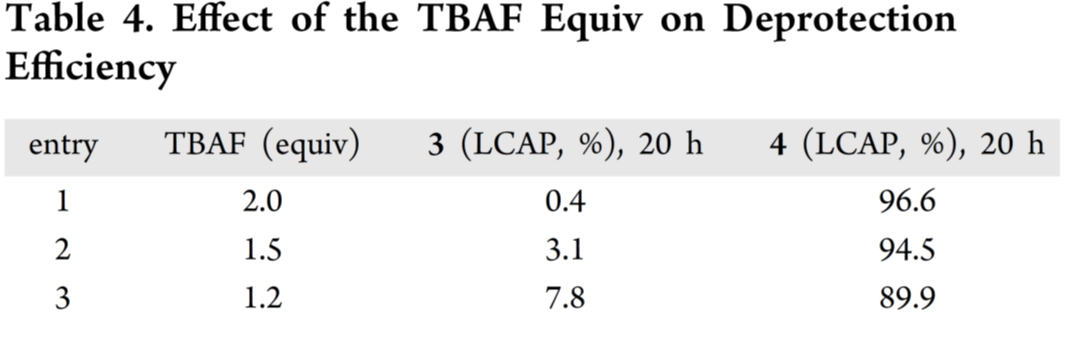
- 温度优化:20 °C需48 h;升至40 °C反应时间减半;热稳定性研究(Table 3)证实45 °C下批次稳定≥5天;最终确定45 °C、2.0 eq TBAF为最优条件,20 h内实现完全脱保护(Table4);
- 残留控制:TBAF残留会干扰下游反应;加标实验明确其携带限值;基于溶解度筛选(Table 5),采用20 wt% NaCl盐水洗涤——化合物4在此介质中溶解度最低(<0.1 mg/mL),可最大限度减少损失;两步盐水洗将TBAF残留从7655 ppm降至1831 ppm,满足工艺要求。

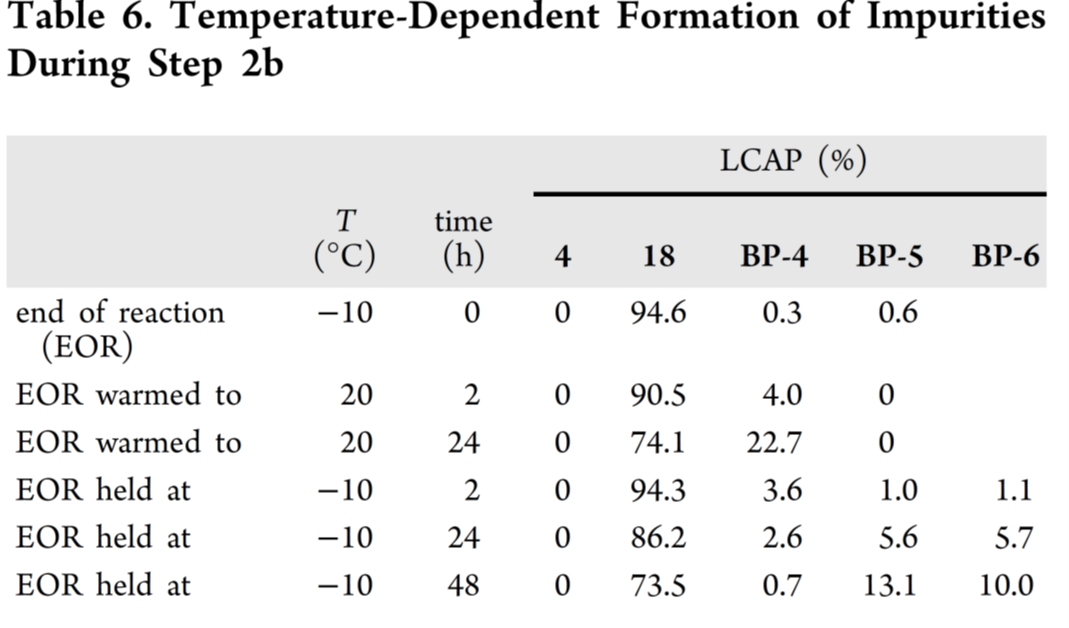
Step 2a:碳酸酯的形成(4 → 18)
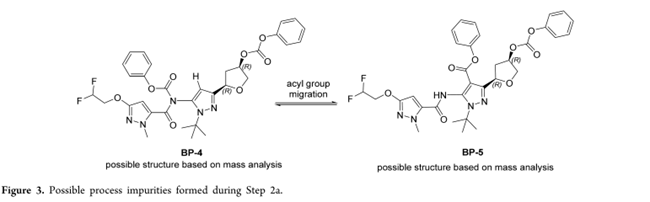
原毒理批次路线(Scheme 2)采用苯氯甲酸酯活化中间体4的伯醇,生成苯基碳酸酯5;但5在反应中显著降解,压力测试(Table 6)检出异构杂质BP-4/BP-5及未解析杂质BP-6(m/z = 732)(Figure 3);过量苯氯甲酸酯(1.4 eq)还引发二酰化副产物,下游纯化无法有效清除。
改用更温和、高选择性的N,N′-二琥珀酰亚胺碳酸酯(DSC)替代:1.3 eq DSC、1.4 eq吡啶、5 vol乙腈为最优条件,反应更洁净,产物碳酸酯18稳定性显著提升(Scheme 5)。
鉴于18对水敏感,反应直接对接步骤2b(telescoping),避免中间体暴露;加标研究确认中间体4水分须≤0.03%(w/w),以抑制水解、保障工艺稳健性。
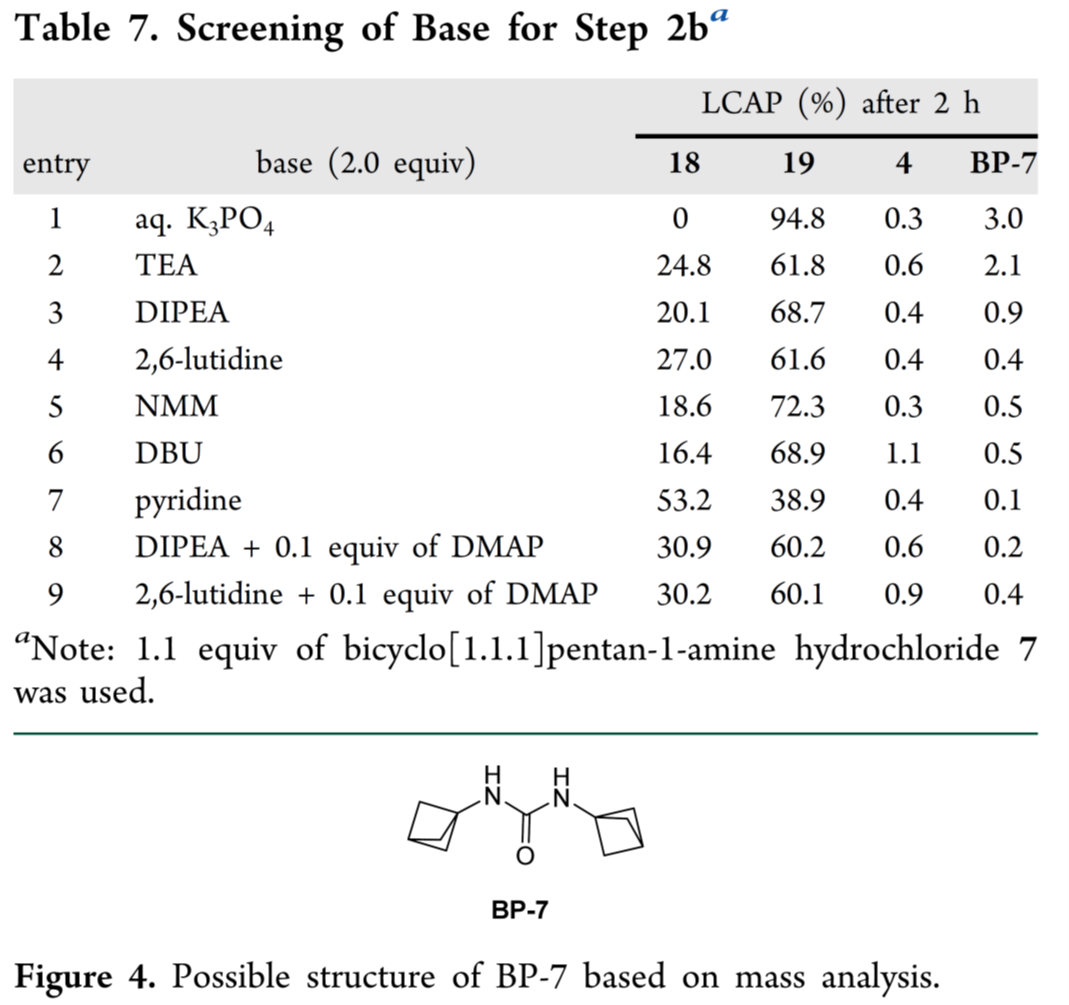
Step 2b:氨基甲酸酯形成(18 + 7 → 19)
- 路线重构:将双环[1.1.1]戊烷胺盐酸盐(7)提前至本步引入,脱保护延至后续步骤——既规避碱性条件下脱保护中间体的副反应,又满足监管对晚期杂质溯源与控制的要求;
- 反应优化:以K₃PO₄水溶液为碱,18与7发生高效亲核取代生成19(Scheme 5);主杂质BP-7源于19与过量7的二次反应;采用“先加水→再加7→最后加K₃PO₄”的加料顺序,最大限度减少18在碱性环境中接触过量亲核试剂,显著抑制BP-7;
- 结晶工艺:直接水淬得粘性固体,不可放大;经筛选,确立两相工作液(MeCN/水/ MTBE)→酸碱洗→浓缩→丙酮置换→控水析晶路径;关键控制点:MTBE残留<10%(防结块),丙酮交换彻底(终产品丙酮<20 ppm);最终实现多公斤级稳定生产,19纯度99.5%(LCAP),2a+2b总收率97%。
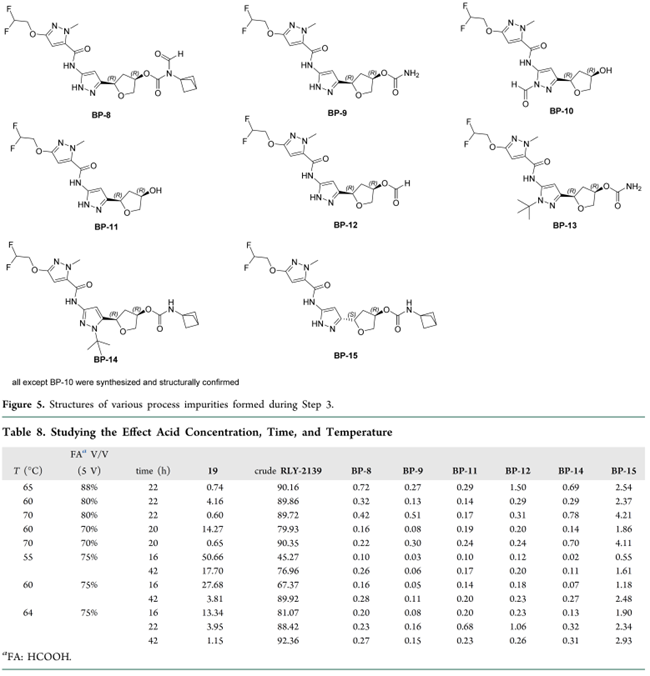
步骤3:叔丁基脱保护(19 → 粗品 RLY-2139)
- 酸筛选广谱但甲酸最优:系统评估甲磺酸、TFA、TsOH、ZnCl₂等十余种Brønsted/Lewis酸及多种溶剂,确认原路线所用甲酸仍为最佳选择;
- 杂质主控点明确:关键风险为甲酰化、水解及C-手性中心差向异构化(Figure 5),强酸/高温/延长时间均加剧杂质积累(Table 8);
- 工艺窗口精准锁定:75%水合甲酸、60–68 °C为放大条件——兼顾完全转化、杂质<0.15%、立体化学完整性100%;
步骤4:RLY-2139重结晶(晶型2)
- 溶剂体系:MEK/n-heptane(1:2.75 v/v)最优——溶解度适中、析油风险低、多晶型转化损失<2%;惰性气氛全程防氧化;
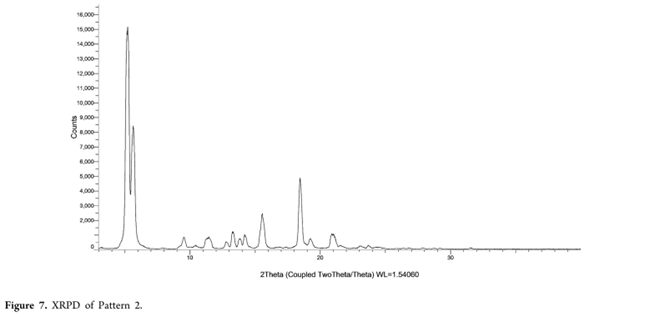
- 固体特性:针状晶体;PLM与XRPD证实晶型2(Figure 6–7);TGA显示95–150 °C失水1.8%,DSC在~130 °C呈单一吸热峰(Figure 8);


- GMP路线总览(方案5):16.9 kg 1 + 11.3 kg 2 → 14.7 kg RLY-2139(单批),纯度99.95%(LCAP)、对映体纯度100%,总收率67%(含5步化学转化+重结晶);
- 性能跃升:较Tox批次,GMP路线杂质更低、收率更高、操作更稳健(Table 9)。
总结:
Relay Therapeutics和康龙化等公司科学家合作成功开发出了一条适用于放大生产且成本效益高的 RLY-2139 合成路线。优化后的工艺相比原始路线有了显著改进,从而形成了一个稳健的生产流程。关键的改变,例如用更安全、更易管理的试剂替代 T3P、HF·TEA 和苯基氯甲酸酯,使得反应更清洁、条件更温和、步骤更紧凑。无需柱层析纯化,产品就能以 99.95%(LCAP)的高纯度分离出来。中间体的分离数量减少,简化了工艺流程,同时批次产量增加了 5 倍,每公斤成本降低了 80%。此外,GMP 生产的前置时间从六个月缩短至三个月,使优化后的路线更高效、更具可扩展性且更具商业可行性。
相关链接:
手性分离到不对称合成: RLY-2139 手性四氢呋喃-吡唑胺中间体的路线探索及早期工艺开发
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
关注Chem-Station抖音号:79473891841
请登陆TCI试剂官网查看更多内容
https://www.tcichemicals.com/CN/zh/
















No comments yet.