本文作者:杉杉
导读
近日,南京大学朱少林教授课题组在ACS Catal.上发表论文,报道了在温和的条件下,以N-氟代双苯磺酰胺(NFSI)作为氟化试剂,实现未活化烯烃的氢氟化反应(hydrofluorination),获得Markovnikov氟氢化产物。同时,该反应不受空气或湿气的影响,并使用廉价且易得的镍化合物作为催化剂。值得注意的是,与先前NiH催化烯烃加氢官能团化的途径不同(离子途径),该反应通过氢原子转移途径进行。
Nickel-Catalyzed Hydrofluorinatio of Unactivated Alkenes througha HAT Pathway
Peihong Song and Shaolin Zhu*
ACS Catal.2020, 10, 13165-13170
正文
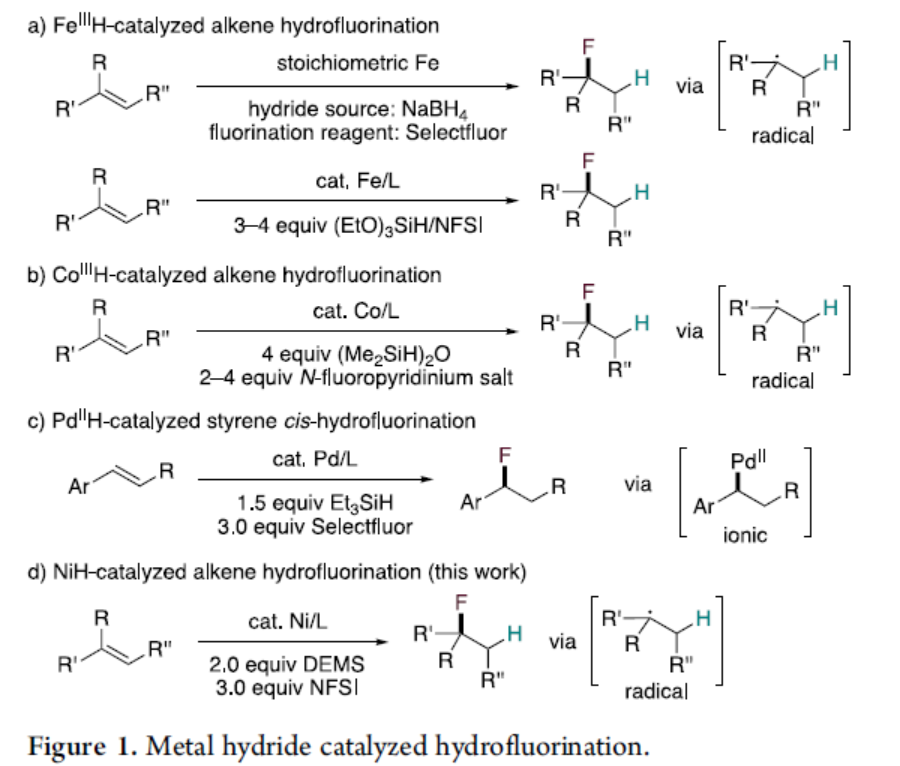
由易得的烯烃生成C-F键的氢氟化反应,是合成氟化分子的有效方法。在经典的酸催化反应中,使用质子作为氢源,可将氟化氢直接加成到烯烃中,并已取得一定的成果。但该类反应存在一定的局限性,如强酸的使用、底物范围有限、官能团耐受性低等。为了克服此类问题,Nicewicz[1]课题组报道了利用吖啶(acridinium)氧化还原催化策略,实现苯乙烯的anti-Markovnikov氟化反应。Barker和Boger等[2]使用NaBH4作为氢源,Selectfluor作为氟化试剂,在化学计量的Fe的作用下,实现了各种未活化烯烃的自由基氢氟化过程(Figure 1a, top)。2019年,Ye和Li等[3]通过铁催化也实现了上述的反应(Figure 1a, bottom)。随后,Shigehisa和Hiroya等[4]报道了使用钴催化实现此类转化(Figure 1b)。此外,Gouverneur[5]课题组报道了钯催化苯乙烯的氢氟化反应(离子途径,不同于上述自由基途径)。2020年,Lei和Liao等[6]进一步开发出一种不对称反应形式(Figure 1c)。基于对NiH催化的迁移性烯烃加氢官能化的持续兴趣,在此,南京大学朱少林教授课题组报道了一种通过镍催化,可在温和的条件下,实现未活化的烯烃的氢氟化反应(Figure 1d)。
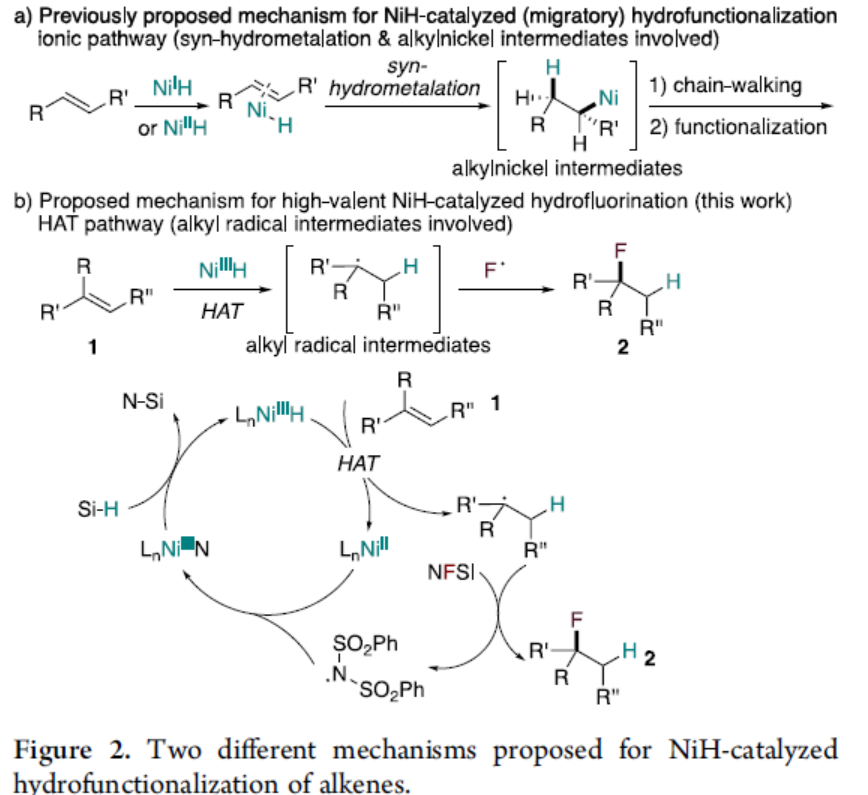
镍成本低廉且具有多种氧化态,可作为偶联反应的高效催化剂。最近报道的还原性NiIH或氧化还原NiIIH催化的迁移性加氢官能化,可将各种官能团直接引入烯烃中,涉及将NiIH或NiIIH化合物插入烯烃中以形成烷基镍配合物,再进一步官能化,获得相应的产物(Figure 2a)。但另一方面,对NiH与烯烃的氢原子转移(HAT)途径研究相对较少。在类似于CoIIIH和FeIIIH催化的过程中,在硅烷和N-氟苯磺酰亚胺(NSFI)存在时,原位生成的高价氢化镍(NiIIIH)可与未活化的烯烃进行HAT,同时发生C-中心自由基的形成(Figure 2b)。
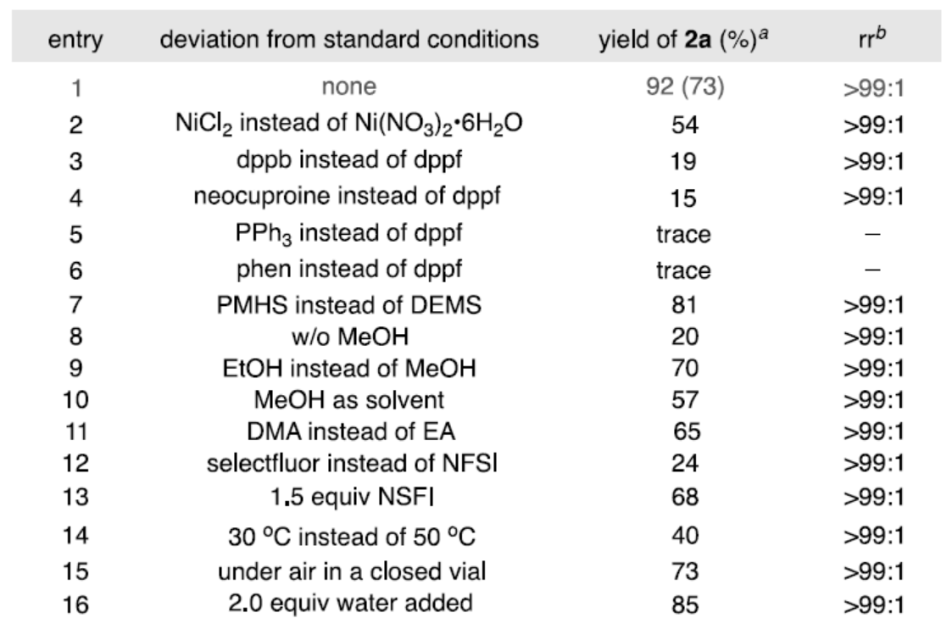
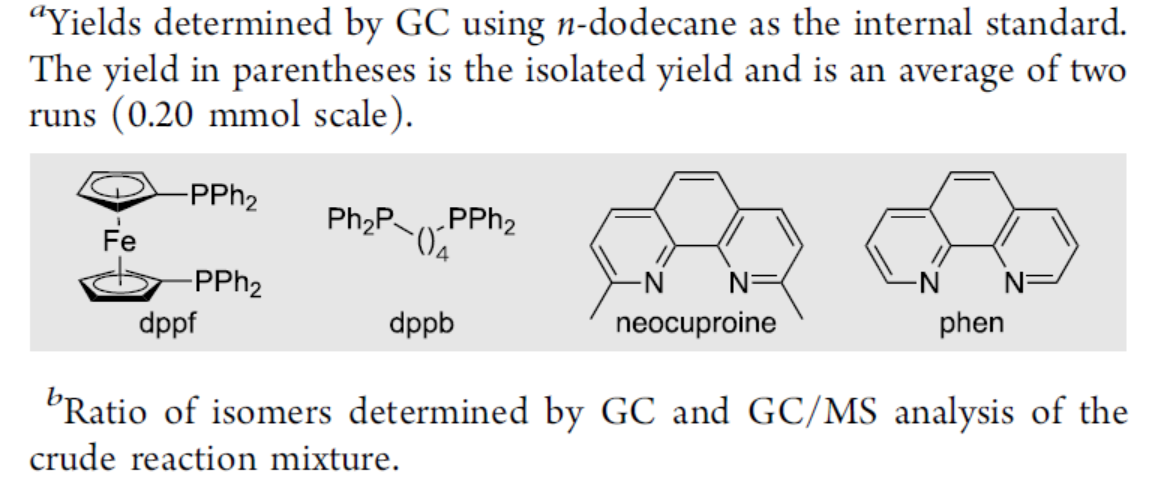
首先,作者以4-苯基-1-丁烯(1a)和NSFI作为模型底物,进行了相关反应条件的筛选,如镍源、配体、氢化物源、溶剂等(Table 1)。反应的最佳条件: Ni(NO3)2•6H2O作为催化剂,dppf(1,1′-二茂铁基双-(二苯基膦))作为配体,二乙氧基(甲基)-硅烷(DEMS)作为氢化物源,可获得所需的Markovnikov氟化氢产物(2a),为单一区域异构体,收率为73%。
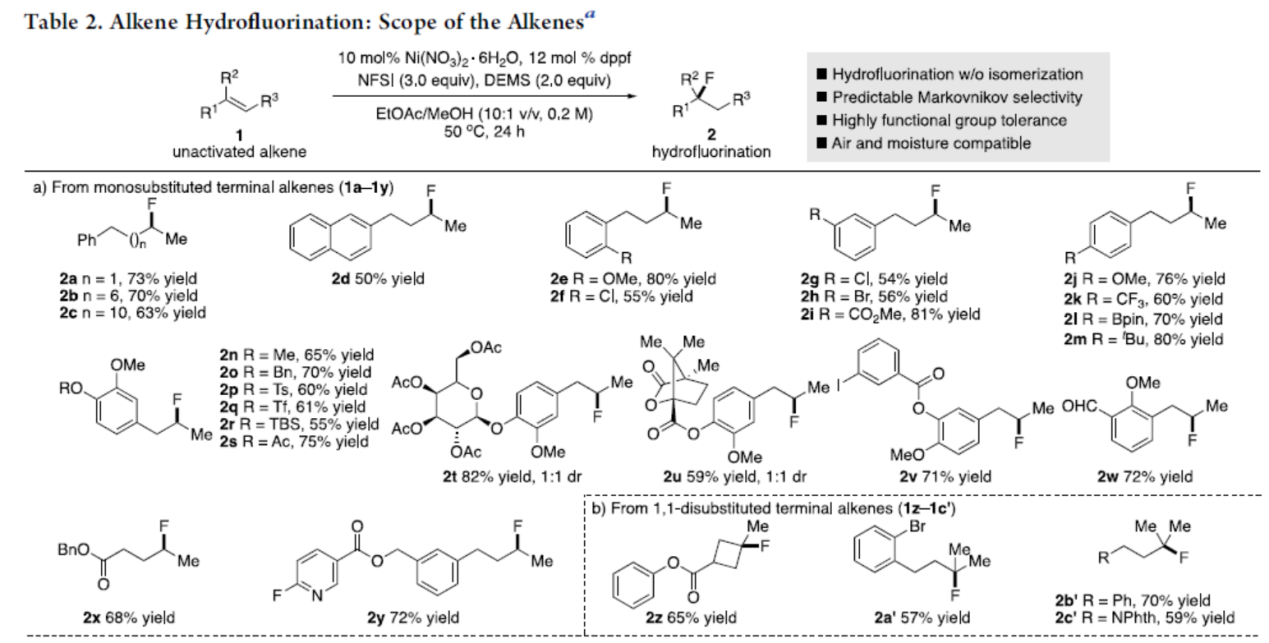
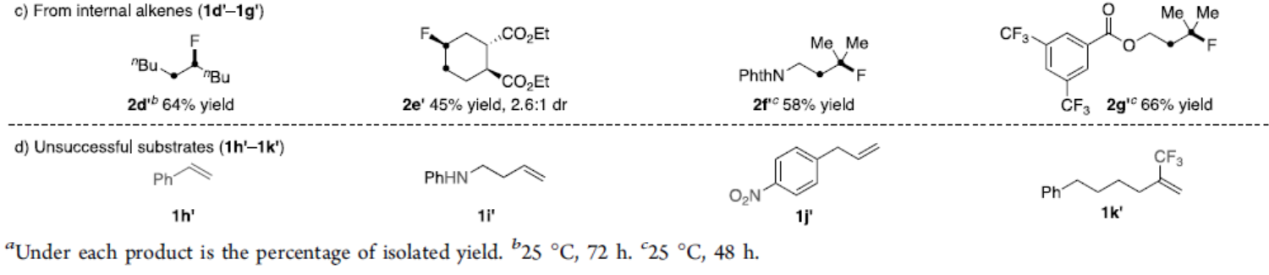
在获得上述最佳反应条件后,作者开始对烯烃底物1进行了扩展(Table 2)。通常,该反应的区域选择性非常好,在所有情况下仅观察到一种区域异构体,且未观察到烯烃异构化或氢氟酸迁移。各种未活化的末端烯烃,如单取代的烯烃(1a-1y)和1,1-二取代的烯烃(1z-1c’)均以优异的收率获得相应的氢氟化产物。同样,可很好的耐受芳基(1a-1d)、醚(1e,1j,1n,1o,1r,1t-1w)、酯(1i,1sv和1xz)、邻苯二甲酰亚胺(1c ‘)以及易还原的官能团(如醛(1w))等。值得注意的是,使用芳基氯化物(1f,1g)、芳基溴化物(1h,1a’)、碘化芳基(1v)、三氟甲磺酸芳基酯(1q)和硼酸频哪醇酯(1l)时,同样取得较好的结果,为后期交叉偶联提供了多种可能。此外,对杂环(如吡啶(1y))、葡萄糖苷衍生物(1t)和(-)-樟脑酸(1u)衍生物,也成功地进行了氢氟化。同时,未活化的内烯烃(1d’-1g’),如1,2-二取代的烯烃(1d’,1e’)和三取代的烯烃(1f’,1g’),也均取得良好的结果。
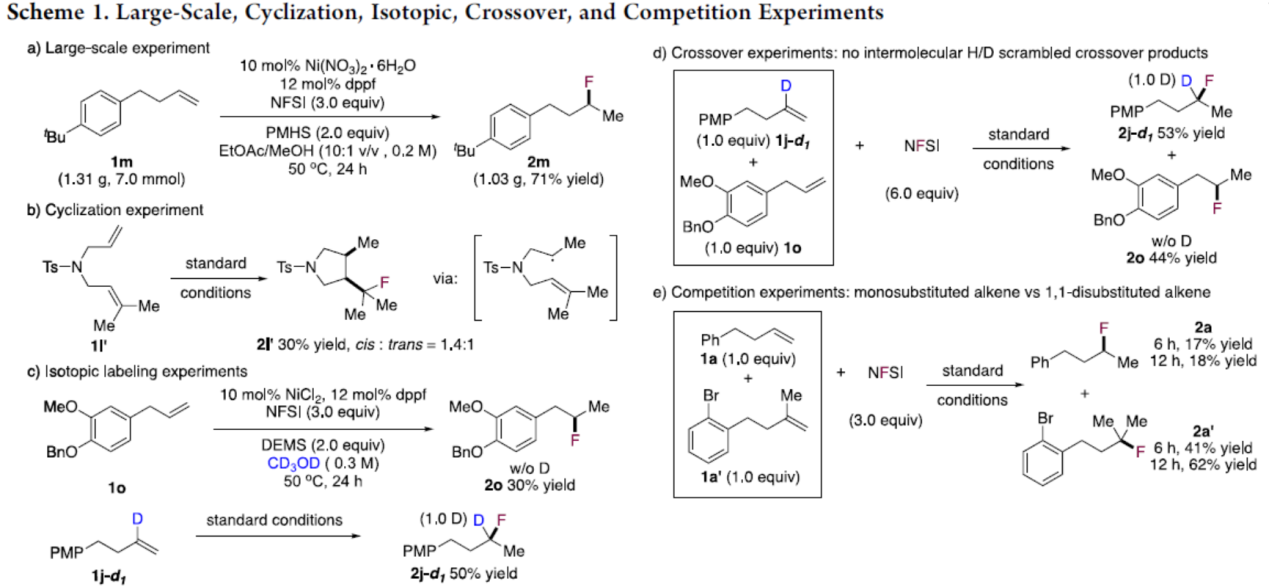
作者使用廉价的聚甲基氢硅氧烷(PMHS)作为硅烷源,进行了2m的克级实验,同样取得了较好的结果(Scheme 1a)。随后,为了进一步了解反应的机理,进行了相关的对照实验。通过分子内捕获的反应,获得30%收率的环化产物(2l’),表明反应涉及烷基自由基的参与(Scheme 1b)。当使用CD3OD作为溶剂时,在2o中未观察到氘掺入(Scheme 1c, top)。与先前报道的NiH催化的迁移氢官能化不同,该反应条件下未发生链行走过程(Scheme 1c, bottom)。同时,在交叉实验中未观察到分子间H/D的交叉产物,进一步证明了上述推测的正确性(Scheme 1d)。最后,通过竞争实验比较单取代烯烃(1a)和1,1-二取代烯烃(1a’)的相对反应性(1a’ > 1a),反应结果表明反应涉及自由基(HAT)途径(Scheme 1e)。
总结
南京大学朱少林教授课题组开发了一种利用简单且商业可得的镍催化剂,在温和的条件下,以N-氟代双苯磺酰胺(NFSI)作为氟化试剂,催化的未活化烯烃的氢氟化反应,具有广泛底物范围。并且,该反应涉氢原子转移(HAT)途径过程,而非离子途径。
参考文献
(1) Wilger, D. J.; Grandjean, J.-M. M.; Lammert, T. R.; Nicewicz, D. A. The Direct anti-Markovnikov Addition of Mineral Acids to Styrenes. Nat. Chem. 2014, 6, 720-726.
(2) Barker, T. J.; Boger, D. L. Fe(III)/NaBH4-Mediated Free Radical Hydrofluorination of Unactivated Alkenes. J. Am. Chem. Soc. 2012, 134, 13588-13591
(3) Xie, Y.; Sun, P.-W.; Li, Y.; Wang, S.; Ye, M.; Li, Z. Ligand-Promoted Iron(III)-Catalyzed Hydrofluorination of Alkenes.Angew.Chem., Int. Ed. 2019, 58, 709-7101.
(4) Shigehisa, H.; Nishi, E.; Fujisawa, M.; Hiroya, K. Org. Lett.2013, 15, 5158-5161.
(5) Emer, E.; Pfeifer, L.; Brown, J. M.; Gouverneur, V. cis-Specific Hydrofluorination of Alkenylarenes under Palladium Catalysis throughan Ionic Pathway.Angew.Chem., Int. Ed. 2014, 53, 4181−4185.
(6) Yin, X.; Chen, B.; Qiu, F.; Wang, X.; Liao, Y.; Wang, M.; Lei, X.; Liao, J. Enantioselective Palladium-Catalyzed Hydrofluorination of Alkenylarenes. ACS Catal.2020, 10, 1954-1960.

























No comments yet.