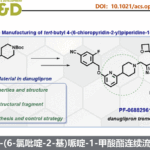
标题论文报道了芳基碘的选择性交叉偶联。作者通过使用新型阳离子三核钯催化剂,可以再C-Br和C-Cl键存在下选择性地对C–I进行偶联反应。
C–I键的选择性偶联反应
如果可以选择性对如碘,溴或氯位点进行偶联反应,则可以快速合成高度官能化的化合物。代表性的例子之一,Fu等人通过使用不同的Pd的催化剂实现了与C-Cl与C-OTf的选择性偶联反应[1](图1A)。另一方面,C–I与C–Br的选择性偶联还未能够解决。Knochel等人使用缺电子的磷配体进行Negishi偶联,虽然在C–Br存在下实现了C–I的选择性偶联、但是只有以对溴苯为底物的两个应用例,还不能说可以作为一般的应用方法使用[2a](图1B)。因此,使用Pd(0)催化剂进行的C–I选择性偶联对底物限制很大是一个巨大的局限。基于此,Molander等人使用Ni/Photoredox催化体系,实现了在C–Br存在下进行C–I选择性烷基化偶联反应,然而该反应不适用于sp2亲核剂[2b](图1B)。
另一方面,本次介绍的论文的作者Schoenebeck等人,开发出了Pd(I)二聚体1、并且使用该二聚体催化剂实现了C–Cl, C–Br以及C–OTf键的选择性偶联反应[3](图1C)。而这次,他们又使用阳离子三核Pd催化剂、在Grignard 试剂作用下,实现了C–I键的高产率・高选择性偶联反应(图1D)。
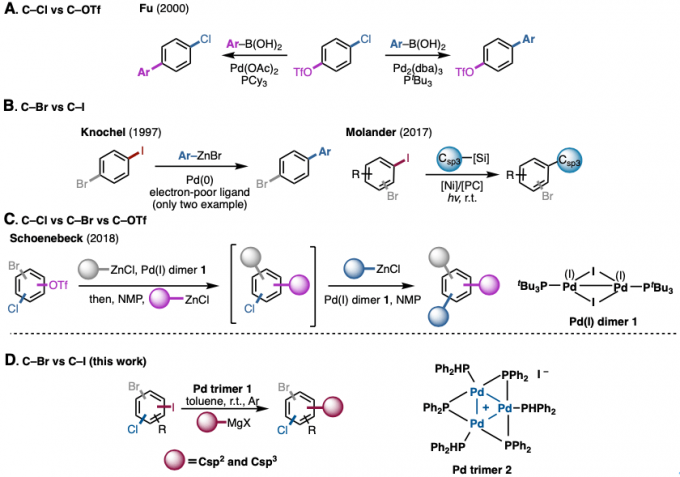
图1. (A), (B), (C) 常规多卤代芳烃的区域选择性偶联 (D) 本次介绍的反应
“C–I Selective Cross-Coupling Enabled by a Cationic Pd Trimer”
Diehl, C. J.; Scattolin, T.; Englert, U.; Schoenebeck, F. Angew. Chem., Int. Ed.2018, Accepted Article
论文作者介绍
履历:
2001–2004 BSc, Technical University Berlin, Germany and University of Strathclyde, Glasgow, UK
2004–2008 Ph.D, WestCHEM Research School, Glasgow, UK (Prof. John A. Murphy)
2008–2010 Posdoc, University of California, Los Angeles, USA (Prof.K. N. Houk)
2010–2013 Assistant Professor, ETH Zürich, Switzerland
2013– Professor (W2), RWTH Aachen University, Germany
研究内容:计算化学与使用计算化学进行的催化剂设计
论文概要
本反应中使用的三核Pd催化剂2、可以通过在Pd(I)二聚体1中加入4当量二苯基膦制备,产率达到99%(图2A)。得到的催化剂2对空气,水稳定。接下来,作者研究了底物1-溴-4-碘苯(3a)和PhMgCl(4a)在催化剂2作用下与其他一般Pd催化剂作用下的选择性偶联反应活性(图2B)。作者发现、Pd(0)催化剂以及Pd(I)二聚体催化剂1的反应,偶联同时能发生在C-Br与C-I键上,副产物为双偶联化合物6。
另一方面、使用三核Pd催化剂2的反应中、完全没有副产物6的形成,反应选择性的发生在C–I键上生成了4-溴联苯(5a),产率高达88%。另外,即使在in-situ下生成催化剂2进行的催化反应,也显示了同样的反应活性。该反应条件底物适用性广、即使使用邻位二取代化合物(5e),也能以高产率进行反应(图2C)。另外,使用烷基取代的Grignard试剂(5g, 5h)也能进行反应。通过EPR解析作者确认在该反应中不存在长寿命的自由基。同时,通过DFT计算,三核催化剂2是直接进行氧化加成催化的反应。
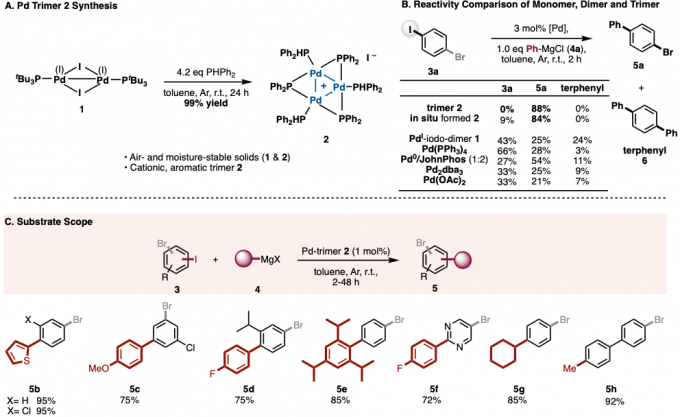
图2. (A) 三核Pd催化剂2的合成 (B) 各Pd催化剂的反应性 (C) 底物适用范围
综上所述,在三核Pd催化剂催化下,作者实现了C-I选择性偶联反应。同时催化剂的稳定性很高,今后很可能作为卤代化合物的偶联反应催化剂被广泛使用。
参考文献
- Littke, A. F.; Dai, C.; Fu, G. C. J. Am. Chem. Soc.2000, 122, 4020 DOI: 10.1021/ja0002058
- (a) Betzemeier, B.; Knochel, P. Angew. Chem., Int. Ed. Engl. 1997, 36, 2623 DOI: 10.1002/anie.199726231(b) Lin, K.; Wiles, R. J.; Kelly, C. B.; Davies, G. H. M.; Molander, G. A. ACS Catal. 2017, 7, 5129. DOI: 10.1021/acscatal.7b01773
- Keaveney, S. T.; Kundu, G.; Schoenebeck, F. Angew. Chem., Int. Ed. 2018, 57, 12573. DOI: 10.1002/anie.201808386
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!















No comments yet.