本文作者:杉杉
导读
烷基氯化物作为一种稳定的亲电试剂,在过渡金属催化中仍未被充分利用。近日,普林斯顿大学David W. C. MacMillan教授课题组在美国化学学会杂志(Journal of the American Chemical Society)发表论文,报道了一种新型有机硅烷试剂,可在温和的光催化条件下进行烷基氯原子的抽取,从而克服C(sp3)-Cl键活化的限制。该反应涉及镍/光氧化还原双重催化循环的机理,同时首次实现了未活化烷基氯和芳基氯的亲电偶联反应。此外,该反应可使用一些低毒、丰富且市售的有机氯化物作为底物,从而合成了各种具有高度官能化的C(sp2)-C(sp3)偶联产物。
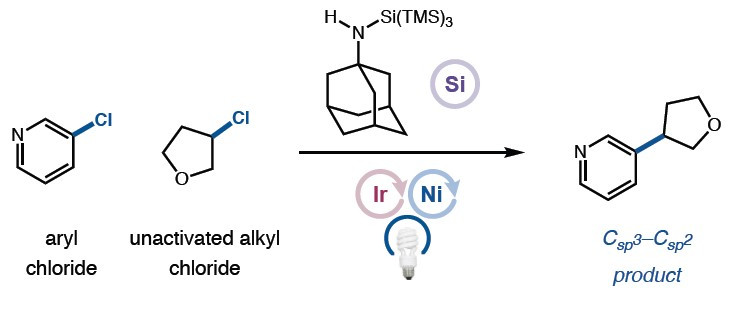
Cross-Electrophile Coupling of Unactivated Alkyl Chlorides
Holt A. Sakai, Wei Liu, Chi “Chip” Le, and David W. C. MacMillan*
J. Am. Chem. Soc. ASAP DOI: 10.1021/jacs.0c04812
正文
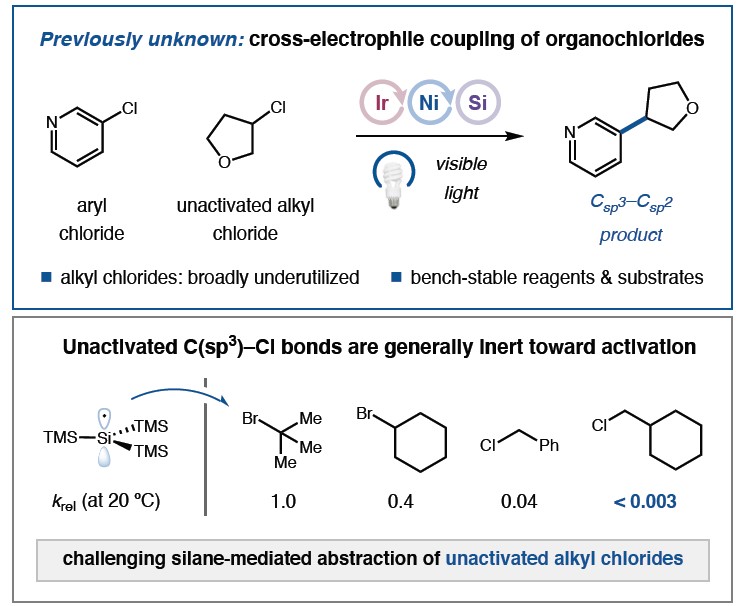
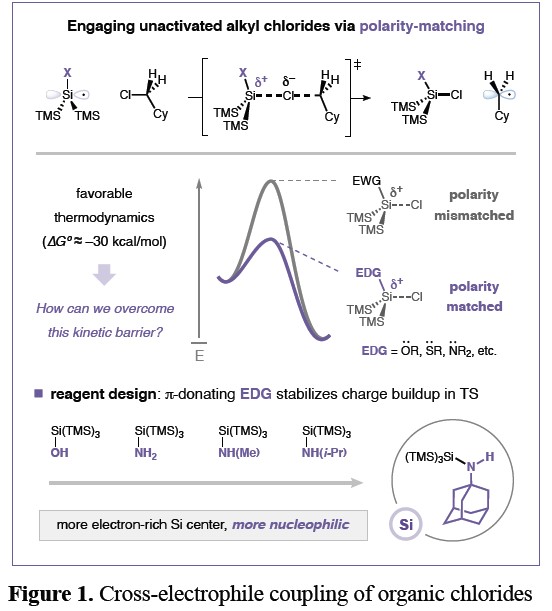
镍催化亲电偶联反应,已成为快速合成富含C(sp3)类药物分子的强大策略,同时能够引入所需的物理化学和药代动力学特性。Weix、Gong、Reisman等人,对该方法的可行性和合成实用性进行了研究,其中金属还原剂(如Zn或Mn)消除了对预官能化的需求,同时也避免了对空气敏感性有机金属试剂的需求。2016年,本课题报道了一种通过硅烷介导的溴原子抽取与镍/光氧化还原双重催化相结合,实现芳基溴化物和烷基溴化物之间的亲电偶联反应,可在温和的条件下,合成大量C(sp2)-C(sp3)偶联产物,同时,而该方法已在制药领域中广泛的应用。随后,一些利用了硅烷介导经卤素原子提取的亲电试剂也实现此类反应,如烷基-烷基偶联、三氟甲基化、烷基氟化以及烯烃氢氨磺酰化等。然而,与C(sp3)-溴化物、碘化物和磺酸盐相比,对于简单烷基氯化物的亲电偶联反应极少被研究。但是,与其相比,有机氯化物仍具备一些优势,如底物易得且丰富、毒性低、化学稳定性和耐受性好、生产成本低等。在金属还原剂介导的镍催化反应中,C(sp3)-Cl键可防止必要的氧化加成步骤,同时还原电势可阻止外层电子的转移。此外,在光氧化还原途径中甲硅烷基提取动力学过程中,由于C-Cl键低极化性,从而阻碍了氯原子的转移。如脂族溴化物通常会通过甲硅烷基自由基进行卤素原子的抽取,其速度要比相应的烷基氯快几个数量级(Figure 1)。为了克服这些限制,作者试图利用极性匹配来开发一种新型的硅烷试剂,以降低氯原子转移的动力学势垒。在此,普林斯顿大学David W. C. MacMillan教授课题组实现了第一个镍催化,使用廉价易得、低毒的烷基氯化物进行亲电偶联反应的例子。
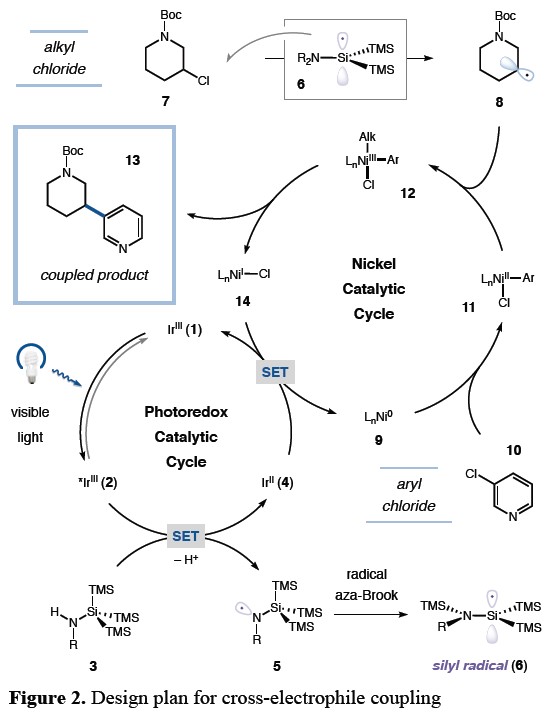
紧接着,作者提出了一种可能的反应机理(Figure 2)。首先,在可见光照射下,光催化剂[Ir(ppy)2(dtbbpy)](PF6)(1)转变为三重激发态2。作为反应的关键之处在于,*IrII与硅烷试剂3通过单电子转移(SET),形成IrII配合物4和N-自由基5,5再经aza-Brook自由基重排,从而获得关键的硅烷基自由基6(该自由基易于从脂肪族氯化物7中进行氯原子的抽取,获得相应的烷基自由基8)。同时,Ni0催化剂9与芳基氯10进行氧化加成,形成NiII-芳基中间体11。再与上述获得的烷基自由基8经氧化形成NiIII配合物12。最后,经还原消除,即可获得所需的C(sp2)-C(sp3)产物13。此外,通过IrII(4)对所得的NiI中间体14进行单电子还原,形成基态IrIII光催化剂(1),并再生Ni0催化剂9,从而完成整个催化循环过程。
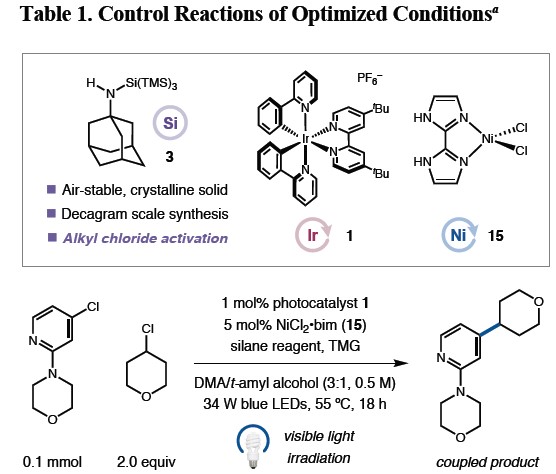
首先,作者以4-(4-氯吡啶-2-基)吗啉和4-氯四氢吡喃作为模型底物,分别对溶剂、光催化剂、配体、硅试剂等进行了筛选(Table 1)。筛选结果表明,当使用1 mol%的光催化剂1,5 mol%的NiCl2•bim催化剂15,使用1-金刚烷基氨基硅烷试剂3,TMG作为碱时,可获得73%收率的偶联产物(entry 1)。
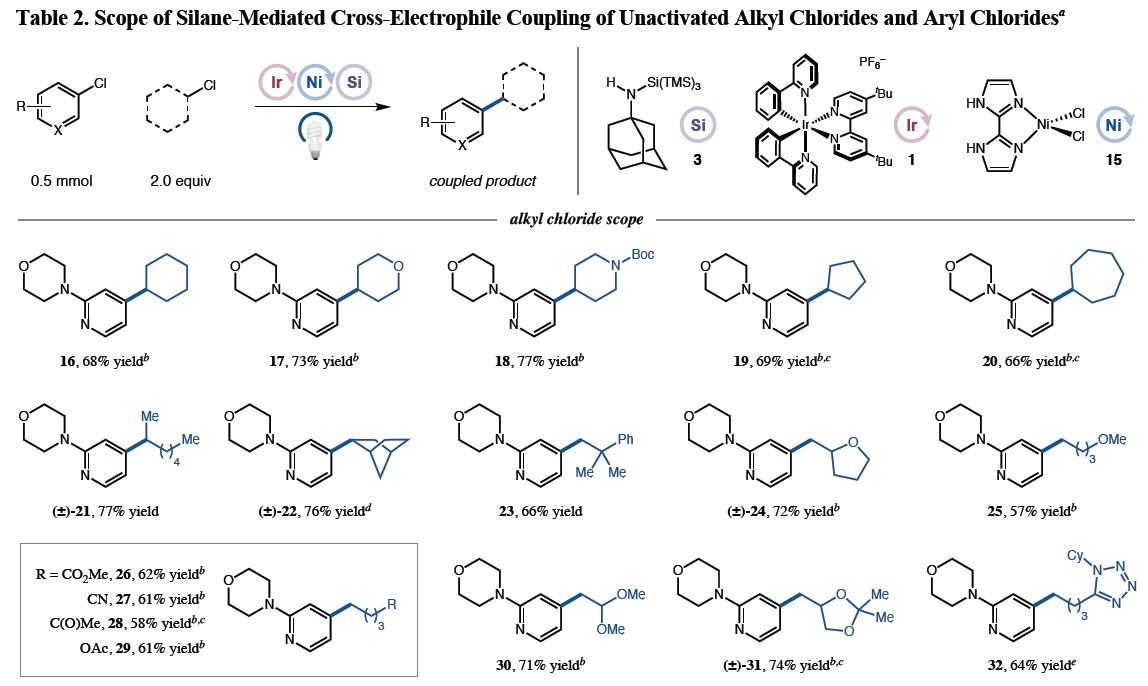
在获得上述最佳反应条件后,作者开始对烷基氯化物的底物范围进行了扩展(Table 2)。反应结果表明,具有五-七元环的烷基氯,均可以66-77%的收率获得产物16–20。同时,使用仲环烷基、位阻较大的双环氯化物底物时,也可获得76-77%收率的产物21–22。此外,对于伯烷基氯中卤原子的抽取在动力学上一直具有挑战性,但通过此方案也可实现相关C(sp2)-C(sp3)偶联,从而获得相应的产物23–32,同时一些活性的官能团(如酯、腈和酮)也具有良好的耐受性,从而为后期修饰提供了多种可能。
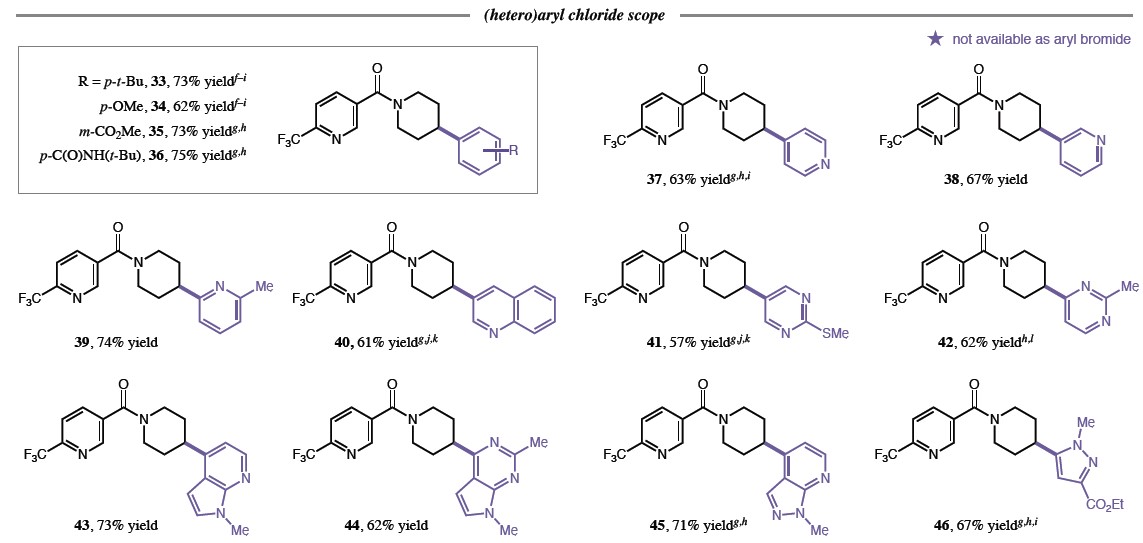
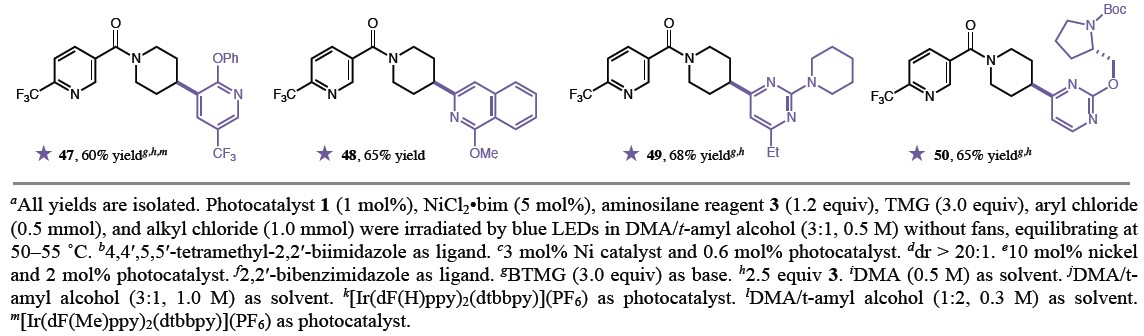
随后,作者对芳基氯化物的底物范围进行了相关的扩展(Table 2)。反应结果表明,具有给电子和缺电子的氯苯衍生物,均可以65-75%的收率获得产物33–36。同时,含有氯取代的氮杂环均可与体系兼容,从而获得相应的产物,如吡啶(37–39)、喹啉(40)、嘧啶(41–42,49–50)、吡咯并吡啶(43)、吡咯并嘧啶(44)、吡唑并吡啶(45)、吡唑(46)、吡啶(47)、异喹啉(48)。值得注意的是,许多杂芳基氯化物可以很容易地使用,而相应的芳基溴化物则无法从市场上买到,从而进一步说明了该方法的实用性(47–50)。
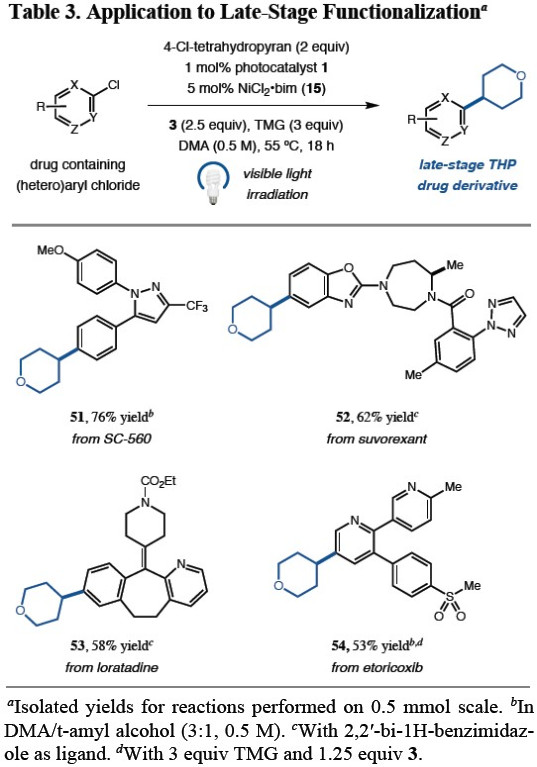
最后,为了进一步证明该方法的合成实用性,作者对一些含有氯化物的药物分子进行了相关的后期修饰(Table 3)。反应结果表明,一些药物分子均可通过该方案进行相关的C(sp2)-C(sp3)偶联反应,从而获得53-76%收率相应的产物51–54。因此,该方法在药物化学领域将会得到广泛的应用。
总结
普林斯顿大学David W. C. MacMillan教授课题组报道了一种新型1-金刚烷基氨基硅烷试剂,可在温和的光催化条件下进行烷基氯原子的抽取,从而实现与芳基氯化物的亲电偶联反应,获得多种C(sp2)-C(sp3)偶联产物。同时,该反应可使用一些低毒、丰富且市售的有机氯化物作为底物(而相应的芳基溴化物则无法从市场上买到)。此外,通过对相关药物分子的后期修饰,进一步证明了该反应实用性。
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!




















No comments yet.