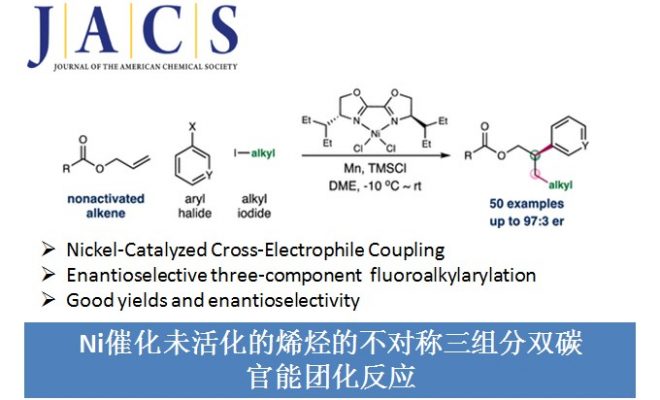
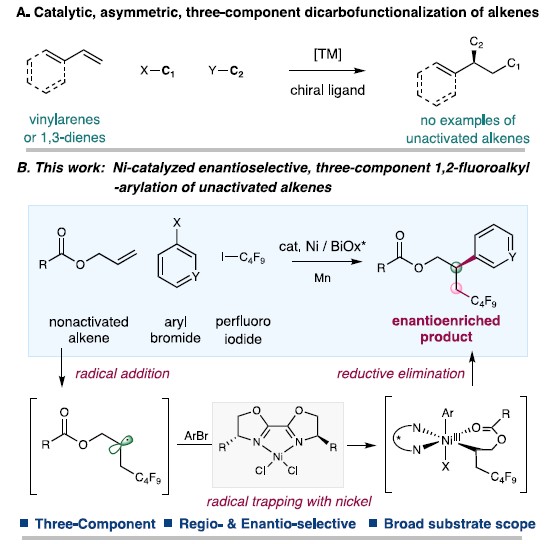
过渡金属催化烯烃的双碳官能团化反应能快速将简单的烯烃化合物转化为含有两个相邻sp3C-C键的复杂分子,但该类反应特别是三组分反应产物的立体选择性均不高,仍然面临着巨大的挑战。手性过渡金属可催化活化的乙烯基芳烃发生不对称三组分双碳官能团化反应,但该策略不适合未活化的烯烃[1]。未活化烯烃的不对称双碳官能团化反应主要局限于分子内或两组分,还没有关于未活化烯烃的不对称三组分双碳官能团化反应。因此,东华大学储玲玲课题组报道了Ni催化未活化的烯烃、芳基卤化物与全氟烷基碘化物发生交叉亲电偶合反应。这是首例过渡金属催化未活化烯烃的不对称三组分双碳官能团化反应(Figure 1)。相关研究成果发表于
“Enantioselective Three-Component Fluoroalkylarylation of Unactivated Olefins through Nickel-Catalyzed Cross-Electrophile Coupling”
Tu, H.-Y.; Wang, F.; Huo, L.; Li, Y.; Zhu, S.; Zhao, X.; Li, H.; Qing, F.-L.; Chu, L.* J. Am. Chem. Soc. 2020, Early View. DOI: 10.1021/jacs.0c03708
Figure 1 背景反应
论文作者介绍
储玲玲特聘研究员
研究经历
- 2012年,毕业于中国科学院上海有机化学研究所
- 2013年-2016年,在美国普林斯顿大学化学系从事博士后研究
- 2016年9月,加入东华大学,任特聘研究员,博士生导师
荣誉及获奖情况
- 2017年,上海市自然科学奖一等奖(排名第二)
- 2013年,中国科学院优秀博士学位论文
- 2012年,中国科学院优秀毕业生
- 2011年,中国科学院院长奖学金
近年来承担的主要科研项目
- 国家自然科学基金青年基金(21702029)
- 2017年上海市青年科技英才“扬帆计划”项目(17YF1400100)
研究方向
- 1.过渡金属催化
- 2.有机含氟功能材料
论文概要
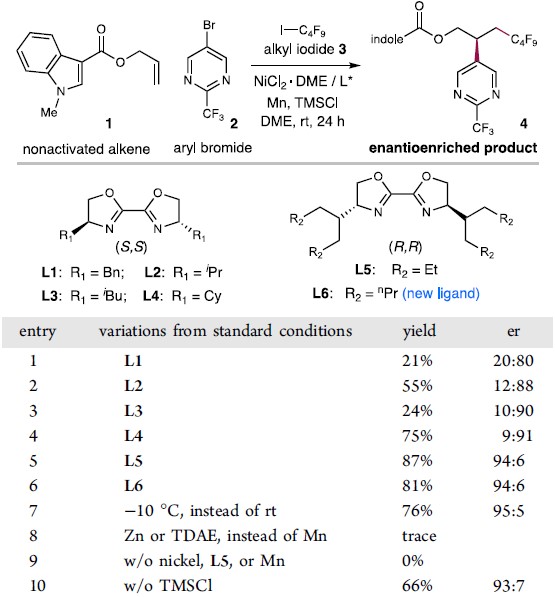
以烯丙基酯1、5-溴-2-(三氟甲基)嘧啶2和C4F9I为模板底物,作者对催化剂、手性配体以及溶剂等反应条件进行反复筛选,确定最优反应条件(Table 1):10 mol% NiCl2·DME为催化剂,12 mol% 手性二噁唑啉L5为手性配体,2.5 equiv Mn和0.1 equiv TMSCl为添加物,DME为溶剂,在-10℃条件下反应24小时,能以76%的收率和90%的对映选择性得到产物4。
在最优反应条件下,作者对芳基卤化物的底物范围进行了考察。各种吸电子或给电子取代的5-溴嘧啶、邻位取代的吡啶和喹啉能较好地适应反应条件,能以良好至优秀的收率和对映选择性得到相应手性β-氟烷基芳基烷烃。但电中性取代和给电子取代的芳基碘化物只能以中等的收率和良好的对映选择性得到相应产物,且简单的2-溴吡啶不能适应反应条件,这说明2-取代的芳基卤化物是该反应发生的必要条件。紧接着,作者考察了全氟烷基卤化物和未活化烯烃的底物范围。各种长度的全氟烷基卤化物均能较好的适应反应条件,能以良好至优秀的对映选择性得到相应产物,但随着烷基链长度变长,相应产物的收率会逐渐降低。同时,各种吲哚-3-羧酸衍生的烯丙酯、苯甲酸酯、碳酸盐、氨基甲酸酯取代的烯丙酯均能较好的适应反应条件,能以能以良好至优秀的收率和对映选择性得到相应产物。但1,1-二取代烯烃和1,2-二取代的内烯烃不能适应反应条件。
Table 1. 条件筛选
为了证明反应的应用潜力,作者进行了扩大化反应和衍生反应(Scheme 3)。扩大化反应产物的收率和对映选择性与模板反应产物的收率和对映选择性保持一致。产物29的酯基在K2CO3的MeOH溶液中发生水解生成γ-氟代烷基-β-芳基醇56。56又可转化为烷基氯57和溴化物58。同时,56和苯基二硫化物或邻苯二甲酰亚胺反应可分别得到氟烷基酰胺59和氟烷基硫醇60。
Scheme 3 衍生反应
论文总结评价
东华大学储玲玲课题组报道了Ni催化未活化的烯烃、芳基卤化物与全氟烷基碘化物发生交叉亲电偶合反应,能以良好至优秀的收率和对映选择性得到一系列手性β-氟烷基芳基烷烃。这是首例过渡金属催化未活化烯烃的不对称三组分双碳官能团化反应。
参考文献
- [1] (a) Zhang, Z. Q.; Meng, X. Y.; Sheng, J.; Lan, Q.; Wang, X. S. Org. Lett. 2019, 21, 8256-8260. DOI: 10.1021/acs.orglett.9b03012 (b) Anthony, D.; Lin, Q.; Baudet, J.; Diao, T. Angew. Chem., Int. Ed. 2019, 58, 3198-3202. DOI: 10.1002/anie.201900228
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!


























No comments yet.