小编 孙苏赟
羟醛缩合,又叫aldol反应,应该算是有机化学中很重要的一个形成C-C单键的方法,关于它的一些基本内容之前在此前chemstation已经有了一些很好的介绍。见 碳碳键构筑的王道反应:羟醛缩合反应(Aldol reaction) 系列
今天在这里给大家介绍一些之前没有提到的一些已有内容的扩充。本文是这个系列的第一部分,为大家简要介绍锂烯醇和两种硼烯醇在Aldol反应中的立体选择性。
1.酸或碱催化的交叉aldol缩合
关于aldol交叉缩合反应的经典条件与其难点,请参见羟醛缩合反应(Aldol reaction) 系列 第一弹
2.手性选择导向的aldol缩合反应
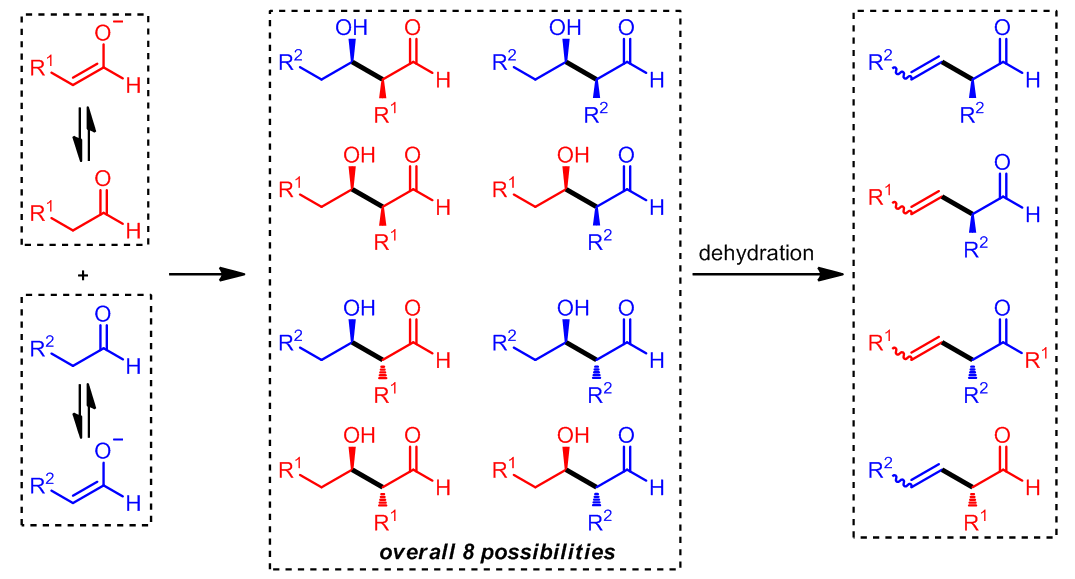
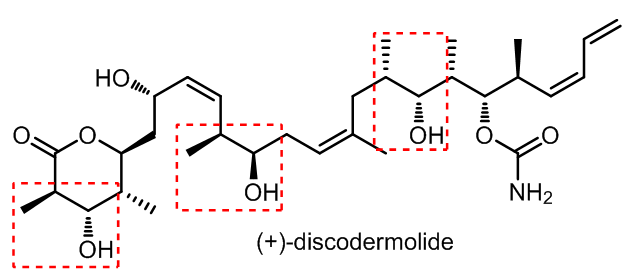
在交叉aldol缩合中会产生两种具有反应活性的烯醇中间体,对于这两种烯醇中间体的控制可以直接影响aldol的受体和供体,这就叫做导向的aldol缩合反应。此外,反应的立体选择性也是可控的,这使得aldol反应在有机合成中具有更加广泛的应用,例如在(+)-discodermolide的结构中就有三个可以考虑用aldol反应进行的结构片段:
i. 利用锂烯醇进行反应选择性
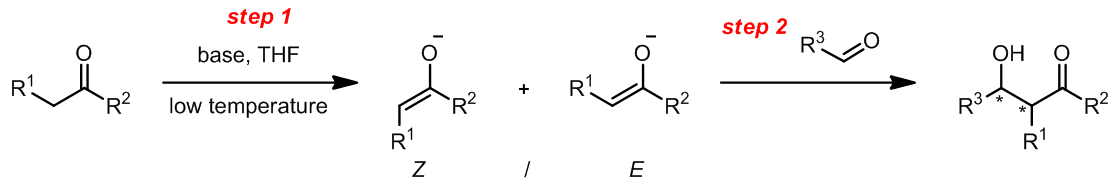
在低温,羰基化合物倾向于和碱生成动力学控制的烯醇产物,这时候另外一个羰基化合物再加入到反应体系中,再将温度逐渐升高,就可以得到aldol缩合产物。通常来说,烯醇化的过程是要比亲核加成要快的,因此可以控制反应的立体选择性。
一般的策略是:
其中,aldol产物的syn/anit-选择性是和烯醇的构形密切相关的,而在动力学条件下,烯醇的构形和反应底物的结构由很大的关系:
一般来讲,在热力学的条件下,Z-烯醇倾向于得到syn-aldol产物,而E-烯醇倾向于得到anti-aldol产物。
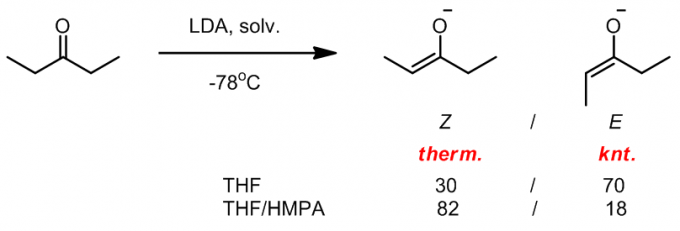
溶剂也会影响烯醇的构形:
HMPA可以减小Li+的配位作用而得到Z-烯醇,而在THF中他们的作用却很强烈,倾向于得到E-烯醇。
此外,烯醇化的过程是通过六元环的过渡态进行的,其详细的机理和立体选择性参见羟醛缩合反应(Aldol reaction) 系列
这里补充一下Z/E-锂烯醇的aldol缩合的立体选择性的差异:
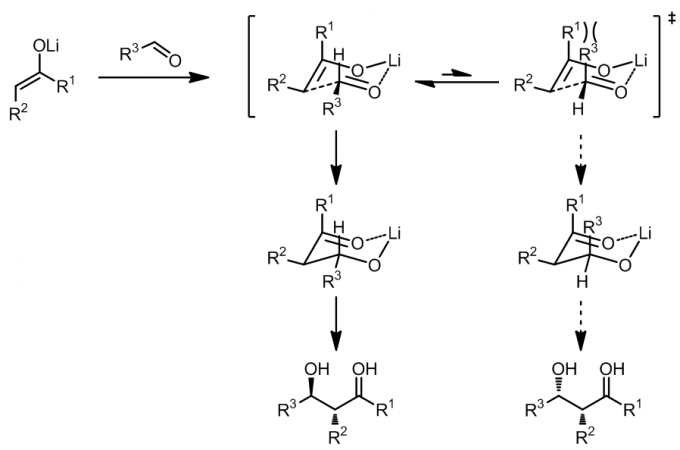
(1) E-锂烯醇
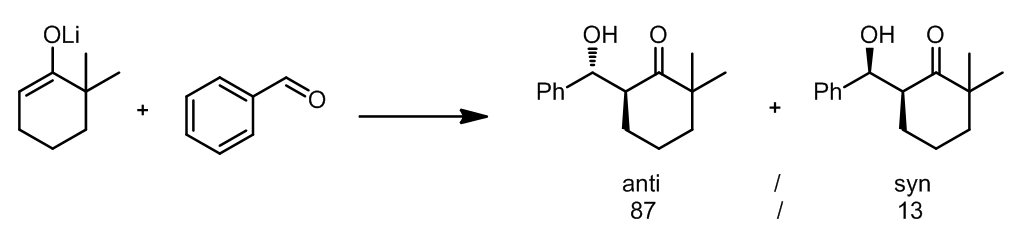
E-烯醇的反应通常会经过一个扭船形的过渡态,这样的能量较椅式过渡态更低,因此E-烯醇反应的选择性不如对应的Z-烯醇其,例如:
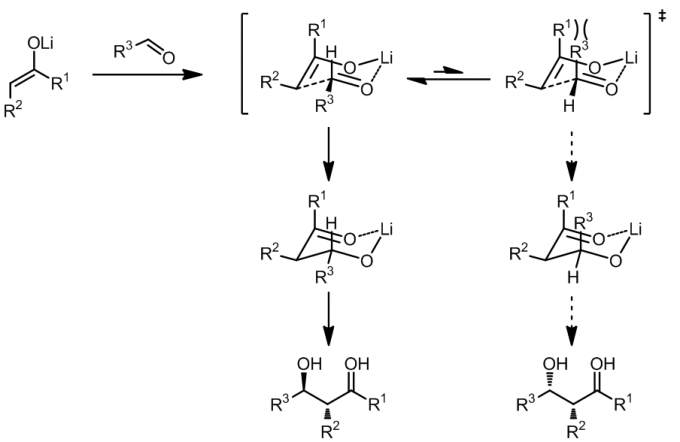
(2) Z-锂烯醇:Z-烯醇在实际上更加容易得到,反应的选择性也更好一些(倾向于生成syn-aldol)
ii. 硼烯醇反应的立体选择性
a. Z-硼烯醇
在烯醇化的过程中,有硼的参与更加倾向于生成Z-烯醇,此外,因为B-O键较Li-O键更加短,位阻效应就被放大了,因此产物的syn/anti比例就更大了,也就是说反应的立体选择性比锂烯醇更好,例如:
反应机理和过渡态:
一般来说,虽然烯醇的构形是基本确定的,但是反应过程还有以下三个因素需要考虑:
- 1.位阻效应,譬如烯丙基体系中的重叠效应
- 2.电子效应,例如偶极弱化等
- 3.立体电子效应,超共轭效应等
反应的实例[1]:
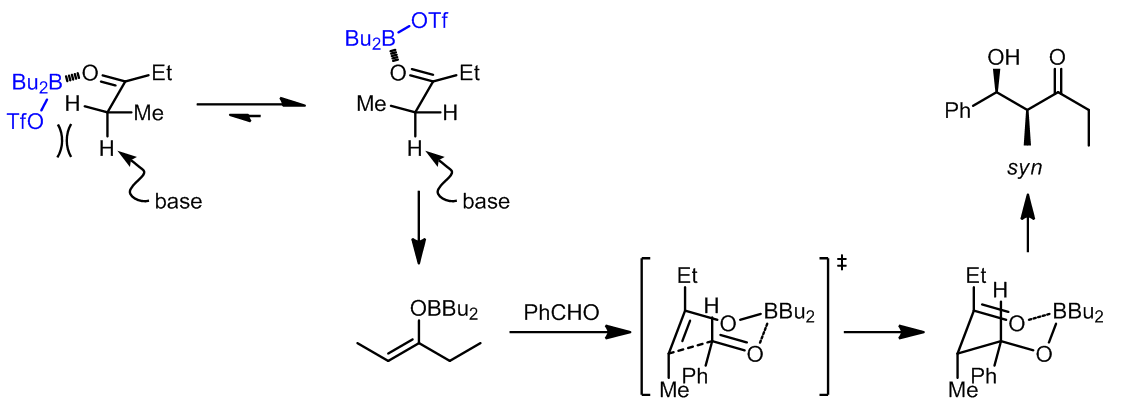
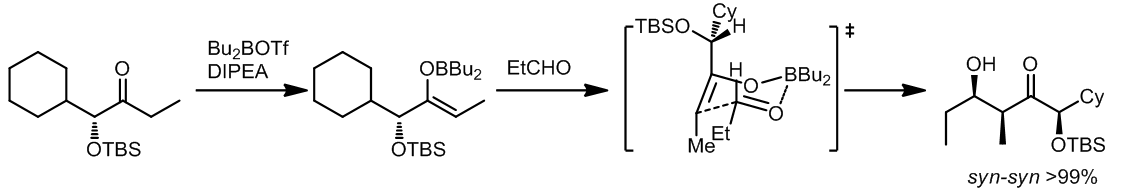
a. E-硼烯醇
在这些实例中,Zimmerman-Traxler提出的模型可以解释反应的立体花雪,反应中最重要的是甲基,同时也和参与反应的金属离子有关。[2]
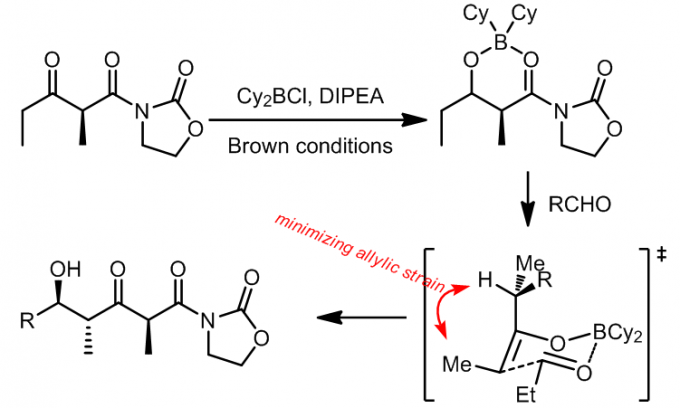
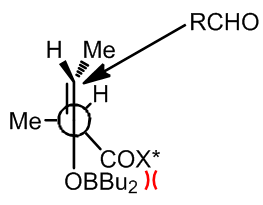
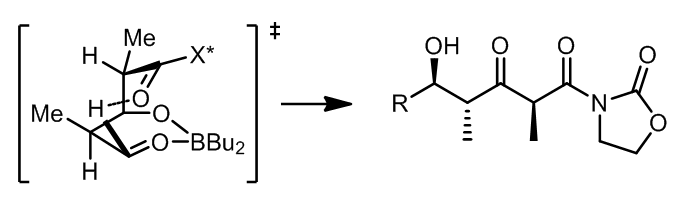
烯醇化过程中使用的是Bu2OTf/DIEPA,那么生成的烯醇的构形是相反的。但是这个反应的后半部分的结果也是有些出乎意料的,但是利用Houk的模型来解释反应的面选择性是很好的:
通过计算之后的结论是更加可靠的情形是反应经过船形过渡态,如果Bu2BOTf作为硼试剂,那么可以有利的支持这个观点:
参考文献:
- Angew. Chem. Int. Engl. Ed., 1980, 19, 557, DOI; 10.1002/anie.198005571
- J. Am. Chem. Soc., 1990, 112(2), pp 866–868, DOI: 10.1021/ja00158a056
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载!

























No comments yet.