作者:杉杉
导读:
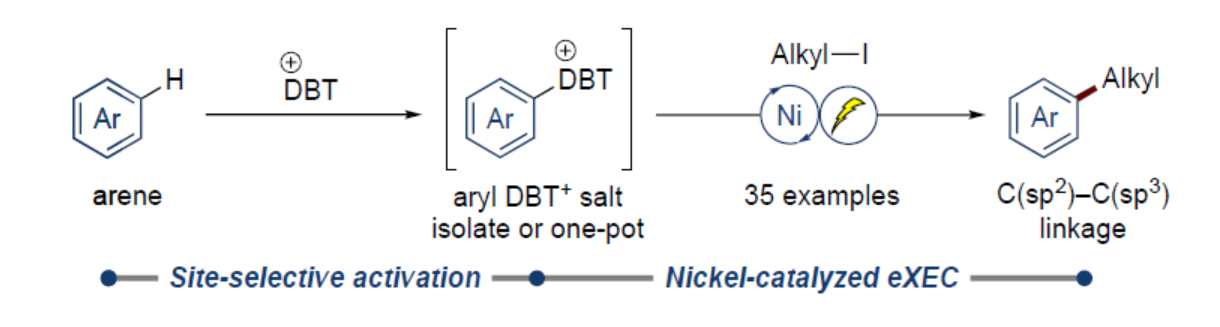
近日,德国哥廷根大学(Georg-August-Universität Göttingen)的Lutz Ackermann课题组在Angew. Chem. Int. Ed.中发表论文,报道一种全新的镍电催化arylsulfonium salts与烷基碘的C(sp2)–C(sp3)交叉亲电偶联反应方法学,进而成功完成一系列具有烷基取代芳烃分子的构建。此外,采用非预官能团化芳烃,通过生成aryldibenzothiophenium salts (DBT+),也可实现相应的烷基化过程。
Electrocatalytic Formal C(sp2)–H Alkylations via Nickel-Catalyzed Cross-Electrophile Coupling with Versatile Arylsulfonium Salts
T. Michiyuki, S. L. Homölle, N. K. Pandit, L. Ackermann, Angew. Chem. Int. Ed. 2024, ASAP. doi: 10.1002/anie.202401198.
正文:
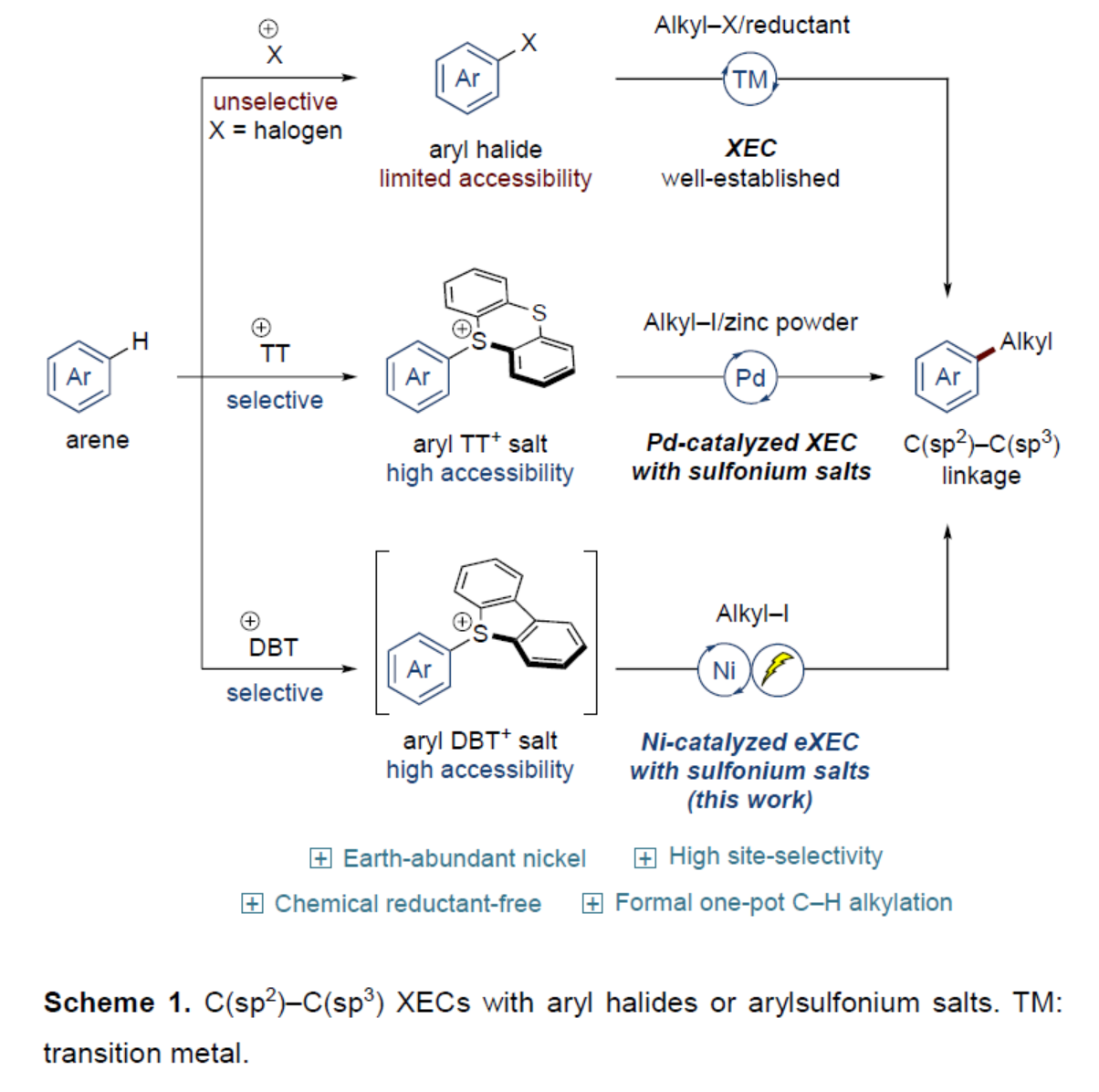
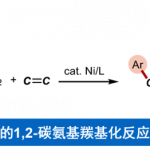
近年来,诸多研究团队利用使用化学还原剂[1]、光化学[2]或电化学[3]策略,实现了有机卤化物的交叉亲电偶联反应方法学 (Scheme 1, top)。然而,对于此类反应的反应物的位点选择性卤化仍具有难度。受到近年来对于钯催化arylthianthrenium (aryl TT+)的位点选择性烷基化反应方法学[4] (Scheme 1, middle)相关研究报道的启发,这里,德国哥廷根大学(Georg-August-Universität Göttingen)的Lutz Ackermann课题组在报道一种全新的镍电催化arylsulfonium salts与烷基碘的C(sp2)–C(sp3)交叉亲电偶联反应方法学,进而成功完成一系列具有烷基取代芳烃分子的构建 (Scheme 1, bottom)。
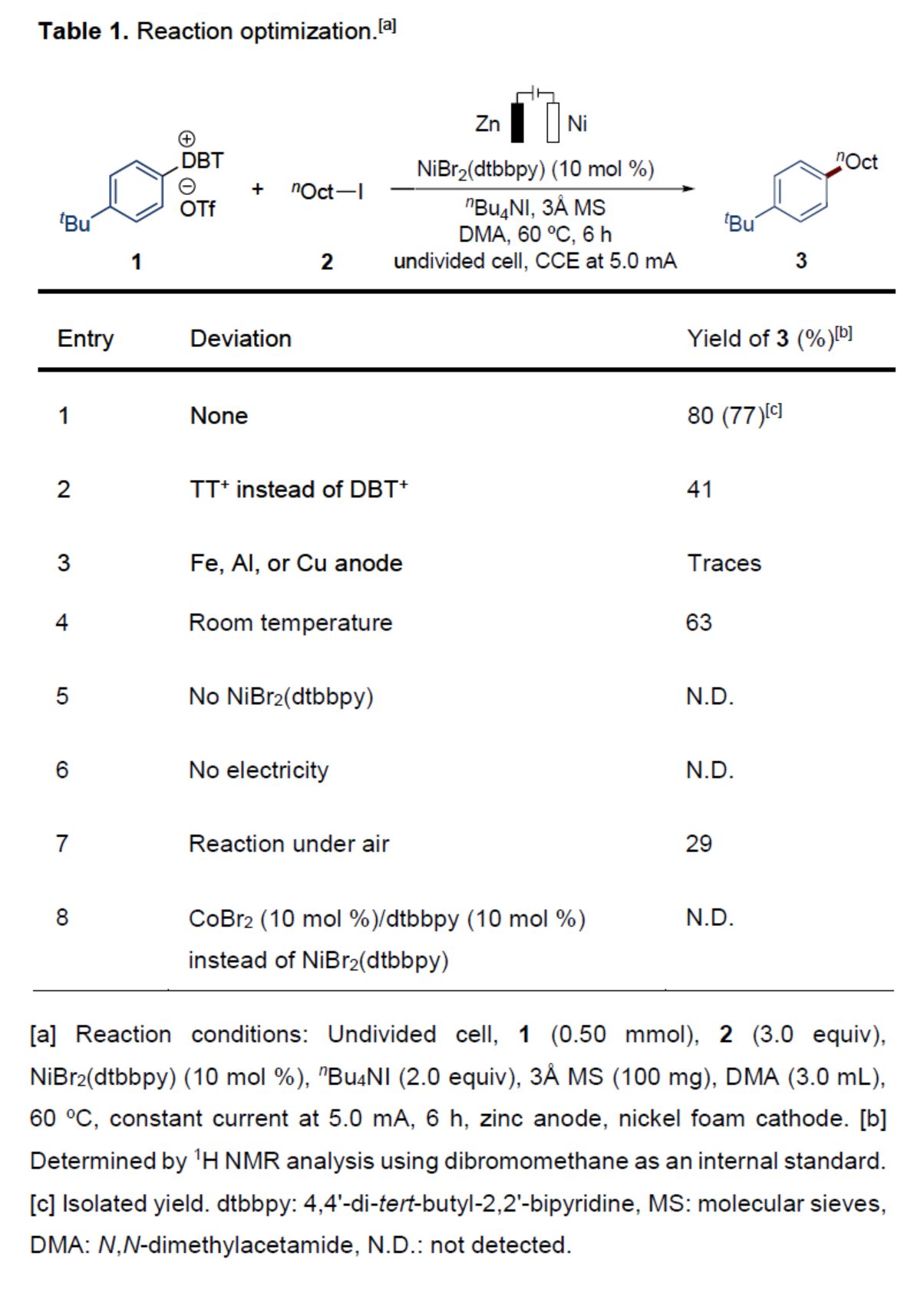
首先,作者采用aryldibenzothiophenium 1与1-碘辛烷2作为模型底物,进行相关反应条件的优化筛选 (Table 1)。进而确定最佳的反应条件为:采用NiBr2(dtbbpy)作为催化剂,Zn/Ni作为电极,nBu4NI作为电解质,3Å MS作为添加剂,电流为5 mA,在DMA反应溶剂中,反应温度为60 oC,最终获得80%收率的产物3。
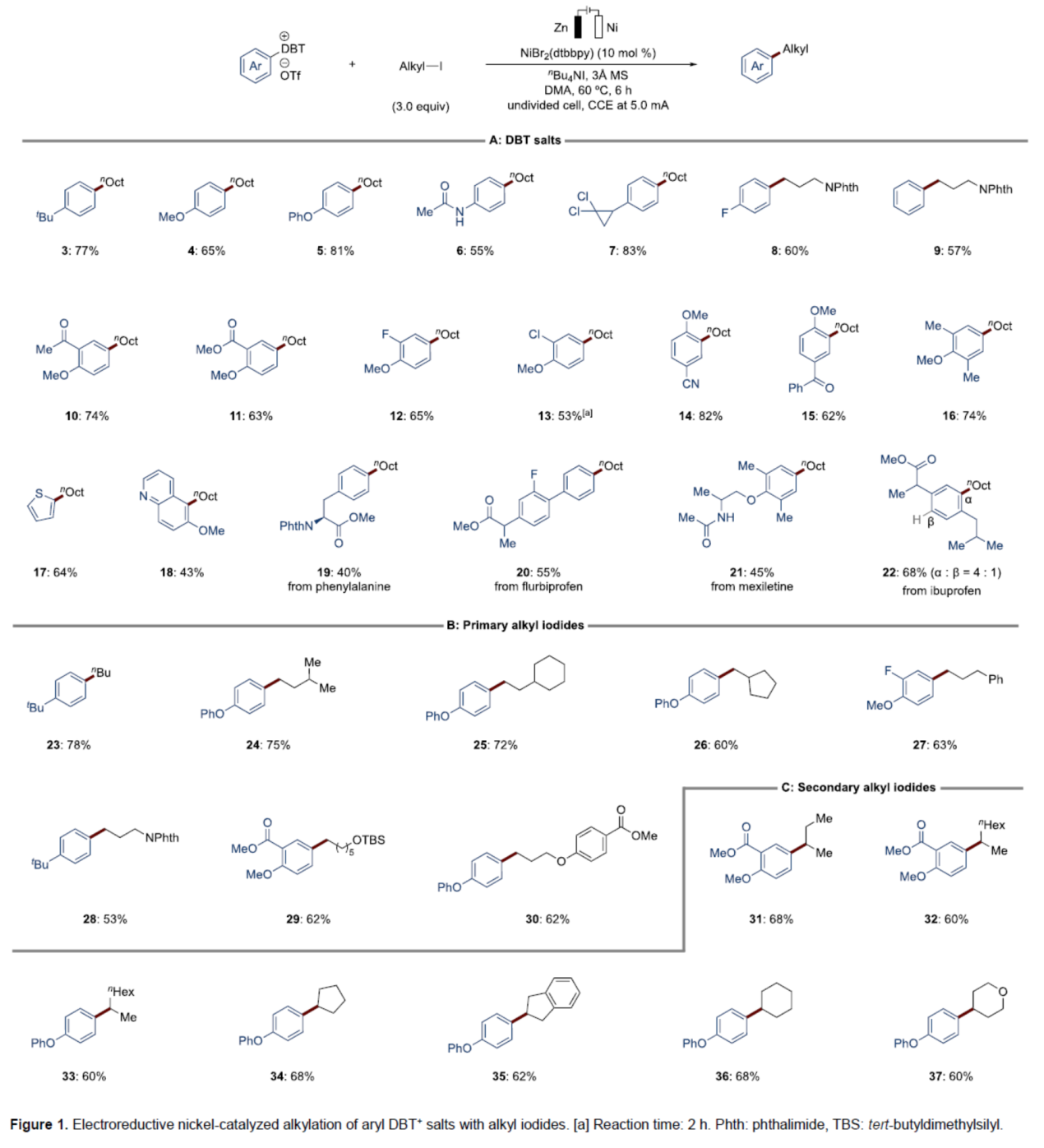
在上述的最佳反应条件下,作者分别对一系列芳基DBT+盐底物以及烷基碘底物 (Figure 1)的应用范围进行深入研究。

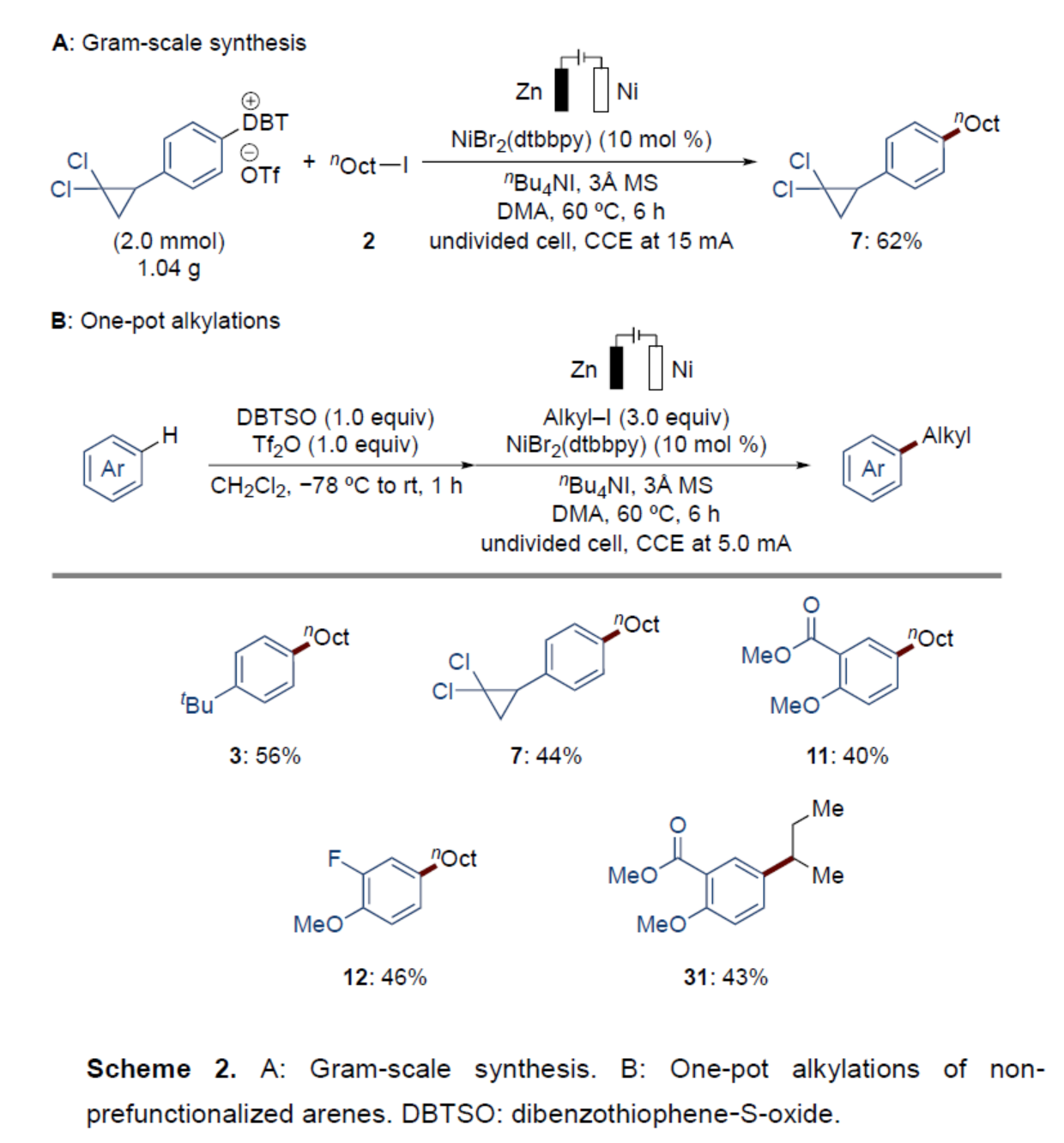
之后,该小组通过如下克级实验以及一锅烷基化反应的研究进一步表明,这一全新的偶联略具有潜在的合成应用价值 (Scheme 2)。
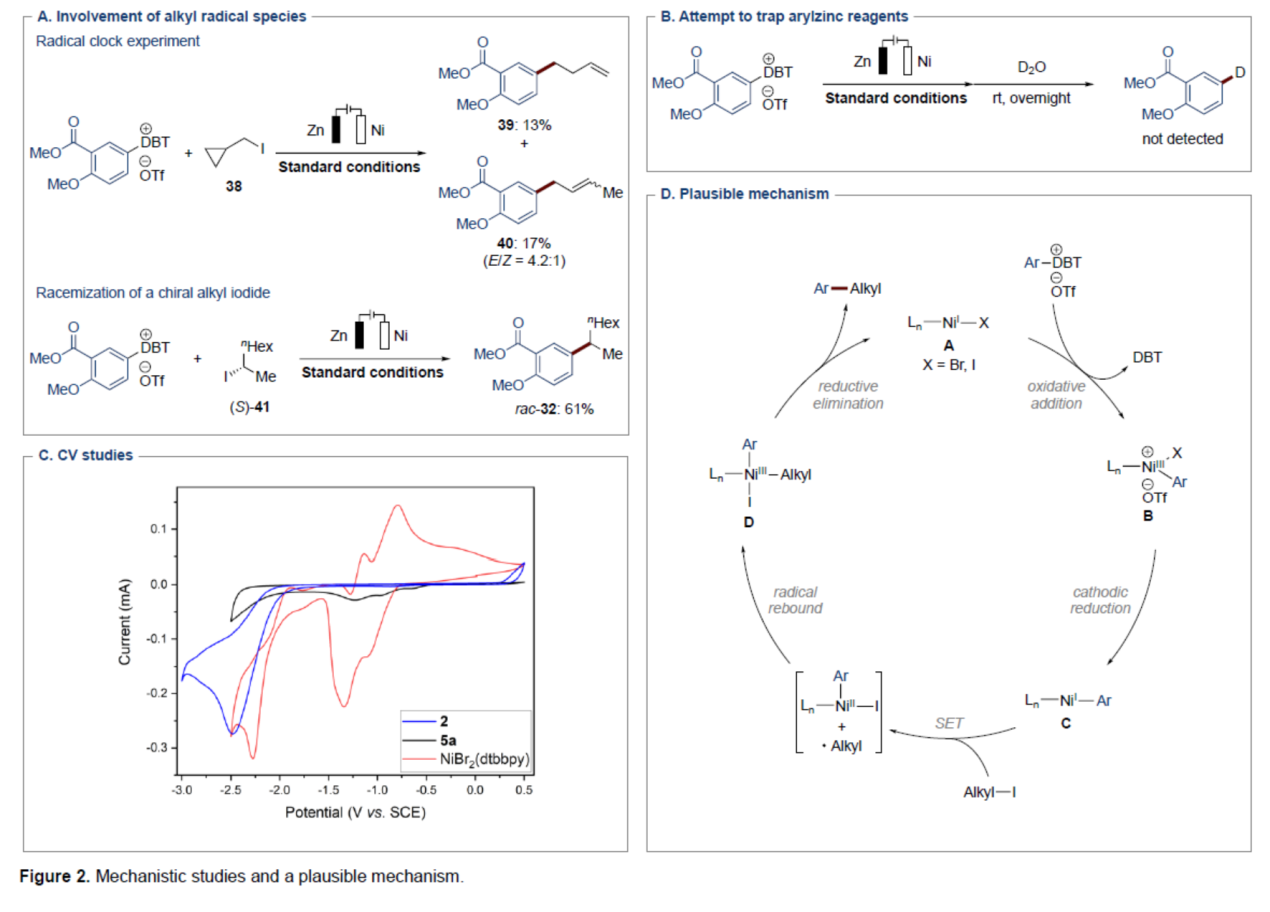
接下来,作者对上述偶联过程的反应机理进行进一步研究 (Figures 2A-2C)。基于上述的实验研究以及前期相关的文献报道[5],作者提出如下合理的反应机理 (Figure 2D)。

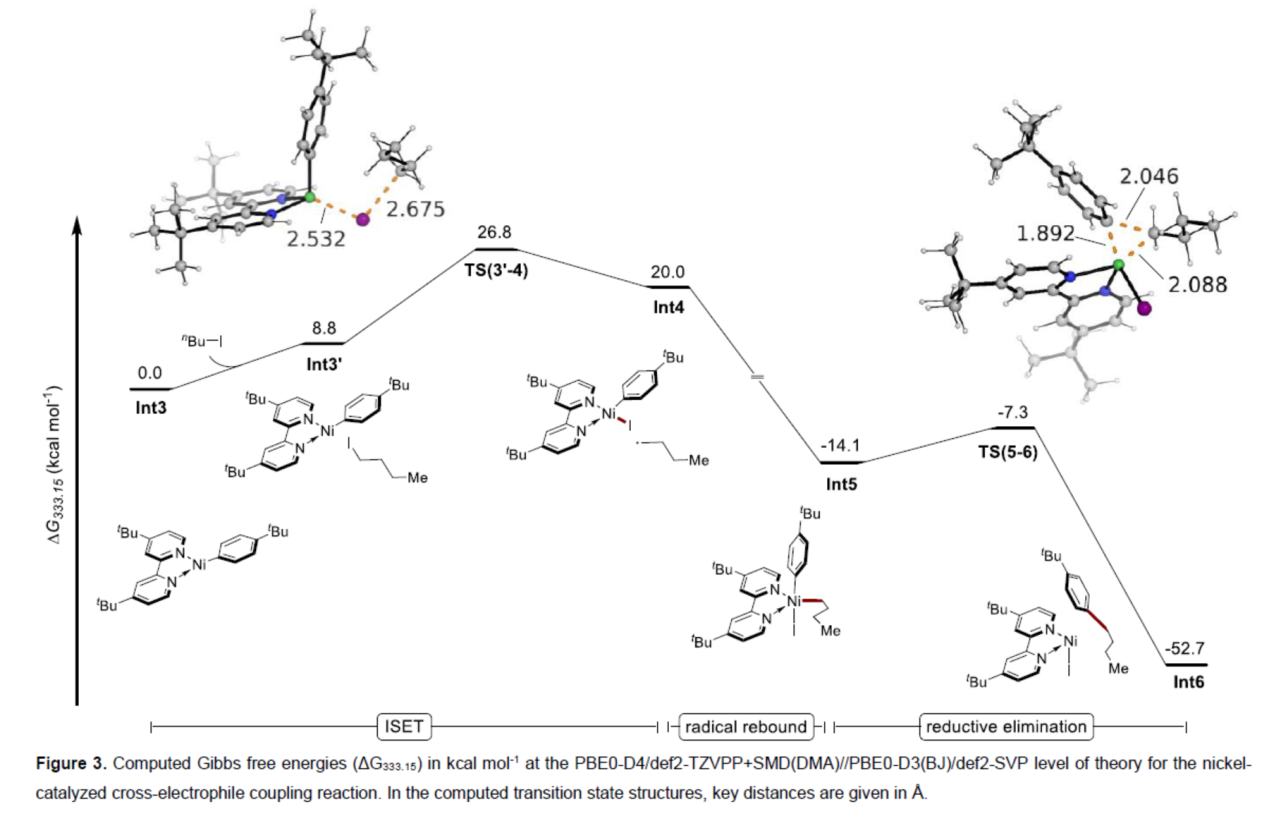
最后,作者对上述的反应机理进行了相关理论计算的研究 (Figure 3)。
总结:德国哥廷根大学(Georg-August-Universität Göttingen)的Lutz Ackermann课题组在报道一种全新的镍电催化arylsulfonium salts与烷基碘的C(sp2)–C(sp3)交叉亲电偶联反应方法学,进而成功完成一系列具有烷基取代芳烃分子的构建。这一全新的偶联合成转化策略具有底物范围广泛、优良的官能团兼容性以及高度的化学选择性等优势。
参考文献:
- [1] S. Kim, M. J. Goldfogel, M. M. Gilbert, D. J. Weix, J. Am. Chem. Soc. 2020, 142, 9902. doi: 10.1021/jacs.0c02673.
- [2] H. A. Sakai, W. Liu, C. Le, D. W. C. MacMillan, J. Am. Chem. Soc. 2020, 142, 11691. doi: 10.1021/jacs.0c04812.
- [3] R. J. Perkins, D. J. Pedro, E. C. Hansen, Org. Lett. 2017, 19, 3755. doi: 10.1021/acs.orglett.7b01598.
- [4] B. Lansbergen, P. Granatino, T. Ritter, J. Am. Chem. Soc. 2021, 143, 7909. doi: 10.1021/jacs.1c03459.
- [5] S. Ni, J. Yan, S. Tewari, E. J. Reijerse, T. Ritter, J. Cornella, J. Am. Chem. Soc. 2023, 145, 9988. doi: 10.1021/jacs.3c02611.
本文版权属于 Chem-Station化学空间, 欢迎点击按钮分享,未经许可,谢绝转载.
















No comments yet.